
- •14.Предмет изучения молекулярной физики.
- •3 Основных положения молекулярно - кинетической теории:
- •15. Уравнение состояния идеального газа
- •16. Основное уравнение мкт
- •17.Среднекинетическая энергия молекул идеального газа
- •Внутренняя энергия термодинамической системы
- •18. Теплоемкость идеального газа.
- •19. Явления переноса.
- •20. Работа в термодинамике.
- •21. Содержание первого начала термодинамики.
- •22.Адиабатический процесс.
- •23. Второе начало термодинамики.
21. Содержание первого начала термодинамики.
Первое начало термодинамики — один из трёх основных законов термодинамики, представляет собой закон сохранения энергии для термодинамических систем. Согласно первому началу термодинамики, термодинамическая система может совершать работу только за счёт своей внутренней энергии или каких-либо внешних источников энергии. Первое начало термодинамики часто формулируют как невозможность существования вечного двигателя первого рода, который совершал бы работу, не черпая энергию из какого-либо источника.
Формулировка
Существует несколько эквивалентных формулировок первого начала термодинамики
В любой изолированной системе запас энергии остаётся постоянным.[2] Это — формулировка Дж. П. Джоуля (1842 г.).
Количество теплоты, полученное системой, идёт на изменение её внутренней энергии и совершение работы против внешних сил
Изменение внутренней энергии системы при переходе её из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе, то есть, оно зависит только от начального и конечного состояния системы и не зависит от способа, которым осуществляется этот переход. Это определение особенно важно для химической термодинамики[2] (ввиду сложности рассматриваемых процессов). Иными словами, внутренняя энергия является функцией состояния. В циклическом процессе внутренняя энергия не изменяется.
![]()
Изменение
полной энергии системы в квазистатическом
процессе равно
количеству теплоты
,
сообщённому системе, в сумме с изменением
энергии, связанной с количеством
вещества
при химическом
потенциале ![]() ,
и работы
,
и работы ![]() [3],
совершённой над системой внешними
силами и полями,
за вычетом работы
[3],
совершённой над системой внешними
силами и полями,
за вычетом работы ![]() ,
совершённой самой системой против
внешних сил
,
совершённой самой системой против
внешних сил
![]() .
.
Применение
первого начала термодинамики к
изопроцессам
Рассмотрим
применение первого закона термодинамики
к изопроцессам, происходящим с идеальным
газом.
В изотермическом процессе температура
постоянная, следовательно, внутренняя
энергия не меняется. Тогда уравнение
первого закона термодинамики примет
вид: ![]() ,
т. е. количество теплоты, переданное
системе, идет на совершение работы при
изотермическом расширении, именно
поэтому температура не изменяется.
В изобарном процессе газ расширяется
и количество теплоты, переданное газу,
идет на увеличение его внутренней
энергии и на совершение им
работы:
,
т. е. количество теплоты, переданное
системе, идет на совершение работы при
изотермическом расширении, именно
поэтому температура не изменяется.
В изобарном процессе газ расширяется
и количество теплоты, переданное газу,
идет на увеличение его внутренней
энергии и на совершение им
работы: ![]() .
При изохорном процессе газ не меняет
своего объема, следовательно, работа
им не совершается, т. е. А = 0, и уравнение
первого закона имеет вид
.
При изохорном процессе газ не меняет
своего объема, следовательно, работа
им не совершается, т. е. А = 0, и уравнение
первого закона имеет вид ![]() ,
т. е. переданное количество теплоты идет
на увеличение внутренней энергии газа.
,
т. е. переданное количество теплоты идет
на увеличение внутренней энергии газа.
22.Адиабатический процесс.
Адиабати́ческий,
или адиаба́тный
проце́сс (от др.-греч. ἀδιάβατος —
«непроходимый») — термодинамический
процесс в
макроскопической системе, при котором
система не обменивается тепловой
энергией с
окружающим пространством .
![]() Серьёзное
исследование адиабатических процессов
началось в XVIII веке[1].
Серьёзное
исследование адиабатических процессов
началось в XVIII веке[1].
Адиабатический процесс является частным случаем политропного процесса, так как при нём теплоёмкость газа равна нулю и, следовательно, постоянна[2]. Адиабатические процессы обратимы только тогда, когда в каждый момент времени система остаётся равновесной (например, изменение состояния происходит достаточно медленно) и изменения энтропии не происходит. Некоторые авторы (в частности, Л. Д. Ландау) называли адиабатическими толькоквазистатические адиабатические процессы[3].
Уравнение Пуассона для идеального газа
Адиабата Пуассона
Для идеальных газов, чью теплоёмкость можно считать постоянной, в случае квазистатического процесса адиабата имеет простейший вид и определяется уравнением[6][15][16]
![]()
где
—
его объём, ![]() — показатель
адиабаты,
— показатель
адиабаты, ![]() и
и ![]() — теплоёмкости газа
соответственно при постоянном давлении
и постоянном объёме.
— теплоёмкости газа
соответственно при постоянном давлении
и постоянном объёме.
![]()
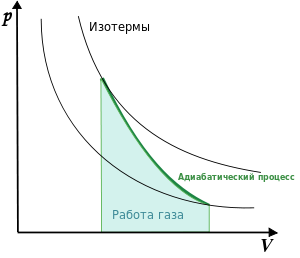
График
адиабаты (жирная линия) на ![]() диаграмме
для газа.
—
давление газа;
—
объём.
диаграмме
для газа.
—
давление газа;
—
объём.
С учётом уравнения состояния идеального газа уравнение адиабаты может быть преобразовано к виду
![]()
где — абсолютная температура газа. Или к виду
![]()
Поскольку ![]() всегда
больше 1, из последнего уравнения следует,
что при адиабатическом сжатии (то есть
при уменьшении
)
газ нагревается (
возрастает),
а при расширении — охлаждается, что
всегда верно и для реальных газов.
Нагревание при сжатии больше для того
газа, у которого больше коэффициент
.
всегда
больше 1, из последнего уравнения следует,
что при адиабатическом сжатии (то есть
при уменьшении
)
газ нагревается (
возрастает),
а при расширении — охлаждается, что
всегда верно и для реальных газов.
Нагревание при сжатии больше для того
газа, у которого больше коэффициент
.
Вывод уравнения
Согласно закону Менделеева — Клапейрона[6] справедливо соотношение
![]()
где R — универсальная газовая постоянная. Продифференцировав обе части, получаем
-
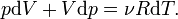
(3)
Если
в (3) подставить ![]() из (2),
а затем
из (2),
а затем ![]() из (1),
получим
из (1),
получим
![]()
или, введя коэффициент :
![]() .
.
Это уравнение можно переписать в виде
![]()
что после интегрирования даёт уравнение
![]() .
.
Окончательно получаем
![]()
что и требовалось доказать
