
- •23. Собственный механический и магнитный моменты электрона.
- •24 Полный механический и магнитный моменты электрона. Принцип Паули
- •25. Распределение электронов в атоме по состояниям. Таблица Менделеева.
- •7. Давление света.
- •8. Гипотеза де Броиля.Волновой пакет частиц.
- •11. Операторы.
- •12 Собственные волновые функции и собственные значения физических величин. Собственные волновые функции оператора компоненты импульса.
- •15 Уравнение Шредингера для свободной частицы.
- •Частица в одномерной потенциальной яме.
- •20. Линейный гармонический квантовый осциллятор
- •21. Классическая модель атома водорода
- •22. Уравнение Шредингера для водорода. Квантовые числа
- •43.Деление ядер
- •44.Плазма
- •9.Соотношение неопределенностей Гейзенберга.
- •10.Опыт Дэвиссона и Джермера. Смысл волн де Бройля
- •4.Гипотеза Планка. Вывод формулы Планка.
- •5.Внешний фотоэффект.
- •6.Эффект Комптона.
- •34. Эффективная масса электрона
- •35. Полупроводники. Собственная и примесная проводимость.
- •36. Полупроводниковый диод.
- •37. Эффект Зеебека. Эффект Пельтье.
- •38. Конт разн потенц Контакт металл-металл.
- •39. Атомное ядро и его характеристики.
- •40. Ядерные силы и их свойства.
- •41. Радиоактивность. Альфа-распад. Бета-распад.
- •42.Закон радиоактивного распада.
- •26 Механический и магнитный моменты атома. Ls-связь.
- •27 Понятия об энергетических уровнях молекул.
- •28.Рентгеновские спектры. Закон Мозли.
- •29. Принцип тождества микрочастиц
- •30. Электронный газ в одномерном случае. Энергия Ферми.
- •31. Распределение Ферми-Дирака
- •32. Распределение Бозе-Эйнштейна
- •33. Энергетические зоны кристалла
- •45. Термоядерный синтез
- •46. Цепная реакция
- •Особенности теплового излучения, его характеристики.
- •2 Законы Кирхгофа, Стефана-Больцмана, Вина.
- •3. Тепловое излучение. Формула Релея-Джинса.
- •17 Решение уравнение Шредингера для низкого потенциального барьера.
- •18 Решение уравнение Шредингера для высокого потенциального барьера.
- •19)Туннельный эффект
- •13. Принцип причинности. Общее уравнение Шрёдингера.
- •14.Уравнение Шредингера для стационарных состояний
41. Радиоактивность. Альфа-распад. Бета-распад.
Радиактивность-процесс самопроизвольного превращения одних ядер в другие, который сопровождается испусканием частиц.
90% из известних ядер нестабильны
Радиоактивные ядра могут испускать частицы 3-х видов: α(полож),β(отриц),γ(нейтральные)
α -распад
α-частица
– ядро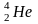
При распаде ядра должны сохраниться законы зарядового и массового числа
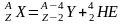
α-частицы при α-распаде вылетают с определенной энергией которая равна разности энергии материнского и дочернего ядер.
α-распад может сопровождаться γ-излучением в том случае, если материнское ядро находилось в возбужденном состоянииб аналогично если дочернее ядро находилось в возбуждненном состоянии.
Энергетическая диаграмма α-распада
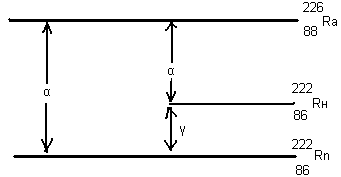
Материнское ядро для α-частицы является потенциальной ямой, вылет α-частицы возможен только при туннельном эффекте.
Β-распад
Электронный
:
 ,
,
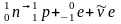
Позитронный : ,
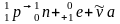
К-захват (ядро захватывает e с К-оболочки)
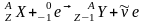 ,
,
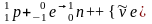
При исследовании Β-распада было обнаружено, что Β-частицы вылетают из ядра с произвольными значениями энергии, что противоречило закону сохранения энергии.
Разность энергии между материнским и дочерним ядрами при Β-распаде распределяется между электроном и частицей нейтрином (нейтральная частица с нулевой массой).
42.Закон радиоактивного распада.
Отдельные радиоактивные ядра испытывают распад независимо друг от друга, поэтому количество распавшихся ядер dN за время dt пропорционально числу имеющихся ядер N и времени
dN= - λN*dt, λ-постоянная распада
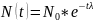
В результате разделения переменных получим
dN/N = - λ*dt
этот
же закон
может быть записан в виде
: N=

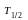 -
период полураспада – время за которое
распадается половина ядер
-
период полураспада – время за которое
распадается половина ядер
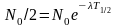
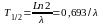
Количество распавшихся ядер определяется:
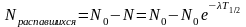
Активность распада A= λN
26 Механический и магнитный моменты атома. Ls-связь.
Различают два способа расчёта суммарного момента атома ls-связь и jj-связь
Под ls связью понимают случай когда орбитальные моменты всех электронов в атоме связаны между собой сильнее чем орбитальные и спиновой момент каждого элуктрона в отдельности
Аналогично спиновые моменты всех электронов связаны между собой прочнее, чем с орбитальным моментом каждого электроа
При jj-связи связь между орбитальным и спиновым моментом бля каждого электрона сильнее, чем связь с орбит (спинов) моментом друг электр. В ls-связи расчитыв с учётом правил. квантов. сначал полный орбит и спи моменты, а затем полн. мех. момент атома.
Для ls-связи необходимо рассчитать сумм орбит и сумм спинов момент атома запишем углов квантов орбит момента импульса
M2=ħ2L(L+1)
Квантовое число L для 2-ух электронов принимает значение от l1 до | l2-l1|
(L=l1+l2; l1+l2-1; | l2-l1|)
Добавим 3-ий электрон в этом случае число (L) меняется
(L=l1+l2+l3; l1+l2+l3-1; lmin)
lmin – минимальное значение по-парной суммы квантового числа для 2-ух электронов с третьим квантовым числом l3
Пример
(l1=1; l2=2; l3=2)
1) L12=2 -
2) L12=1 - добавляем l3=2
3) L12=0 -
Получаем
1) L123=4;3;2;1;0 -
2) L123=3;2;1 - для трёх электронов получаем
3) L12=2 - L=4;3;2;1;0
Для проекции орбитального момента атома
Mz=ml ħ ( Mz=m ħ)
(ml=-L; -L+1;…..0…L;)
Для суммарного спинового момента атома
Mz2= ħ2S(S+1)
Квантов число (для 2-ух электронов)
(S=S1+S2;…;|S1-S2|)
Для н-го колич электронов возможно 2 случ
-если в атоме чётное число электронов, то число S будет меньше(Nx1/a,0)
-при нечетном количестве электронов спиновое число будет полуцелым, то будет менье (Nx1/2…;1/2)
Полный мех момент атома J, определяется
Mj2= ħ2j(j+1)
(j=L+S…|L-S|)
Условие квантов
Mjz=
ħ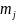
(Mj=-J; -J+1;.. 0.. J)
