
- •Ход работы.
- •Часть 1
- •Часть 2
- •Лабораторная работа №2.
- •Порядок выполнения лабораторной работы:
- •Ход работы:
- •Лабораторная работа №6.
- •Лабораторная работа №8
- •Лабораторная работа №10
- •Ход работы:
- •Лабораторная работа №11 Определение коэффициента внутреннего трения жидкости методом Стокса
- •Порядок выполнения лабораторной работы
Лабораторная работа №8
“ Определение скорости распространения звука в твердых телах и модуля Юнга”
Цель работы: Опрелить скорость распространения звука в твердых телах, добившись резонансной частоты в твердых телах, добившись резонансной частоты в твердом стержне и расчитать и сравнить с табличным значением модуля Юнга.
Ход работы:
Измерить длину стержня линейкой.
Закрепить стержень в зажиме, установить зазор между датчиком, приемником и концами стержня не более 0,5 мм.
Включить в сеть звуковой генератор и осциллограф.
Изменяя частоту звукового генератора от О в сторону увеличения, добиться резонанса колебаний стержня.
Все результаты измерений и расчетов нужно представить в виде таблицы.
Сравнить полученные результаты с табличными.
Таблица №1
№ п/п |
L, м |
Р, кг/м3 |
|
V, м/с |
Ерасч, Н/м3 |
Етабл Н/м3 |
1 |
0,544 |
7700 |
4687 |
4125 |
2,03·1011 |
2,16·1011 |
2 |
0,530 |
8400 |
3139 |
2574 |
9,3·1010 |
1,18·1011 |
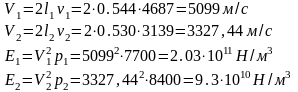
Вывод: Проведя два опыта с двумя различными стержнями мы видим, что: Ерасч≈ Етабл.
Лабораторная работа №10
“Определение отношения теплоемкости воздуха при постоянном давлении и постоянном объеме”.
Цель работы: Измерить отношение теплоемкости воздуха при постоянном давлении и теплоемкости воздуха при постоянном объеме.
Теоретическое введение:
Теплоемкость газа
численно равна количеству теплоты,
которое необходимо сообщить этому газу,
чтобы увеличить его температуру на
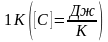 .
.
Для определения отношения теплоемкости при постоянном давлении Ср к теплоемкости при постоянном объеме Cv следует рассмотреть процесс, где это отношение играет существенную роль. Таким процессом является адиабатический процесс, описываемый уравнением Пуассона:
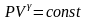 (1)
(1)
либо
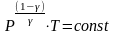 (2)
(2)
здесь Р- давление газа ([Р] = Па), V - объем газа ([v] = м3)
и
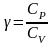 (3)
(3)
Для идеального газа
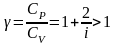 (4)
(4)
Здесь
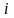 - количество степеней свободы молекулы
рассматриваемого газа, т.е. число
координат, достаточное для фиксации
положения молекулы в пространстве между
рассматриваемым газом и окружающей
средой. В реальных условиях осуществить
полную теплоизоляцию невозможно. Однако
на практике пользуются тем фактом, что
установление равновесного давления
протекает очень быстро - за доли секунды,
а на выравнивание температуры требуются
минуты. Следовательно, осуществления
процесса близкого к адиабатическому
быстро изменяют давление в газе.
- количество степеней свободы молекулы
рассматриваемого газа, т.е. число
координат, достаточное для фиксации
положения молекулы в пространстве между
рассматриваемым газом и окружающей
средой. В реальных условиях осуществить
полную теплоизоляцию невозможно. Однако
на практике пользуются тем фактом, что
установление равновесного давления
протекает очень быстро - за доли секунды,
а на выравнивание температуры требуются
минуты. Следовательно, осуществления
процесса близкого к адиабатическому
быстро изменяют давление в газе.
При адиабатическом процессе первое начало термодинамики (закон сохранения энергии) имеет следующий вид:
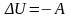 (5)
(5)
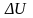 - изменение
внутренней энергии газа (U –суммарная,
механическая энергия всех молекул газа
([U] = Дж), А - работа при адиабатическом
расширении либо сжатии ([А] = Дж).
- изменение
внутренней энергии газа (U –суммарная,
механическая энергия всех молекул газа
([U] = Дж), А - работа при адиабатическом
расширении либо сжатии ([А] = Дж).
Если газ расширяется, то А > 0, следовательно, соглао уравнению (5) внутренняя энергия уменьшается температура газа Т понижается. При сжатии газа А - имеет место обратный эффект.
Если газ расширяется изобарически (при постоями давлении), то согласно первому началу термодинамики
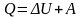 (6)
(6)
Количество теплоты Q, полученное газом, расходуется на изменение внутренней энергии и совершение работы А ([Q] = Дж).
Если же процесс изохорический (при постоянном объеме), то работа А = 0 и по первому закону гермодинамики:
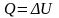 (7)
(7)
Тепло расходуется лишь на изменение внутренней энергии. Если в обоих случаях температура изменилась больше на величину совершенной работы А.
Если мы имеем один моль газа, то работа:
A=R (8)
Где R – универсальная
газовая постоянная
 .
.
Полученный нами вывод, что Ср >Cv согласуется с соотношением (4) (9)
Так как в дальнейшем нам понадобиться уравнение изобарического и изохорического процессов, напишем уравнение Менделеева - Клапейрона – уравнение состояния идеального газа:
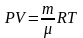 (10)
(10)
m -масса газа,
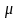 - масса моля газа.
- масса моля газа.

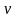 ,
Гц
,
Гц