
- •19. Перенос в-в через биологические мембраны
- •20. Биологическое окисление: типы, функции. Ферменты биологического окисления в митохондриях: пиридин-, флавин-зависимые дегидрогеназы, цитохромы.
- •21. Молекулярные комплексы внутренних мембран митохондрий. Пункты сопряжения транспорта электронов и фосфорилирования. Хемиосмотическая теория окислительного фоффорилирования. Атф-синтаза митохондрий.
- •22. Микросомальное окисление: цитохром р-450, молекулярная организация пути переноса электронов.
- •23. Цтк. Локализация, последовательность ферментативных реакций, регуляция, значение в обмене в-в. Энергетический баланс цтк.
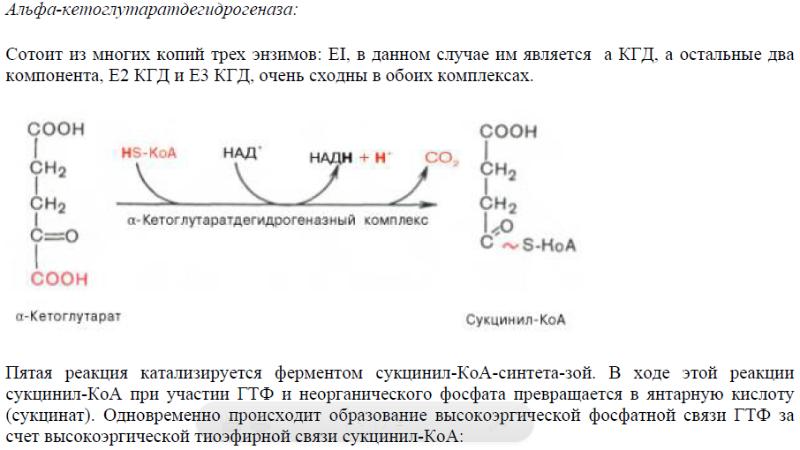
- •24.Особенности функционирования пируват-дегидрогеназного и α-кетоглуторат-дегидрогеназного мультиферментных комплексов. Регуляция
- •25. Пентозофосфатный путь окисления глюкозо- 6-фосфата и его биологическая роль.
- •26. Аэробный и анаэробный распад глюкозы. Общая характеристика процессов, регуляция
- •27. Гликолиз и брожение. Последовательность реакций и ферменты
24.Особенности функционирования пируват-дегидрогеназного и α-кетоглуторат-дегидрогеназного мультиферментных комплексов. Регуляция
Особую группу ферментов составляют надмолекулярные ферментные комплексы, в состав которых входят разные ферменты, катализирующие последовательные ступени превращения какого-либо субстрата. Отличительными особенностями подобных муль-тиферментных комплексов являются прочность ассоциации ферментов и определенная последовательность прохождения промежуточных стадий во времени, обусловленная порядком расположения каталитически активных белков в пространстве . Типичными примерами подобных мультиферментных комплексов являются пируватдегидрогеназа и α-кетоглутаратдегидрогеназа, катализирующие соответственно окислительное декарбоксилирование пиро-виноградной и α-кетоглутаровой кислот в животных тканях. Ряд таких мультиферментных комплексов структурно связан с какой-либо органеллой или с биомембраной и составляет высокоорганизованные надмолекулярные системы, обеспечивающие жизненно важные функции, например перенос электронов от субстратов к кислороду через систему дыхательных ферментов.
Регуляция пируватдегидрогеназного комплекса
Регулируемым ферментом ПВК-дегидрогеназного комплекса является первый фермент – пируватдегидрогеназа (Е1). Два вспомогательных фермента – киназа и фосфатаза обеспечивают регуляцию активности пируватдегидрогеназы путем ее фосфорилирования и дефосфорилирования.
Вспомогательный фермент киназа активируется при избытке конечного продукта биологического окисления АТФ и продуктов ПВК-дегидрогеназного комплекса – НАДН и ацетил-S-КоА. Активная киназа фосфорилирует пируватдегидрогеназу, инактивируя ее, в результате первая реакция процесса останавливается.
Фермент фосфатаза, активируясь ионами кальция или инсулином, отщепляет фосфат и активирует пируватдегидрогеназу.
Регуляция активности пируватдегидрогеназы
Таким образом, работа пируватдегидрогеназы подавляется при избытке в митохондрии (в клетке) АТФ и НАДН, что позволяет снизить окисление пирувата и, следовательно, глюкозы в случае когда энергии достаточно.
Если АТФ мало или имеется влияние инсулина, то образуется ацетил-SКоА. Последний в зависимости от условий будет направляться либо в цикл трикарбоновых кислот с образованием энергии АТФ, либо на синтез холестерина и жирных кислот.
25. Пентозофосфатный путь окисления глюкозо- 6-фосфата и его биологическая роль.
Пентозофосфатный путь служит альтернативным путём окисления глюкозо-6-фосфата. состоит из 2 фаз (частей) - окислительной и неокислительной.
В окислительной фазе глюкозо-6-фосфат необратимо окисляется в пентозу - рибулозо-5-фосфат, и образуется восстановленный NADPH.
В неокислительной фазе рибулозо-5-фосфат обратимо превращается в рибозо-5-фосфат и метаболиты гликолиза.
Пентозофосфатный путь обеспечивает клетки рибозой для синтеза пуриновых и пиримидиновых нуклеотидов и гидрированным ко-ферментом NADPH, который используется в восстановительных процессах.
Суммарное уравнение пентозофосфатного пути выражается следующим образом:
3 Глюкозо-6-фосфат + 6 NADP+ → 3 СО2 + 6 (NADPH + Н+) + 2 Фруктозо-6-фосфат + Глицеральдегид- 3 -фосфат.
Ферменты пентозофосфатного пути локализованы в цитозоле.
Наиболее активно протекает в жировой ткани, печени, коре надпочечников, эритроцитах, молочной железе в период лактации, семенниках.
А. Окислительный этап
глюкозо-6-фосфат подвергается окислительному декарбоксилированию, в результате которого образуются пентозы.
Первая реакция дегидрирования - превращение глюкозо-6-фосфата в глюконолактон-6-фосфат - катализируется МАDР+-зависимой глюкозо-6-фосфатдегидрогеназой и сопровождается окислением альдегидной группы у первого атома углерода и образованием одной молекулы восстановленного кофермента NADPH.
Далее глюконолактон-6-фосфат быстро превращается в 6-фосфоглюконат при участии фермента глюконолактонгидратазы.
Фермент 6-фосфоглюконатдегидрогеназа катализирует вторую реакцию дегидрирования окислительной части, в ходе которой происходит также и декарбоксилирование. При этом углеродная цепь укорачивается на один атом углерода, образуется рибулозо-5-фосфат и вторая молекула гидрированного NADPH.
Восстановленный NADPH ингибирует первый фермент окислительного этапа пентозофосфатного пути - глюкозо-6-фосфатдегидрогеназу. Превращение NADPH в окисленное состояние NADP+ приводит к ослаблению ингибирования фермента. При этом скорость соответствующей реакции возрастает, и образуется большее количество NADPH.
Суммарное уравнение окислительного этапа пентозофосфатного пути можно представить в виде:
Глюкозо-6-фосфат + 2 NADP+ + Н2О → Рибулозо-5-фосфат + 2 NADPH + Н+ + СО2.
Реакции окислительного этапа служат основным источником NADPH в клетках. Гидрированные коферменты снабжают водородом биосинтетические процессы, окислительно-восстановительные реакции, включающие защиту клеток от активных форм кислорода. NADPH как донор водорода участвует в анаболических процессах, например в синтезе холестерина.

Рис. 7-62. Окислительный этап пентозофосфатного пути.
