
- •21.Структуры кристаллов с формулами типа ax2, построенные на основе плотнейшей упаковки и без нее. Примеры
- •22.Полиэдрический метод изображения кристаллических структур, построенных на основе плотнейших упаковок и без них.
- •23. Двух и трех буквенный способ обозначения при описании плотнейших упаковок.
- •24. Определение симметрии многослойных плотнейших упаковок.
- •25. Структуры SiC и СdI 2 . Явление политипии.
- •26. NaCl-подобные структуры. Примеры.
- •27. Структуры полиморфных модификаций углерода.
- •28. Октаэдрические мотивы в кристаллических структурах оливина, корунда, кальцита, шпинели, рутила.
- •29. Классификация кристаллических структур на основе локализованных в них химических связей. Типы химических связей.
- •30. Классификация кристаллических структур на геометрической основе Геометрический характер структур.
- •35. Кремнекислородные радикалы силикатов с конечными мотивами. Примеры структур.
27. Структуры полиморфных модификаций углерода.
Есть несколько модификаций углерода: Лонсдейлит, алмаз, альфа-графит, бетта-графит
Кристаллическая структура лонсдейлита С
Взяв за основу структуру вюрцита ZnS (рис. 6.77а) и «перекрасив» ее в один цвет, т. е. поместив в позиции Zn и S атомы С (рис. 6.776, в), получим структуру одной из модификаций углерода — лонсдейлита. В этой структуре, несмотря на то что симметрия позиций атомов углерода наследуется от атомов Zn и S структуры вюрцита — Зm, появляются горизонтальные плоскости mz , связывающие теперь уже одинаковые атомы, расположенные друг над другом на осях 3-го порядка . Таким образом, как бы возвращается голоэдрическая пространственная группа «пустой» двухслойной плотнейшей упаковки P63/mmc. рода (занимающими позиции Zn и S структуры вюрцита). Плотнейшая упаковка, естественно, исчезает, так как в позициях, центрирующих тетраэдрические пустоты, оказываются атомы (шары) такого же размера, как и те, центры тяжести которых располагаются по закону гексагональной плотнейшей упаковки. В результате образуются углеродные слои со встречной гофрировкой, что отличает слои структуры этого минерала от графитовых слоев в альфа- и бетта- (3-модификациях углерода, где они плоские)
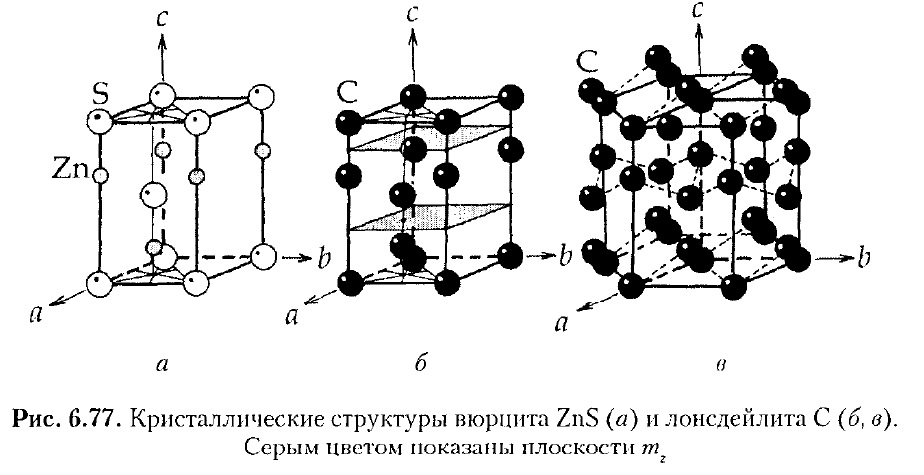
Кристаллическая структура алмаза С
Действительно, в структуре алмаза одна половина атомов С расположена в позиции атомов S, создающих в сфалерите кубическую плотнейшую упаковку, другая же половина атомов С, располагаясь в центрах тяжести тетраэдрических пустот в позициях Zn, как бы раздвигает соседние атомы, ликвидируя этим плотнейшую упаковку. И хотя позиции и их симметрия при такой замене остаются теми же, что и в структуре сфалерита, — -43m, правильные системы точек, занятые атомами Zn и S структуры сфалерита, объединяются за счет появления в структуре алмаза координатных клиноплоскостей d. В результате симметрия всей кристаллической постройки алмаза повышается от гемиэдрической, описываемой пространственной группой сфалерита F-43m без координатных осей симметрии, до голоэдрической F-43m:
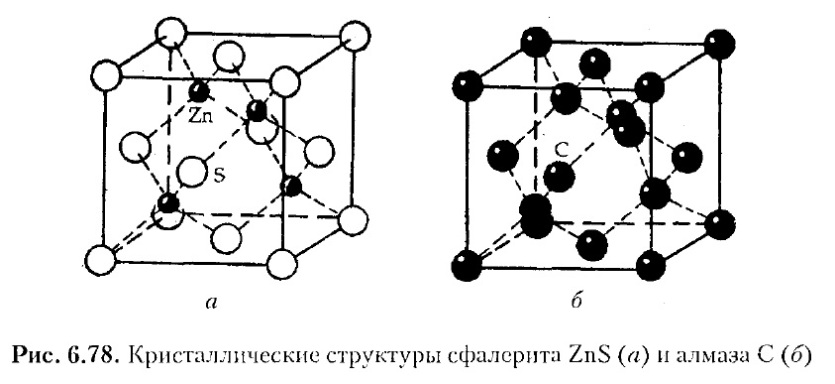
Кристаллическая структура альфа-графита С
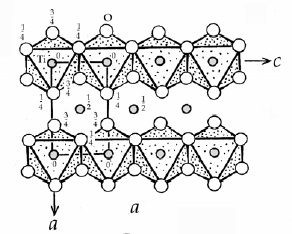
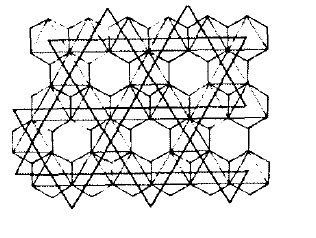
28. Октаэдрические мотивы в кристаллических структурах оливина, корунда, кальцита, шпинели, рутила.
Оливин корунд кальцит
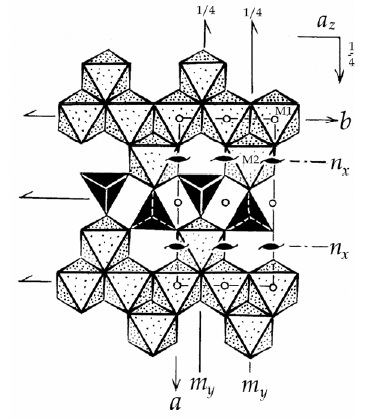
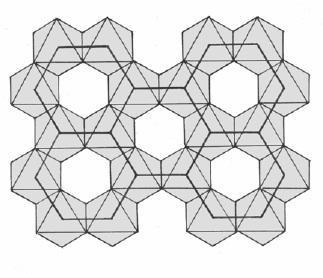

Рутил шпинель
29. Классификация кристаллических структур на основе локализованных в них химических связей. Типы химических связей.
Если попытаться провести классификацию соединений па основе реализованных в них химических связей между структурными единицами, то увидим, что сделать это будет достаточно сложно, поскольку рассмотренные выше предельные типы химической связи в чистом виде проявляются чрезвычайно редко. Чаще всего в одном и том же кристалле одновременно реализуются различные типы связей, из которых одни нередко преобладают над остальными. В этом случае соответственно преобладанию того или иного типа связи между атомами образуются ионные или ковалентные кристаллы. Возможно образование кристаллов из молекул. В этом случае каждая молекула образуется за счет ковалентных связей между атомами, ее составляющими, отдельные же молекулы связаны между собой ваи-дер-ваальсовыми связями. Кроме того, при анализе структуры любого химического соединения принято учитывать традиционную классификацию межатомных взаимодействий, различая сильные связи — ковалентиые, ионные, металлические и слабые — водородные и межмолскулярные (ван-дер-ваальсовы). Все это затрудняет классификацию кристаллов но типам реализованных в них химических связей. Тем не менее полезную информацию о кристаллической структуре можно получить, выявив ее геометрический характер, так как именно на нем в значительной степени отражается тип химической связи. Если в кристалле связь между всеми атомами одинакова, то такие структуры называют гомодесмическшш (от греч. гомо (6цою() — одинаковый, десмос (беаро() — связь). При этом отнюдь не обязательно этот единственный тип связи проявляется в чистом виде. Так, в ряду одинаковых по структуре кристаллов SiC, AlP, ZnS, Agl, возглавляемом существенно ковалентным карбидом кремния SiC, наблюдается постепенное и значительное нарастание полярности (ионности) связи. В тех случаях, когда в структуре кристалла реализуются несколько типов химической связи, структуры называют гетеродесмическими (от греч. гетеро (етеро() — разные). Причем один тип связи проявляется внутри какой-либо группировки атомов, другой — между атомами из соседних группировок или между отдельными атомами и атомами группировок.
