
- •Исследование каталитических свойств протеолитических ферментов
- •Исследование зависимости скорости ферментативной реакции от времени
- •Исследование зависимости активности фермента от
- •Исследование влиянии ингибитора металлопротеииаз на активность ферментного препарата
- •Техника безопасности
- •Лабораторная работа № 2 солевое фракционирование белков
- •Ход работы
- •Получение клеточного экстракта дрожжей
- •Фракционирование клеточного экстракта
- •Обработ ка экспериментальных данных
- •Техника безопасности
- •Разделение белков методом ионообменной хроматографии
- •Подготовка сорбента
- •Заполнение колонки и внесение образца
- •Элюция белков с колонки
- •Регенерация колонки
- •Обработка экспериментальных данных
- •Техника безопасности
- •Определение молекулярной массы белка методом гель-хроматографии
- •I лкие компоненты не проникаюл в фанулы гелевой фазы и выхолят из колонки первыми. Более мелкие молекулы, способные проникать внутрь
- •Заиолнс'ние колонки
- •Определение объемов элюции калибровочных белков
- •Определение объема элюции исследуемого белка
- •Техника безопасности
Регенерация колонки
После окончания работы КМ-целлюлозу извлекают из колонки в нмический стакан и заливают 100 мл дистиллированной воды. После обработки в соответствии с описанием п.1 она может быть использована для ныделения белковых смесей.
Обработка экспериментальных данных
На основании полученных результатов строят профиль элгоции. Для пот вычерчивают график, на горизонтальной оси которого откладывают пш.ем прошедшей через колонку жидкости (или номера фракций), а на iu-ртикальной оси - величины оптической плотности фракций.
Делают заключение о составе анализируемого белкового препарата.
Техника безопасности
При работе на установке соблюдать правила работы со стеклом. Перед включением перистальтического насоса и магнитной мешалки проверим, исправность розетки шнура, вилки, а также наличие заземления. При ш.пюлнении измерения оптической активности руководствоваться инструкцией по работе со спектрофотокалориметром (документация на рабочее место № 3).
ЛАБОРАТОРНАЯ РАБОТА № 4
Определение молекулярной массы белка методом гель-хроматографии
Гель-хроматография (гель-фильтрация) - фракционирование смеси компонентов но размерам молекул путем прохождения их через гели с оп- pi- пленной величиной пор.
Раствор, содержащий смесь двух и более веществ, отличающихся по размеру молекул, а следовательно, и по молекулярной массе, вносят в колонку, заполненную гелем с сетчатой структурой и уравновешенную буферным раствором. Наибольшей скоростью продвижения по колонке об- I а лают компоненты раствора, размеры молекул которых больше пор геля.
I лкие компоненты не проникаюл в фанулы гелевой фазы и выхолят из колонки первыми. Более мелкие молекулы, способные проникать внутрь
е.ля. непрерывно обмениваются между жидкими фазами внутри и вне геля и продвигаются по колонке значительно медленнее. Находящиеся в рас- шоре самые маленькие частицы (например, неорганические соли) выходят и I колонки последними.
Смесь
белков и неорганических солей
Неорганические
соли
Мелкие
белки
Средние
белки
Крупные
белки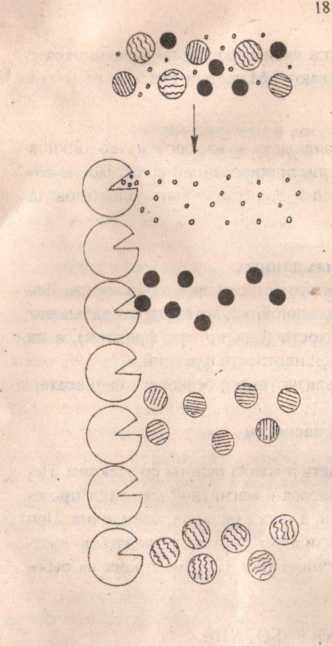
Рис. 6. Распределение молекул различных размеров по длине
колонки в процессе гель-фильтрации
Наиболее широкое распространение среди носителей для гель- хроматографии белков получили сорбенты, приготовленные на основе декстрана (оефадексы. сефакрилы, молселекты), полиакриламида (биогели Р, ак-рилексы) и агарозы (сефарозы, биогели А). Набухая в воде эти вещества образуют гели.
Простейшее устройство для проведения гель-фильтрации изображено на рис.7.
Важнейшей частью данного устройства является хроматографическая колонка. В упрошенном варианте она представляет собой полую стеклянную трубку, в основание которой впаивают пористую стеклянную пластинку или перфорированный диск. Диск служит подложкой для гелевого слоя и предотвращает унос частиц геля из колонки.
Колонка с помощью капиллярных шлангов присоединяется к сосуду с жидкостью. которую собираются прокачать через колонку (элюент). а мкже к коллектору фракций, который позволяет собирать вытекающую из колонки жидкость (элюат) небольшими порциями. Внутренний размер шланга, соединенного с коллектором, а также “мертвое" пространство под пи ком должны быть минимальны. В противном случае происходит сме- шинание разделенных на колонке веществ. Коммерческие колонки снаб- | eilbi специальными приспособлениями - концевыми адаптерами, которые > ноляI к минимуму перемешивание элюируемых фракций.
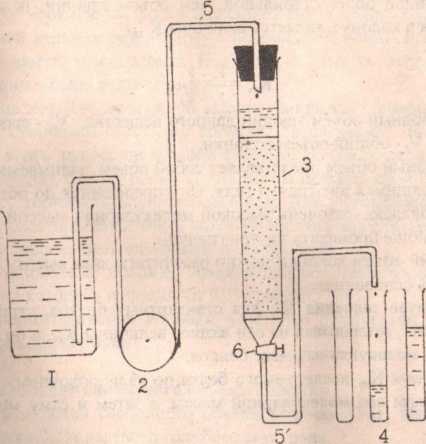
1’ИС.7 . Схема хромагофафической установки •. .
-сосуд с элюентом; 2 - перистальтический насос; 3 - хроматофа-
фическая колонка: 4 - коллектор фракций; 5 - капиллярные шланги;
6 - кран-зажим
Метод гель-фильтрации может быть использован для разделения не IKOB и других полимеров, их обессоливания. замены одних буферных расгворов другими, а также для определения молекулярной массы полимерных молекул.
Целыо данной работы является определение молекулярной массы Г>с 1ков на колонке с сефадексом.
В основе метода определения молекулярной массы с помощью пчь-фильтрации лежит линейная зависимость между логарифмом моле- kv гярной массы глобулярного белка и объемом его элюирования с колонки. мполненной гелем. Поэтому для оценки молекулярной массы глобулярного белка достаточно определить объем его элюции с предварительно откалиброванной колонки.
Калибровку колонки проводят, пропуская через нее белки с известной молекулярной массой и регистрируя объемы элюции каждого их них. Объем элюции - это объем элюата, собранного с момента внесения образца на колонку до момента его элюции, включая фракцию с максимальным его содержанием.
Величиной более стабильной, чем объем элюции, не зависящей от уро вня геля в колонке, является величина К
где Ve - свободный объем элюции данного вещества; V0 - свободный объем колонки; Vt- общий-объем колонки.
Свободный объем представляет собой объем, занимаемый растворителем, находящимся вне гранул геля. Он определяется по объему элюции вещества, обладающей очень высокой молекулярной массой, которое не способно вообще проникать внутрь гранул.
Рабочий объем колонки можно рассчитать, зная высоту столбика геля и площадь основания.
Подсчитав значения Кау для стандартных белков, строят калибровочный график, откладывая на оси абсцисс величины Ка», а по оси ординат
логарифмы молекулярных масс белков.
Используя Kav исследуемого белка,по калибровочному графику находят логарифм его молекулярной массы, а затем и саму молекулярную массу.
ХОД РАБОТЫ 1. Подготовка сорбента
Сефадексы - продукты взаимодействия полисахарида декстрана с эпихлоргидрином. При определении молекулярной массы белков пользуются сефадексами марки G-100.
При работе сефадексам дают предварительно набухнуть в избытке растворителя. Для этого 1 г сухого сефадекса суспензируют в 200-кратном объеме дистиллированной воды и оставляют при комнатной температуре на 48 часов до полного набухания.
Густую суспензию набухшего геля используют для заполнения колонки.
