
- •Билет № 1
- •Материальная точка
- •Система отсчёта
- •Билет № 2
- •1. 1)Прямолинейное равномерное движение
- •Графики прямолинейного равномерного движения.
- •2) Средняя и мгновенная скорости
- •3) Уравнение движения
- •4)Графическое представление неравномерного прямолинейного движения
- •Можно выделить три вида сил трения:
- •Трение скольжения
- •Трение качения
- •Билет № 3
- •1. Относительность движения
- •2. Механическая работа
- •Билет № 4
- •1. Ускорение
- •2) Нормальная и тангенциальная составляющие ускорения
- •3) Классификация движений в зависимости от величины и направления ускорения
- •Энергия связи ядер
- •Билет № 5
- •1. Свободное падение тел
- •2. Строение атома
- •Билет № 6
- •Линейная скорость при вращении:
- •2. Энергия
- •Билет № 7
- •Билет № 8
- •1. Законы Кеплера
- •Билет № 9
- •3) Условия равновесия твердого тела
- •Чтобы не вращающееся тело находилось в равновесии, необходимо, чтобы равнодействующая всех сил, приложенных к телу, была равна нулю.
- •Билет № 10
- •2) Давление в движущихся жидкостях и газах
2. Строение атома
Модель строения атома Научные исследования, проводившиеся в конце XIX - начале XX вв. позволили предложить следующую модель строения атома: 1. В центре атома находится положительно заряженное ядро, занимающее ничтожную часть пространства внутри атома. 2. Весь положительный заряд и почти вся масса атома сосредоточены в его ядре. 3. Ядра атомов состоят из протонов и нейтронов ( нуклонов). Число протонов в ядре равно порядковому номеру элемента, а сумма чисел протонов и нейтронов соответствует его массовому числу. 4. Вокруг ядра по замкнутым орбитам вращаются электроны. Их число равно положительному заряду ядра.
Ядро - это центральная позитивно заряженная часть атома, в которой сосредоточена его масса. Электрон - частица с негативным зарядом, который условно принят за -1. Нейтрон - нейтральная частица, не имеющая электрического заряда. Масса нейтрона равна 1 а. е. м. Протон - положительно заряженная частица, с такой же массой, как и нейтрон. Заряд протона равен заряду электрона и противоположен по знаку. Число протонов в ядре атома равно числу электронов. Это число определяет заряд ядра атома элемента и его порядковый номер элемента в таблице Менделеева. При известных условиях нейтрон может превращаться в протон и наоборот. Атомные массы элементов в периодической таблице являются средним значением из массовых чисел природных смесей из изотопов. Поэтому они не могут, как считал Менделеев, служить главной характеристикой атома и элемента. Такой характеристикой является заряд ядра атома. Он определяет число электронов в нейтральном атоме, которые распределяются вокруг ядра по определенным орбитам и определяют химические свойства атомов. В результате этого было дано новое определение химического элемента и уточнена формулировка периодического закона: Химический элемент - это совокупность атомов с одинаковым зарядом ядра. Свойства элементов, а также свойства и формы их соединений находятся в периодической зависимости от заряда ядра атома элемента. Открытое Беккерелем явление радиоактивности было первым примером ядерных реакций - превращений ядер одного элемента в ядра другого элемента. Сейчас известно очень много ядерных реакций; все они относятся к физическим явлениям и поэтому в обычном курсе химии не рассматриваются.
Опыты Резерфорда
Изображение атомов солнечной батареи, полученное с помощью туннельного микроскопа.
В 1913 г. английский физик Резерфорд проделал классические опыты по рассеянию a-частиц тонкими слоями различных веществ. a-частицы, испускаемые радиоактивными веществами, являются подходящими пробными зарядами для исследования внутриатомных электрических полей. Они представляют собой полностью ионизированные атомы гелия, имеют положительный заряд, равный удвоенному элементарному заряду (q = 3.2·10-19 Кл), массу m = 6.67·10-27кг, обладают высокой энергией (а значит и скоростью), достаточной для проникновения в атомы вещества.
Схема опытов Резерфорда и его учеников Гейгера и Марсдена изображена на рис.1.Внутри герметичной камеры, в которой был создан высокий вакуум, находился свинцовый контейнер с радиоактивным элементом, испускавшим a-частицы. Узкий пучок частиц падал перпендикулярно на поверхность металлической (золотой) фольги, толщиной около 1 мкм (10-6м). Регистрация частиц производилась по вспышкам света (сцинтилляциям), вызываемыми ими на экране, покрытом люминофором. Экран был укреплен перед объективом на корпусе микроскопа, с помощью которого визуально наблюдали сцинтилляции и подсчитывали их число. Так определяли количество частиц, движущихся по данному направлению после их взаимодействия с атомами вещества. Микроскоп вместе с экраном мог вращаться вокруг вертикальной оси, походящей через центр камеры, для регистрации рассеянных атомами фольги частиц.
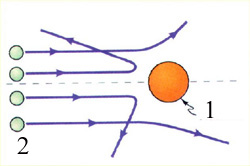
На рисунке: 1- атом золота, 2- a-частицы
Результаты опытов Резерфорда:
1.большинство частиц проходит через атомы вещества. не рассеиваясь (как через "пустоту");
2.с увеличением угла рассеяния число отклонившихся от первоначального направления частиц резко уменьшается;
3.имеются отдельные частицы, отбрасываемые атомами назад, против их первоначального движения (как мяч от стенки).
Резерфорд вывел формулу, по которой можно рассчитать количество a-частиц, рассеянных под определенными углами. В эту формулу входит характеристический параметр "d ", являющийся поперечным размером образований, отклоняющих частицы.
Для совпадения расчетов с результатами опытов это параметр должен быть порядка 10-13 см. Атомы имеют диаметр 10-8 см, т.е. на пять порядков выше. Следовательно, в атоме имеется область занимающая ничтожно малую часть атома, которая и отклоняет частицы на большие углы вплоть до 1800.
