
- •1. Реакции катионов первой аналитической группы
- •2. Реакции катионов второй аналитической группы
- •3. Реакции катионов третьей аналитической группы
- •4. Анализ смеси катионов II - III групп
- •4. Реакции катионов четвёртой аналитической группы
- •5. Реакции катионов пятой аналитической группы
- •6. Реакции катионов шестой аналитической группы
6. Реакции катионов шестой аналитической группы
6.1. Д е й с т в и е г р у п п о в о г о р е а г е н т а
Групповым реагентом на катионы шестой группы является гидроксид аммония в избытке. Возьмите 5 пробирок, внесите в каждую из них по 3 капли раствора солей меди (II), ртути (II), кадмия, никеля и кобальта, добавьте сначала по 3 капли 25%-ного раствора аммиака, перемешайте стеклянной палочкой. Обратите внимание на цвет осадков, затем добавьте в каждую пробирку по 6 капель концентрированного раствора аммиака, снова перемешайте стеклянной палочкой, кроме того, добавьте в растворы , содержащие катионы Hg2+ и Co2+, несколько кристаллов хлорида аммония NH4Cl. Сравните цвет осадков с окраской растворов комплексных солей. Напишите уравнения реакций.
6.2. Р е а к ц и и к а т и о н а Cu2+
1) Металлические алюминий, железо и цинк восстанавливают катион Cu2+ до свободного металла, имеющего вид красной губчатой массы. Напишите уравнения реакций. Для проведения эксперимента на обезжиренную и зачищенную металлическую пластину (алюминиевую, железную или цинковую) нанесите каплю раствора меди, подкисленного серной кислотой. Через некоторое время появляется красноватое пятно меди. Нужно иметь в виду, что в присутствии азотной кислоты выделение меди не происходит.
2) Йодид калия окисляется солями меди (II) с выделением свободного йода. Одновременно выпадает малорастворимый осадок йодида меди (I): 2Cu2+ + 4I- 2CuI + I2

6.3. Р е а к ц и и к а т и о н а Cd2+
Сероводород (или сероводородная вода), в не слишком сильно кислых, а также в нейтральных и в щелочных растворах (при рН0,5) образует жёлтый осадок CdS, нерастворимый в щелочах. Открытию катиона Cd2+ мешают другие катионы шестой группы.
Cd2+ + S2- CdS

6.4. Р е а к ц и и к а т и о н а Со2+
Роданид аммония NH4SCN или калия KSCN образует с катионом Со2+ комплексную соль синего цвета:
![]()
Для проведения реакции к 3-4 каплям раствора соли Со2+ прибавьте 10-12 капель насыщенного раствора и несколько кристаллов твёрдой соли роданида аммония, а также 6-8 капель амилового (или изоамилового) спирта. В его присутствии чувствительность реакции повышается, т.к. образующееся комплексное соединение более растворимо в амиловом спирте, чем в воде. Образовавшиеся Co(SCN)42--ионы окрашивают кольцо растворителя в интенсивно синий цвет. Проведению реакции мешает присутствие катионов Cu2+, Fe3+.
6.5. Р е а к ц и и к а т и о н а Ni2+
Диметилглиоксим (реактив Чугаева) в аммиачной среде даёт с катионом Ni2+ осадок внутрикомплексной соли:
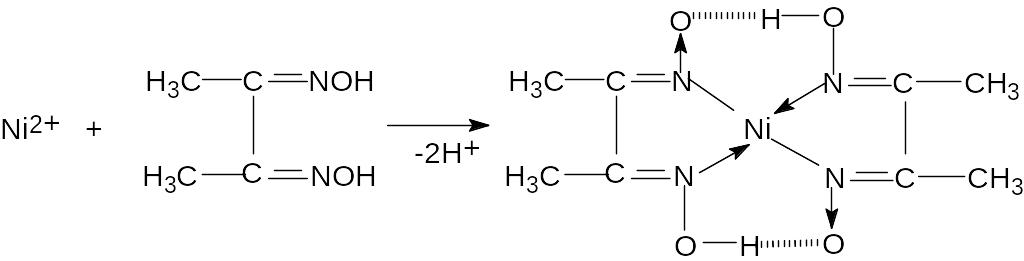

Проведению этой реакции мешают ионы Fe3+, образующие с диметилглиоксимом растворимые комплексы красного цвета. На фильтровальную бумагу нанесите одну каплю раствора Na2HPO4. Образующийся осадок FePO4 (если раствор загрязнён ионами Fe3+) остаётся в центре пятна, а растворимый Ni3(РО4)2 - на периферии. Обведите вокруг пятна капилляром с диметилглиоксимом. После этого бумагу обработайте аммиаком (подержите над склянкой с концентрированным аммиаком). На бумаге появляется розовое кольцо или пятно, указывающее на присутствие ионов никеля.
