
- •Физическая термодинамика Лекция 10 Физика макросистем
- •Термодинамические состояния и термодинамические процессы
- •Работа, совершаемая макросистемой
- •Первое начало термодинамики
- •Адиабатически изолированная термодинамическая система
- •Лекция 11
- •Уравнение состояния идеального газа
- •Основное уравнение молекулярно-кинетической теории
- •Экспериментальное подтверждение молекулярно-кинетической теории
- •Лекция 12 Теплоёмкость идеального газа
- •Адиабатический процесс
- •Политропический процесс
- •Работа газа при политропических процессах
- •Внутренняя энергия газа Ван-дер-Ваальса
- •Лекция 13 Тепловые и холодильные машины
- •Второе начало термодинамики
- •Термодинамический цикл Карно
- •Неравенство Клаузиуса
- •Термодинамическая энтропия
- •Свойства энтропии
- •Основное уравнение термодинамики
- •Вычисление энтропии
- •4. В изотермическом процессе
- •Термодинамическая диаграмма
- •Лекция 14 Статистическое описание равновесных состояний
- •Барометрическая формула
- •Равновесные флуктуации
- •Статистическое обоснование второго начала термодинамики
- •Энтропия и вероятность
- •Лекция 15 Явления переноса Термодинамические потоки
- •Описание явлений переноса в газах
- •Эффузия в разреженном газе
- •Физический вакуум
- •Броуновское движение
- •Лекция 16 Агрегатные состояния вещества
- •Условия равновесия фаз
- •Явления на границе раздела газа, жидкости и твёрдого тела
- •Диаграммы состояния
Работа, совершаемая макросистемой
Если объём газа получает приращение dV , а давление газа равно р , то элементарная работа сил, действующих со стороны газа на стенки,
δА = р.dV .
Это равенство легко получить, когда газ находится в цилиндре с поршнем (оно справедливо и в других случаях, например, при работе газовой турбины).
Э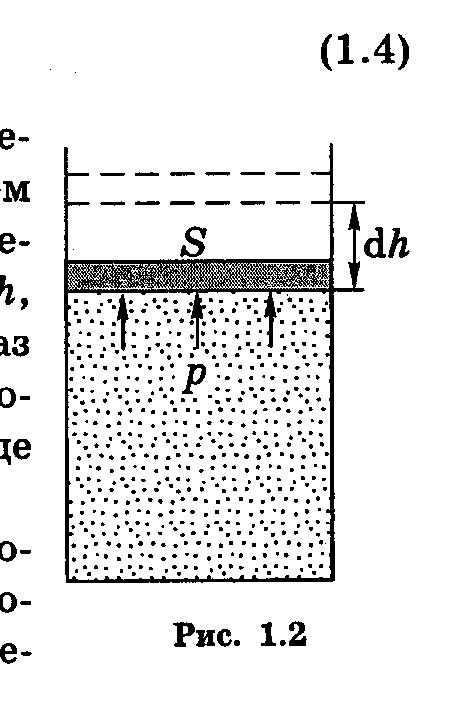 лементарная
работа, совершаемая газом при перемещении
поршня на dh
, равна δА
= F.dh
, где F
= р.S
– cила,
с которой газ действует на поршень.
площадь которого – S
. Поэтому
δА
= р
dh S
= p.(dh
S)
= p.dV.
лементарная
работа, совершаемая газом при перемещении
поршня на dh
, равна δА
= F.dh
, где F
= р.S
– cила,
с которой газ действует на поршень.
площадь которого – S
. Поэтому
δА
= р
dh S
= p.(dh
S)
= p.dV.
В изобарном процессе
A = p (V2 – V1).
Если давление в процессе 1 – 2 меняется то работа, совершаемая газом при конечных изменениях объёма от до V2 , представляют в виде интеграла:
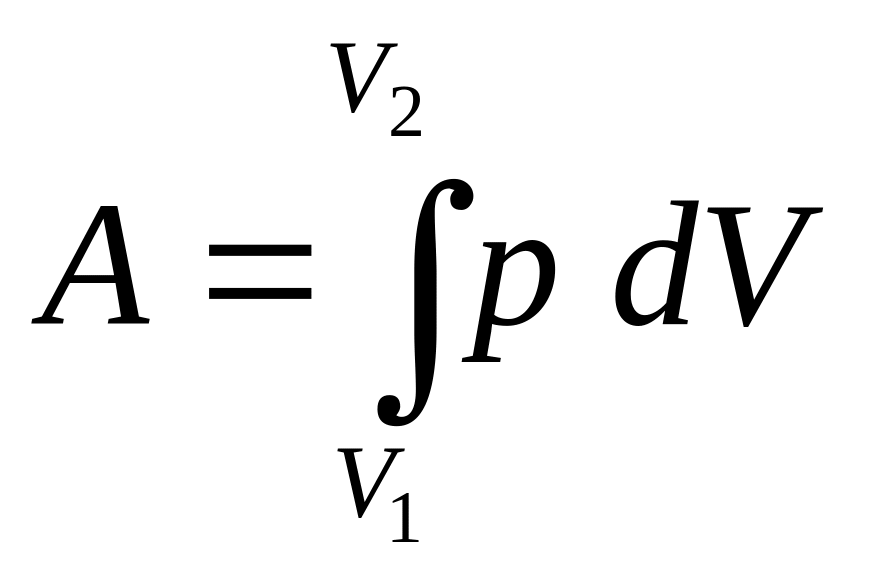 .
.
Г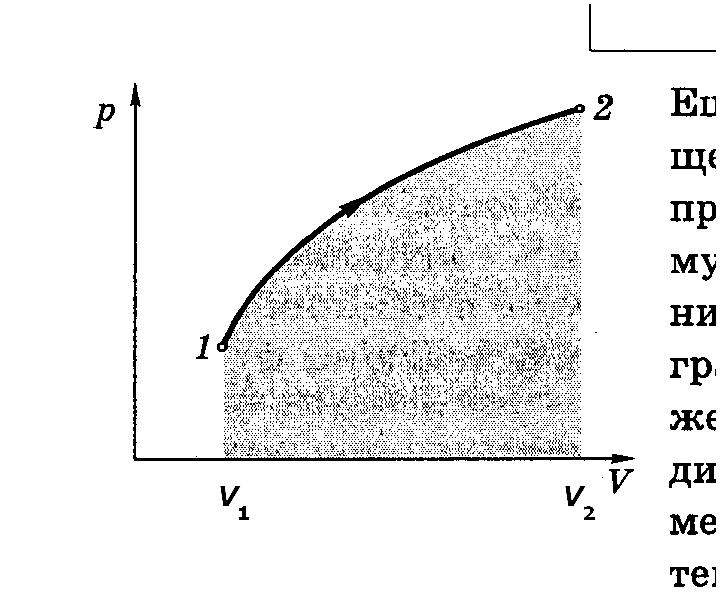 еометрическая
интерпретация интеграла – «площадь»
под кривой 1 – 2, а эта площадь зависит
от вида кривой, т.е. от процесса.
еометрическая
интерпретация интеграла – «площадь»
под кривой 1 – 2, а эта площадь зависит
от вида кривой, т.е. от процесса.
Если V2 < V1 то работа газа отрицательная, а работа внешних сил А* положительная и А* = – А.
Е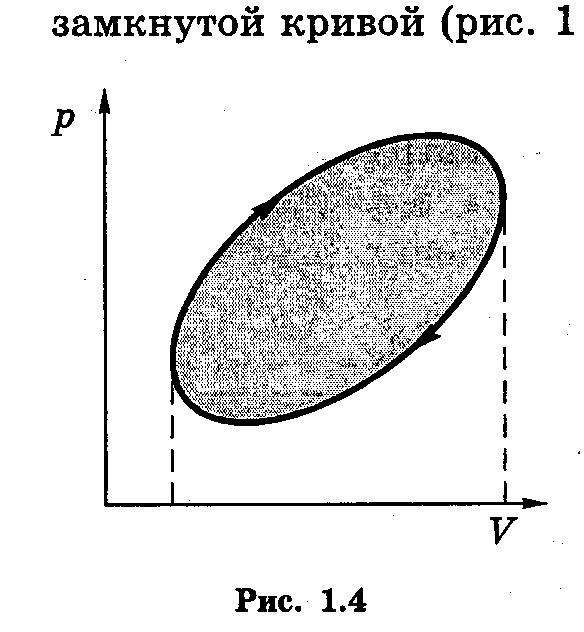 сли
в результате изменений макросистема
возвращается в исходное состояние, то
говорят, что она совершила круговой
процесс
или цикл.
На диаграмме p-V
такой процесс имеет вид замкнутой
кривой .
сли
в результате изменений макросистема
возвращается в исходное состояние, то
говорят, что она совершила круговой
процесс
или цикл.
На диаграмме p-V
такой процесс имеет вид замкнутой
кривой .
Работа, совершаемая системой за цикл, численно равна площади внутри цикла. При этом, если точка, изображающая состояние системы, описывает цикл по часовой стрелке, то работа системы А > 0, а если против часовой стрелки, то А < 0.
Первое начало термодинамики
Внутреннюю энергию макросистемы можно изменить, совершив над системой работу А* внешними макроскопическими силами, либо путём теплопередачи.
Совершение работы А* сопровождается перемещением внешних тел, действующих на систему (поршень, сжимающий газ в цилиндре).
Передача макросистеме тепла Q не связана с перемещением внешних тел. Она осуществляется путём непосредственной передачи внутренней энергии макросистеме от внешних тел при контакте с ними либо через излучение. Если Q > 0 , то это означает, что тепло подводится к системе, а если Q < 0 , то отводится.
U2 – U1 = ΔU = Q + A* = Q – A или
Q = ΔU + A
Последнее уравнение выражает первое начало термодинамики: количество теплоты Q, сообщённое макросистеме, идёт на приращение ΔU её внутренней энергии и на совершение системой работы над внешними телами.
В дифференциальной форме первое начало термодинамики имеет вид:
δQ = dU + δA , где
δQ
– элементарное значение теплоты
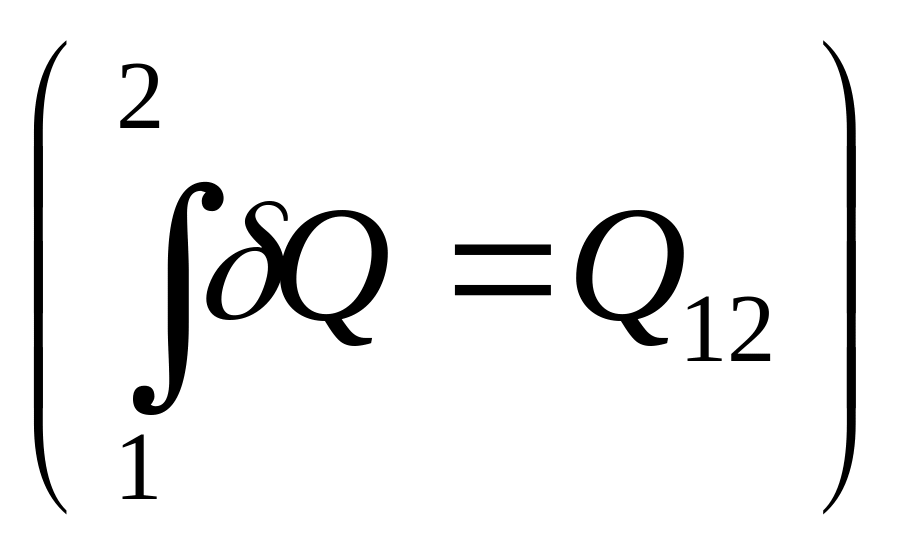 ;
;
δA
– элементарная работа системы
 ;
;
dU
– бесконечно малое изменение внутренней
энергии (полный дифференциал функции
состояния U
)
 .
.
Адиабатически изолированная термодинамическая система
Адиабатически изолированной термодинамической системой называют такую систему, в которой изменения её состояния могут происходить только благодаря механическим перемещениям частей оболочки (окружающих тел) и не могут происходить путём теплообмена с окружающими телами.
Изменение состояния адиабатически изолированной системы называют адиабатическим процессом, а оболочку, окружающую такую систему – адиабатической оболочкой.
Ещё в первой половине XIX в. Английский физик Дж.Джоуль экспериментально показал, что для адиабатического перехода термодинамической системы из определённого начального состояния в определённое конечное состояние всегда требуется одинаковая работа независимо от того, как осуществляется адиабатический переход.
Первое начало термодинамики для адиабатически изолированных систем имеет следующий вид:
ΔU12 = U2 – U1 = A*12 = – A12 .
