
- •Содержание
- •Введение
- •1 Инженерное образование
- •1.1 Овладение знаниями
- •1.2 Фактические знания инженера
- •1.3 Техническое образование в России
- •1.4 Подготовка инженера в высшем учебном заведении
- •1.4.1 Основные умения инженера
- •1.4.2 Требования к основной образовательной программе
- •1.5 Научные и инженерные основы технологии
- •1.5.1 Инженерное дело
- •1.5.2 Роль инженерного дела
- •1.5.3 Различие между наукой и инженерным делом
- •1.5.4 Специализация в инженерном деле
- •1.6 Основные свойства инженера
- •1.6.1 Представление
- •1.6.1.1 Моделирование
- •1.6.1.2 Упрощения, предположения, идеализация
- •1.6.1.3 Оптимизация
- •1.6.2 Формулировка задачи
- •1.6.3 Поиски возможных решений
- •1.6.4 Принятие решения
- •1.6.5 Спецификация решений
- •1.7 Квалификация инженера
- •1.7.1 Квалификационная характеристика выпускника по направлению подготовки «Химическая технология
- •1.7.2 Виды профессиональной деятельности выпускника
- •1.7.3 Квалификационные требования
- •1.8 Инженерные задачи
- •1.9 Инженерное дело на практике
- •1.10 Учебный план подготовки инженеров
- •2 Производство энергонасыщенных материалов и изделий
- •2.1 История возникновения и развития энергонасыщенных материалов и изделий
- •2.2 Открытие бризантных взрывчатых веществ
- •2.2.1 Применение бризантных взрывчатых веществ в артиллерии
- •2.2.2 Развитие отечественного производства бризантных взрывчатых веществ
- •2.3 История создания отечественных ракетных зарядов
- •2.3.1 Ракетные заряды из пироксилинотротилового пороха
- •2.3.2 Разработка нитроглицериновых баллиститных порохов для ствольной артиллерии
- •2.4 История развития и совершенствования производства отечественных боеприпасов
- •2.4.1 Стрелковые боеприпасы
- •2.4.2 Артиллерийские боеприпасы
- •2.5 История высшей школы по подготовке специалистов для отечественной пороховой промышленности
- •2.5.1 Бийский технологический институт Алтайского государственного университета им. И.И. Ползунова
- •2.5.2 История создания кафедры «Химическая технология высокомолекулярных соединений» Бийского технологического института
- •2.5.3 История создания кафедры «Технология химического машиностроения» Бийского технологического института
- •2.6 Классификация взрывчатых веществ
- •2.6.1 Инициирующие взрывчатые вещества
- •2.6.2 Бризантные взрывчатые вещества
- •2.6.2.1 Азотнокислые эфиры (нитраты)
- •2.6.2.2 Нитросоединения
- •2.6.3 Взрывчатые смеси, содержащие окислители
- •2.6.4 Метательные вв
- •2.6.4.1 Дымный порох
- •2.6.4.2 Нитроцеллюлозные пороха
- •2.7 Химия и технология получения бризантных вв
- •2.7.1 Технология получения основных ароматических
- •2.7.1.1 Тринитротолуол
- •2.7.1.2 Тринитрофенол
- •2.7.2 Технология получения нитросоединений алифатического ряда (нитропарафины)
- •2.7.2.1 Нитрометан
- •2.7.2.2 Тринитрометан
- •2.7.3 Технология получения алифатических
- •2.7.3.1 Гексоген
- •2.7.3.2 Октоген
- •2.7.4.1 Глицеринтринитрат
- •2.7.4.2 Пентаэритриттетранитрат
- •Литература
2.7.3.2 Октоген
Октоген (циклотетраметилентетранитрамин, 1,3,5,7-тетранитро- 1,3,5,7-тетразациклооктан) – высокоплавкое белое кристаллическое вещество, существующее в четырех кристаллических модификациях:
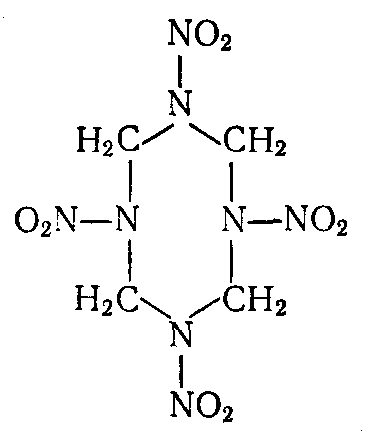
Октоген, обладая всеми достоинствами гексогена, выгодно отличается от него более высокой термостойкостью (до 220°С), большей плотностью и соответственно лучшими взрывчатыми характеристиками. Термостойкость позволяет использовать октоген в зарядах, подверженных воздействию высоких температур, например, при проведении взрывных работ в глубоких и сверхглубоких скважинах, в снарядах скорострельных автоматических пушек, в боеприпасах для сверхзвуковой авиации. Второе преимущество дает возможность существенно повысить плотность и эффективность применяемых взрывчатых материалов. Так, замена гексогена на октоген во взрывчатых смесях приводит к увеличению их скорости детонации, бризантности и мощности. Применяют октоген как в виде самостоятельных зарядов, так и в смеси с тротилом (октолы); используют его также в качестве окислителя в твердых ракетных топливах и артиллерийских порохах.
Технологический процесс получения октогена состоит из следующих этапов.
Нитролиз проводят в две стадии. На первой стадии к уксуснокислому раствору уротропина в присутствии уксусного ангидрида и параформальдегида прибавляют раствор нитрата аммония в азотной кислоте и уксусный ангидрид в количестве, обеспечивающем перевод уротропина в дициклодинитропентаметилентетрамин (ДПТ). На второй стадии в нитратор добавляют остальное количество реагентов.
После окончания
нитролиза добавляют воду, острым паром
доводят температуру массы до 98°С и
выдерживают ее при этой
температуре.
Смесь охлаждают, фильтруют, промывают
до нейтральной реакции и продукт
высушивают. Для выделения октогена
октоген-сырец растворяют в ацетоне и
кипятят раствор в течение 45 мин. За это
время любая форма октогена в горячем
ацетоне превращается в
![]() -форму.
Ацетон отгоняют с водяным паром.
-форму.
Ацетон отгоняют с водяным паром.
Стабилизацию проводят длительным кипячением водной суспензии -формы октогена после отгонки ацетона. Во время кипячения нестабильные соединения разлагаются. Затем продукт охлаждают, фильтруют и сушат. Сухой продукт содержит от 30 до 40 % гексогена и от 60 до 70 % октогена.
Предложен непрерывный способ прямого получения -модифи-кации октогена за счет энергичного перемешивания реагентов, длительной выдержки реакционной массы в последнем нитраторе и высокой температуры гидролиза побочных продуктов (рисунок 2.13). Растворы уротропина в уксусной кислоте и аммиачной селитры в азотной кислоте, а также уксусный ангидрид перед дозировкой их в нитратор 2 пропускают через термостат 1 для подогрева до температуры 40°С.
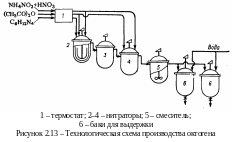
Процесс проводят в две стадии. На первой стадии в основной нитратор 2 дозируют весь раствор уротропина в уксусной кислоте, часть раствора аммиачной селитры в азотной кислоте и часть уксусного ангидрида в количествах, необходимых для образования промежуточных продуктов синтеза октогена. Нитромасса из нитратора 2 поступает в буферный нитратор 3 и затем в основной нитратор второй стадии 4, куда одновременно и непрерывно подается оставшаяся часть раствора аммиачной селитры в азотной кислоте и уксусный ангидрид. Далее нитромасса поступает в смеситель 5 и затем в один из баков выдержки 6. Время пребывания компонентов на первой стадии 30 мин, на второй – 64 мин (4 мин в нитраторе и 60 мин в смесителе). Во всех аппаратах поддерживается температура от 40 до 50°С. В бак выдержки 6 подают воду (для гидролиза побочных продуктов) и нагревают нитромассу до температуры 102°С, выдерживая ее при этой температуре 30 мин. По окончании выдержки нитромассу охлаждают и отфильтровывают октоген-сырец от отработанной уксусной кислоты. Октоген-сырец содержит от 20 до 30 % гексогена.
Нитраторы представляют собой емкости с рубашками, снабженные мощными мешалками, а также вращающимися скребками в виде лопаток для предотвращения прилипания вещества к стенкам аппарата. Октоген применяется в виде -модификации с температурой плавления 270°С и кислотностью по уксусной кислоте не выше 0,03 %. Транспортируют октоген в водонепроницаемых мешках (резиновых, прорезиненных, пластмассовых) в пастообразном виде с содержанием не менее 10 % смеси растворителей, состоящей из 40 % (масс.) изопропилового спирта и 60 % (масс.) воды.
2.7.4 Технология получения нитратов спиртов (О–NО2)
Нитраты спиртов, или нитроэфиры, составляют основу бездымных порохов и твердых ракетных топлив, а также входят в состав многих промышленных ВВ – динамитов, победитов, некоторых аммонитов и др. Ассортимент используемых для вооружения и промышленных целей нитроэфиров, который долгое время ограничивался нитроглицерином и пироксилином, все время расширяется. Широкому применению нитроэфиров в мирной технике, несмотря на их высокую чувствительность к механическим воздействиям и относительно низкую стойкость, способствует легкость получения, доступность исходных материалов и высокие взрывчатые свойства. Многие нитроэфиры способны пластифицировать высокомолекулярный нитроэфир – нитрат целлюлозы, что используется при производстве высокоэнергетического баллиститного пороха. По свойствам нитроэфиры резко отличаются от нитросоединений и нитраминов.
