
- •Содержание
- •Введение
- •1 Инженерное образование
- •1.1 Овладение знаниями
- •1.2 Фактические знания инженера
- •1.3 Техническое образование в России
- •1.4 Подготовка инженера в высшем учебном заведении
- •1.4.1 Основные умения инженера
- •1.4.2 Требования к основной образовательной программе
- •1.5 Научные и инженерные основы технологии
- •1.5.1 Инженерное дело
- •1.5.2 Роль инженерного дела
- •1.5.3 Различие между наукой и инженерным делом
- •1.5.4 Специализация в инженерном деле
- •1.6 Основные свойства инженера
- •1.6.1 Представление
- •1.6.1.1 Моделирование
- •1.6.1.2 Упрощения, предположения, идеализация
- •1.6.1.3 Оптимизация
- •1.6.2 Формулировка задачи
- •1.6.3 Поиски возможных решений
- •1.6.4 Принятие решения
- •1.6.5 Спецификация решений
- •1.7 Квалификация инженера
- •1.7.1 Квалификационная характеристика выпускника по направлению подготовки «Химическая технология
- •1.7.2 Виды профессиональной деятельности выпускника
- •1.7.3 Квалификационные требования
- •1.8 Инженерные задачи
- •1.9 Инженерное дело на практике
- •1.10 Учебный план подготовки инженеров
- •2 Производство энергонасыщенных материалов и изделий
- •2.1 История возникновения и развития энергонасыщенных материалов и изделий
- •2.2 Открытие бризантных взрывчатых веществ
- •2.2.1 Применение бризантных взрывчатых веществ в артиллерии
- •2.2.2 Развитие отечественного производства бризантных взрывчатых веществ
- •2.3 История создания отечественных ракетных зарядов
- •2.3.1 Ракетные заряды из пироксилинотротилового пороха
- •2.3.2 Разработка нитроглицериновых баллиститных порохов для ствольной артиллерии
- •2.4 История развития и совершенствования производства отечественных боеприпасов
- •2.4.1 Стрелковые боеприпасы
- •2.4.2 Артиллерийские боеприпасы
- •2.5 История высшей школы по подготовке специалистов для отечественной пороховой промышленности
- •2.5.1 Бийский технологический институт Алтайского государственного университета им. И.И. Ползунова
- •2.5.2 История создания кафедры «Химическая технология высокомолекулярных соединений» Бийского технологического института
- •2.5.3 История создания кафедры «Технология химического машиностроения» Бийского технологического института
- •2.6 Классификация взрывчатых веществ
- •2.6.1 Инициирующие взрывчатые вещества
- •2.6.2 Бризантные взрывчатые вещества
- •2.6.2.1 Азотнокислые эфиры (нитраты)
- •2.6.2.2 Нитросоединения
- •2.6.3 Взрывчатые смеси, содержащие окислители
- •2.6.4 Метательные вв
- •2.6.4.1 Дымный порох
- •2.6.4.2 Нитроцеллюлозные пороха
- •2.7 Химия и технология получения бризантных вв
- •2.7.1 Технология получения основных ароматических
- •2.7.1.1 Тринитротолуол
- •2.7.1.2 Тринитрофенол
- •2.7.2 Технология получения нитросоединений алифатического ряда (нитропарафины)
- •2.7.2.1 Нитрометан
- •2.7.2.2 Тринитрометан
- •2.7.3 Технология получения алифатических
- •2.7.3.1 Гексоген
- •2.7.3.2 Октоген
- •2.7.4.1 Глицеринтринитрат
- •2.7.4.2 Пентаэритриттетранитрат
- •Литература
2.7.2.1 Нитрометан
Нитрометан СН3О2 применяется в ряде стран в качестве компонента ракетного топлива и как добавка к дизельному топливу. Его используют как растворитель для нитратов целлюлозы и как взрывчатое вещество для производства буровзрывных работ при добыче нефти, а в композиции с желатинизатором (нитратом целлюлозы) и сенсибилизатором – для снаряжения детонирующего шнура. Может служить исходным продуктом для получения трихлорнитрометана, тетранитрометана и ряда ВВ.
Нитрометан – бесцветная жидкость со следующими физическими характеристиками:
чувствительность к удару (груз массой 10 кг, h = 25 см) – 0…8 %;
расширение в бомбе Трауцля – 470 мл;
бризантность по Гессу – 25 мм;
скорость детонации – 6600 м/с.
Получают нитрометан в промышленном масштабе при газофазном нитровании алифатических углеводородов, а также рядом косвенных методов. Практическое значение имеет метод получения нитрометана из диметилсульфата или натриевой соли метилсульфата, а также действием хлоруксусной кислоты на нитрит калия или натрия в водном растворе. Образующаяся при этом нитроуксусная кислота разлагается при кипячении с водой:
СlСН2СООН + NaNO2 СH2(NО2)СООН СН3NО2 + СО2
В лаборатории нитрометан получают также действием нитрита серебра на иодистый или бромистый метил.
2.7.2.2 Тринитрометан
Тринитрометан СН(NО2)3 (нитроформ) впервые был получен в 1857 г. Шишковым. Благодаря чрезвычайно высокой реакционной способности он широко используется для синтеза полинитросоединений.
Чистый безводный нитроформ представляет собой бесцветное кристаллическое вещество, обладающее характерным резким запахом. Температура затвердевания его 26,38°С, но сильно понижается в присутствии примесей. Температура кипения 45…47°С при давлении 2,9 кПа, плотность 1,615 г/см3.
Быстрое нагревание вызывает взрыв нитроформа. В обычных условиях он относительно устойчив и на холоде может сохраняться без изменений. Концентрированные минеральные кислоты при высокой температуре вызывают разложение нитроформа.
Получение нитроформа из ацетилена. Реакция превращения ацетилена в тринитро- и затем в тетранитрометан действием азотной кислоты была открыта в 1900 г., но выход продукта не превышал 20…25 %. В 1920 г. в качестве катализатора был применен нитрат ртути и выход увеличился до 40…45 %. Позже было установлено положительное влияние окислов азота на выход тетранитрометана и на скорость процесса. Некоторые металлы (Fе, Ni, Со, Аl) являются ингибиторами этого процесса. Основные реакции можно представить следующим образом:
СН=СН + 5НNО3 СН(NО2)3 + СО2 + 3Н2О + 2NО2
CН(NО2)3 + HNО3 С(NO2)4 + Н2О
На рисунке 2.11 показана схема установки нитрования. Основным аппаратом является нитратор 6, представляющий собой колонну с наружной трубой для циркуляции раствора. Внутри нитратора расположены вертикальные трубки. В межтрубное пространство подается вода для охлаждения. Ниже трубок находится распределитель для подачи ацетилена и азотной кислоты, вверху трубки соединены переливной трубой, по которой часть нитромассы выводится на дистилляцию, а остаток направляется в наружную трубу для циркуляции внутри системы. В нитраторе поддерживается температура от 45 до 48°С. Из переливной трубы реакционная смесь (13 % нитроформа, 77 % НNО3, 10 % Н2О) подается в колонну 7, где в противотоке с воздухом освобождается от окислов азота. Воздух затем очищают от окислов азотной кислотой, охлажденной до температуры минус 15°С; кислоту используют для нитрования.
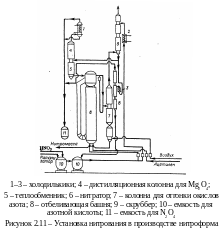
Газы, образующиеся при нитровании (СО2, СО, N2О3, небольшое количество нитроформа и частично окисленный ацетилен), проходят скруббер 9, где вымывается нитроформ, и поступают в охлаждаемую рассолом колонну 4 для конденсации N2О4. Выход нитроформа повы-
шается с увеличением высоты нитратора, скорости подачи ацетилена и с уменьшением количества нитроформа, циркулирующего в системе.
