
- •Глава 3. Биологическая очистка сточных вод в анаэробных условиях
- •3.1. Характеристика метанового брожения
- •3.2. Факторы, влияющие на процесс анаэробной очистки стоков
- •3.2.1. Состав и концентрация загрязнений
- •3.2.2. Величина рН сточной воды и температура процесса
- •3.2.3. Наличие в сточной воде биогенных элементов, ингибиторов и токсичных веществ
- •3.3.Кинетические закономерности функционирования анаэробных биореакторов
- •Кинетические параметры роста анаэробных
- •3.4. Конструкции современных анаэробных биореакторов
- •3.4.1. Анаэробный биофильтр с восходящим потоком жидкости
- •1 − Поддерживающая решетка; 2 − слой засыпного загрузочного материала; а − исходная сточная вода; б − биогаз; в − очищенная сточная вода
- •3.4.2. Биореактор с нисходящим потоком жидкости
- •1 − Поддерживающая решетка;
- •2 − Слой вертикально ориентированного загрузочного материала;
- •3.4.3. Биореактор с гранулированной биомассой активного ила
- •3.4.4. Комбинированный (гибридный) биореактор
- •1 − Распределительная система; 2 − поддерживающая решетка;
- •3 − Слой загрузочного материала;
- •3.4.5. Биореактор с псевдоожиженным слоем носителя.
- •1 − Распределительная система; 2 − слой частиц носителя; 3 − насос;
- •3.5.Технологические особенности анаэробных методов очистки сточных вод
3.2.3. Наличие в сточной воде биогенных элементов, ингибиторов и токсичных веществ
Как уже отмечалось, анаэробный биоценоз вследствие низкого прироста биомассы менее требователен к содержанию в реакционной среде биогенных элементов, чем аэробный активный ил. Если для аэробного процесса необходимые количества азота и фосфора определяются соотношением БПК : N : P = 100 : 5 : 1, то при анаэробной очистке достаточно количества этих элементов в пропорции 100 : 1 : 0,2.
Имеет значение соотношение С : N, оптимальная величина которого колеблется по различным данным от 20 : 1 до 100 : 1. При большей доле азота в сточной воде наблюдается ингибирование метаногенеза высокой концентрацией образующегося аммиака, который присутствует в реакционной среде в двух находящихся в равновесии формах: в виде растворенного аммиака и иона аммония. Более токсичным является растворенный аммиак, при концентрации которого 50 мг/дм3 скорость биохимических превращений уменьшается в 2 раза. Кроме аммиака, ингибирующим действием при высокой концентрации обладают собственные интермедиаты метаногенеза − ЛЖК и водород, а также побочный продукт − сероводород. Ингибирующий эффект ЛЖК проявляется при концентрации 2000 мг/дм3, причем большей токсичностью обладают не анионы кислот, а недиссоциированные молекулы, которые легче проникают через клеточную стенку микроорганизмов. Наиболее токсична и трудноразлагаема из ЛЖК –пропионовая кислота.
Если рН реакционной среды >7, то концентрация недиссоциированных молекул ЛЖК низкая и ингибирование маловероятно.
Сильным ингибитором является водород. При нарушении баланса в образовании и потреблении водорода и достижении концентрации его в газовой фазе 0,2−0,5% метаногенез затормаживается. Присутствие в сточной воде соединений серы приводит к развитию сульфатвосстанавливающих бактерий, продуцирующих сероводород, который распределяется между газовой и жидкой фазами. Токсичностью обладает растворенный сероводород при концентрации свыше 200 мг/дм3. Продукт его диссоциации − сульфид-ион − не токсичен. В процессе метаногенеза часть растворенного сероводорода взаимодействует с тяжелыми металлами с образованием нерастворимых в воде сульфидов, что способствует предотвращению ингибирования.
В числе потенциально токсичных соединений являются также тяжелые металлы, антибиотики, галогенсодержащие органические соединения и другие ксенобиотики. В то же время установлено, что микроорганизмы метанового биоценоза обладают достаточно высокими адаптационными способностями и проблема ингибирования биометаногенеза не так серьезна, как предполагали раньше.
3.3.Кинетические закономерности функционирования анаэробных биореакторов
Сложность и многообразие протекающих при метановом сбраживании процессов сильно затрудняет математическое моделирование биореакторов. Разработанные к настоящему времени модели применимы в определенных границах и описывают функционирование биореакторов второго поколения с различной степенью адекватности. Они непрерывно совершенствуются и имеют своей целью прогнозирование, управление и интенсификацию процесса.
В практике проектирования анаэробных установок пользуются упрощенными эмпирическими моделями на основе теории хемостата.
Если не учитывать сложность составов как загрязнений сточной воды, так и метанового биоценоза, то для описания кинетики процесса в проточном биореакторе с идеальным перемешиванием можно использовать уравнения хемостатной культуры:

(1)
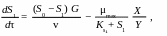
(2)
где X, X1 − концентрация биомассы в биореакторе и в очищенной сточной воде на выходе из биореактора соответственно, кг/м3;
μmax − максимальная удельная скорость роста биомассы, сут−1;
Ks – константа, численно равная концентрации биомассы, при которой μ = 0,5 μmax, кг/м3;
b − удельная скорость отмирания биомассы, сут−1;
S0, S1 − концентрация загрязнений в исходной и очищенной сточной воде соответственно, кг ХПК/м3;
G − скорость протока сточной воды, м3/сут;
v − рабочий объем биореактора, м3;
Y − экономический коэффициент (выход биомассы от деструктированных загрязнений), кг/кг ХПК.
Удельная скорость роста биомассы μ зависит от концентрации субстрата S по уравнению Моно:
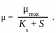
(3)
В установившемся режиме функционирования биореактора имеем:
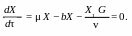
(4)
Следует отметить, что для биореактора, не удерживающего биомассу активного ила, X = X1.
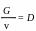
Отношение представляет собой удельную скорость
р азбавления
ферментационной среды в биореакторе,
сут−1.
Этот параметр
часто выражают в виде процентной суточной
дозы загрузки
биореактора:
азбавления
ферментационной среды в биореакторе,
сут−1.
Этот параметр
часто выражают в виде процентной суточной
дозы загрузки
биореактора:
После преобразования уравнения (3.4) получим:

т. е. «чистая» удельная скорость прироста биомассы равна:

(5)
Отсюда возраст биомассы
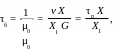
(6)
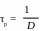
г
 де
− время пребывания сточной воды
в биореакторе, сут.
де
− время пребывания сточной воды
в биореакторе, сут.
Из уравнения (6) следует, что , где называют коэффициентом выноса биомассы.
Для биореакторов первого поколения (метантенков со свободными клетками микроорганизмов) X = X1, f = 1, а следовательно,
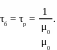
(7)
Это означает, что проток сточной воды не может быть больше величины максимальной «чистой» удельной скорости роста метаногенного биоценоза и на практике соответствует времени пребывания стока в метантенке, функционирующем в мезофильном режиме, 10−15 сут.
Для биореакторов второго поколения величина коэффициента выноса биомассы значительно меньше единицы и составляет 0,005−0,1, что обеспечивает возможность устойчивой работы биореактора при гидравлической нагрузке, в 10−200 раз превышающей значение удельной скорости роста биомассы, что соответствует времени пребывания сточной воды в аппарате 0,5−10 ч.
В стационарном режиме работы биореактора из уравнения (2) следует:
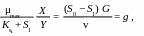
(8)
где g − удельная производительность биореактора по деструктируемым загрязнениям, кг ХПК/(м3 ˙ сут).
Удельный выход метана (на единицу объема жидкой среды в аппарате) связан с удельной производительностью через коэффициент выхода метана из единицы массы деструктированных загрязнений:
gм = g yм,
где gм − удельный выход метана, м3/(м3 ˙ сут);
yм − выход метана, м3/кг ХПК.
Приведенные уравнения справедливы как для кислотогенной и метаногенной стадий в отдельности, так и для процесса анаэробной очистки в целом (табл. 6).
Таблица 6
