
- •Введение в аминокислоты
- •Аминокислоты объединяют по разным признакам
- •Классификация аминокислот
- •Двадцать аминокислот необходимы для синтеза белка
- •Право- и левовращающие формы аланина
- •Для аминокислот характерна амфотерность
- •Изменение заряда аминокислот при смещении рН раствора в кислую или щелочную сторону. Аминокислоты соединяются пептидной связью
- •Участок белковой цепи длиной в 6 аминокислот (Сер-Цис-Тир-Лей-Глу-Ала) (пептидные связи выделены желтым цветом, аминокислоты - красной рамкой)
- •Участие водородных связей в формировании вторичной структуры
- •Укладка белка в виде β-складчатого слоя
- •Свойства белков следуют из их строения
- •Амфотерность
- •Влияние рН на заряд белка
- •Растворимость
- •Удаление белков из раствора
- •Денатурация
- •1. Физическая денатурация
- •2. Химическая денатурация
- •Высаливание
- •Классификация по строению
- •Простые белки
- •Альбумины
- •Глобулины
- •Картина электрофореза белков сыворотки крови
- •Гистоны
- •Протамины
- •Коллаген
- •Эластин
- •Роль десмозина в соединении белков
- •Способ присоединения фосфата к белку на примере серина и тирозина Фосфорная кислота может выполнять:
- •Изменение конформации белка в фосфорилированном и дефосфорилированном состоянии
- •Строение липопротеинаВыделяют четыре основных класса липопротеинов:
- •Гликопротеины
- •Способ присоединения углевода к белку Функцией гликопротеинов являются:
- •Протеогликаны
- •Строение гиалуроновой кислоты и хондроитинсульфата
- •Гемопротеины
- •Цитохромы
- •Флавопротеины
Аминокислоты объединяют по разным признакам
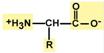
Аминокислоты –это строительные блоки макромолекул белков. По строению они являются органическими карбоновыми кислотами, у которых, как минимум, один атом водорода замещен на аминогруппу. Таким образом, в аминокислотах обязательно присутствует карбоксильная группа (СООН), аминогруппа (NH2), асимметричный атом углерода и боковая цепь (радикал R). Именно строением боковой цепи аминокислоты и отличаются друг от друга.
Классификация аминокислот
Из-за разнообразного строения и свойств классификация аминокислот может быть различной, в зависимости от выбранного качества аминокислот. Аминокислоты подразделяются:
1. В зависимости от положения аминогруппы по отношению к С2 (α-углеродный атом) на α-аминокислоты, β-аминокислоты и др.
2. По абсолютной конфигурации молекулы на L- и D-стереоизомеры.
3. По оптической активности в отношении плоскости поляризованного света – на право- и левовращающие.
4. По участию аминокислот в синтезе белков – протеиногенные и непротеиногенные.
5. По строению бокового радикала – ароматические, алифатические, содержащие дополнительные СООН- и NH2-группы.
6. По кислотно-основным свойствам – нейтральные, кислые, основные.
7. По необходимости для организма – заменимые и незаменимые.
Двадцать аминокислот необходимы для синтеза белка
Среди многообразия аминокислот только 20 участвует во внутриклеточном синтезе белков (протеиногенные аминокислоты). Также в организме человека обнаружено еще около 40 непротеиногенных аминокислот.
Все протеиногенные аминокислоты являются α-аминокислотами. На их примере можно показать дополнительные способы классификации. Названия аминокислот обычно сокращаются до 3-х буквенного обозначения. Профессионалы в молекулярной биологии также используют однобуквенные символы для каждой аминокислоты.
По строению бокового радикала
Выделяют алифатические (аланин, валин, лейцин, изолейцин, пролин, глицин), ароматические (фенилаланин, тирозин, триптофан), серусодержащие (цистеин, метионин), содержащие ОН-группу (серин, треонин, опять тирозин), содержащие дополнительную СООН-группу (аспарагиновая и глутаминовая кислоты) и дополнительную NH2-группу (лизин, аргинин, гистидин, также глутамин, аспарагин).
Строение протеиногенных аминокислот
По полярности бокового радикала
Существуют неполярные аминокислоты (ароматические, алифатические) и полярные (незаряженные, отрицательно и положительно заряженные).
По кислотно-основным свойствам
По кислотно-основным свойствам подразделяют нейтральные (большинство), кислые (аспарагиновая и глутаминовая кислоты) и основные (лизин, аргинин, гистидин) аминокислоты.
По незаменимости
По необходимости для организма выделяют такие, которые не синтезируются в организме и должны поступать с пищей – незаменимые аминокислоты (лейцин, изолейцин, валин, фенилаланин, триптофан, треонин, лизин, метионин). К заменимым относят такие аминокислоты, углеродный скелет которых образуется в реакциях метаболизма и способен каким-либо образом получить аминогруппу с образованием сответствующей аминокислоты. Две аминокислоты являются условно незаменимыми (аргинин, гистидин), т.е.их синтез происходит в недостаточном количестве, особенно это касается детей.
Аминокислоты обладают изомерией
Изомерия аминокислот в зависимости от положения аминогруппы
В зависимости от положения аминогруппы относительно 2-го атома углерода выделяют α-, β-, γ- и другие аминокислоты.
α- и β- формы аланина
Для организма млекопитающих наиболее характерны α-аминокислоты.
Изомерия по абсолютной конфигурации
По абсолютной конфигурации молекулы выделяют D- и L-формы. Различия между изомерами связаны с взаимным расположением четырех замещающих групп, находящихся в вершинах воображаемого тетраэдра, центром которого является атом углерода в α-положении. Имеется только два возможных расположения химических групп вокруг него.
Две конформации тетраэдра
В белке любого организма содержится только один стереоизомер, для млекопитающих это L-аминокислоты.
L- и D-формы аланина
Однако оптические изомеры претерпевают самопроизвольную неферментативную рацемизацию, т.е. L-форма переходит в D-форму. Данное обстоятельство используется для определения возраста, например, костной ткани зуба (в криминалистике, археологии).
Деление изомеров по оптической активности
По оптической активности аминокислоты делятся на право- и левовращающие.
Наличие в аминокислоте ассиметричного α-атома углерода (хирального центра) делает возможным только два расположения химических групп вокруг него. Это приводит к особому отличию веществ друг от друга, а именно – изменению направления вращения плоскости поляризации поляризованного света, проходящего через раствор. Величину угла поворота определяют при помощи поляриметра. В соответствии с углом поворота выделяют правовращающие (+) и левовращающие (–) изомеры.
