
- •БиооргаНическая химия
- •Содержание
- •1. Строение и номенклатура органических соединений. Химическая связь. Электронные эффекты
- •1.1 Введение
- •1.2 Теории строения органических соединений
- •Основные положения теории строения органических соединений а.М. Бутлерова
- •Алкены Алкадиены Алкины
- •1.4 Номенклатура органических соединений
- •1.5 Изомерия органических соединений
- •1.6 Электронное строение атома углерода, гибридизация
- •1.7 Сопряженные системы
- •1.8 Электронные эффекты (индуктивный и мезомерный)
- •1.9 Кислотность и основность органических соединений
- •2. Общая характеристика реакций органических соединений.
- •2.1 Общая характеристика химических реакций
- •2.2 Радикальные реакции
- •2.3 Реакции электрофильного присоединения
- •2.5 Нуклеофильные реакции
- •2.6 Окислительно-восстановительные реакции (овр)
- •3. Поли- и гетерофункциональные соединения, участвующие в процессах жизнедеятельности
- •3.5. Классы гетерофункциональных соединений
- •3.6 Гетерофункциональные производные бензола как лекарственные средства
- •4. Биологически важные гетероциклические соединения
- •5. Аминокислоты, пептиды, белки
- •5.3 Пептиды.
- •5.5 Пространственное строение полипептидов и белков
- •6. Углеводы: моно, ди- и полисахариды
- •6.4 Олиго- и полисахариды
- •7. Нуклеотиды и нуклеиновые кислоты
- •7.1. Нуклеозиды.
- •7.2. Нуклеотиды.
- •8. Липиды и низкомолекулярные биорегуляторы
- •8. 1 Простые омыляемые липиды
- •8.2. Сложные омыляемые липиды
- •8.3 Неомыляемые липиды или низкомолекулярные биорегуляторы
- •9. Практикум лабораторный
- •9.1. Правила техники безопасности при работе в химической лаборатории
- •9.2. Общие закономерности реакционной способности органических соединений
- •3. Строение и свойства биополимеров
- •Литература
- •Биоорганическая химия Учебное пособие
8. Липиды и низкомолекулярные биорегуляторы
Липиды — природные жироподобные вещества, практически нерастворимые в воде, хорошо растворимые в неполярных органических растворителях.
Липиды не являются биополимерами, однако наряду с ними выполняют чрезвычайно важные функции в организме:
– являются структурными элементами клеточных мембран (в виде комплекса с белками);
– при их окислении синтезируются молекулы АТФ, являющиеся источниками энергии для организма;
– являются запасными веществами;
– выполняют в организме защитную функцию;
– функционируют как биорегуляторы метаболических процессов.
Липиды чаще всего классифицируют по их способности к гидролизу на омыляемые (содержат сложноэфирные связи, способные гидролитически расщепляться) и неомыляемые (не содержат сложноэфирных связей и не подвергаются гидролизу).
Омыляемые липиды подразделяют на простые и сложые. Простые липиды состоят только из остатков высших кислот и спиртов, образующих сложные эфиры; к ним относят воски и жиры. В состав сложных липидов входят, кроме того, остатки фосфорной кислоты, моно- и дисахаридов. К сложным омыляемым липидам относятся, прежде всего, фосфолипиды, гликолипиды и сфинголипиды.
Неомыляемые липиды не содержат жирнокислотных остатков, соединенных сложноэфирной связью, поэтому в щелочной среде они не гидролизуются с образованием жирных кислот и не образуют мыла. К данной группе липидов относят стероиды и терпены, а также жирорастворимые пигменты, витамины.
8. 1 Простые омыляемые липиды
Животные жиры и растительные масла имеют единую химическую природу. Их молекулы представляют собой триацилглицерины — сложные эфиры трёхатомного спирта глицерина и высших алифатических кислот. Кислоты, выделенные из жиров, часто так и называют жирными кислотами. Номенклатура жиров основана на названии кислот, входящих в их состав с указанием номера глицеринового атома углерода, с которым соединён остаток кислоты, например:

Как запасные вещества триацилглицерины обладают рядом преимуществ перед углеводами и белками. Они не растворимы в воде и клеточном соке и, следовательно, не влияют на физико-химические свойства цитоплазмы; до омыления ни в какие реакции в водной среде не вступают. Триацилглицерины выполняют, кроме того, функции поставщиков энергии, восполняя около 45 % суммарной энергетической потребности организма.
В составе природных триацилглицеринов обнаружено несколько десятков различных жирных кислот. Однако в жирах организма около 85 % составляют: олеиновая С17Н33СООН, пальмитиновая C15H31COOH и линолевая C17H31COOH кислоты.
Жирные кислоты, входящие в состав липидов высших растений и животных, обладают рядом общих свойств:
1) содержат четное число атомов углерода, чаще 16 или 18 атомов;
2) имеют неразветвленную углеродную цепь;
3) ненасыщенные кислоты имеют цис-конфигурацию;
4) в полиненасыщенных жирных кислотах растительного происхождения обнаружены сопряженные двойные связи: –СН=СН–СН=СН–; а в жирных кислотах животных липидов — дивинилметановые фрагменты: –СН=СН–СН2–СН=СН–
Е сли
в составе триацилглицеринов присутствуют,
преимущественно, предельные кислоты,
то жир имеет твёрдую консистенцию
(свиной жир, сливочное масло). Если же
преобладают ненасыщенные кислоты, то
агрегатное состояние жира — жидкое
(растительные масла). Природные
непредельные кислоты имеют цис-конфигурацию
относительно двойных связей. Углеводородный
радикал кислоты в цис-конфигурации
имеет изогнутый и укороченный вид,
молекулы занимают больший объём, а при
образовании кристаллов упаковываются
менее плотно, чем транс-изомеры. Отсюда
и разница в температурах плавления и
агрегатном состояниии кислот. Так,
олеиновая кислота при комнатной
температуре — жидкая, а её транс-изомер,
элаидиновая кислота — твёрдая.
сли
в составе триацилглицеринов присутствуют,
преимущественно, предельные кислоты,
то жир имеет твёрдую консистенцию
(свиной жир, сливочное масло). Если же
преобладают ненасыщенные кислоты, то
агрегатное состояние жира — жидкое
(растительные масла). Природные
непредельные кислоты имеют цис-конфигурацию
относительно двойных связей. Углеводородный
радикал кислоты в цис-конфигурации
имеет изогнутый и укороченный вид,
молекулы занимают больший объём, а при
образовании кристаллов упаковываются
менее плотно, чем транс-изомеры. Отсюда
и разница в температурах плавления и
агрегатном состояниии кислот. Так,
олеиновая кислота при комнатной
температуре — жидкая, а её транс-изомер,
элаидиновая кислота — твёрдая.
Рисунок 11 – Шаростержневые модели молекул транс- (вверху) и цис- (внизу) изомеров олеиновой (а), линолевой (б), линоленовой (в) кислот.
Цис- конфигурация непредельных кислот менее устойчива, чем транс-конфигурация. Это делает пищевые жиры более подверженными катаболизму, они легче перевариваются.
Реакции гидролиза. Гидролиз — первая стадия метаболизма пищевых жиров в организме. При гидролизе нейтральных жиров образуются кислоты и глицерин. В организме эта реакция катализируется ферментами — липазами. Вне организма гидролиз жира происходит при его нагревании в присутствии кислот или щелочей.
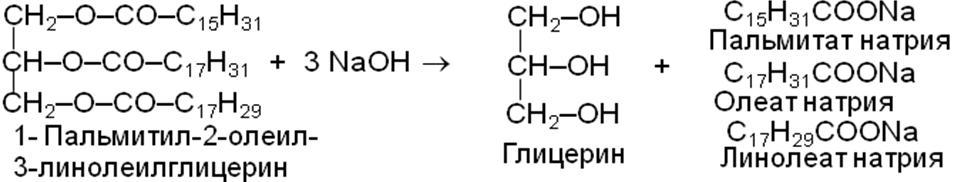
В последнем случае образуются соли жирных кислот — мыла, а реакция называется омылением. Мыла, так же как и многие сложные липиды, обладают поверхностной активностью (являются поверхностно-активными веществами, ПАВ).
Реакции присоединения. Липиды с остатками непредельных кислот присоединяют по двойным связям водород галогены, галогеноводороды, воду в кислой среде. На способности ненасыщенных кислот присоединять по месту двойной связи галогены основан один из методов определения степени ненасыщенности жирных кислот и масел.
Ж идкие
жиры могут быть превращены в твердые
путем гидрирования, т.е. присоединения
водорода по двойным связям непредельных
кислот в присутствии катализаторов
идкие
жиры могут быть превращены в твердые
путем гидрирования, т.е. присоединения
водорода по двойным связям непредельных
кислот в присутствии катализаторов
Реакция гидрирования растительных масел используется в промышленных масштабах для получения маргаринов и «мягких» масел, не содержащих холестерина. Холестерин в таких продуктах действительно отсутствует (ведь растения не вырабатывают холестерин). Однако установлено, что в процессе гидрирования происходит также цис-транс- изомеризация углеводородных радикалов кислот, доля транс-изомеров в «мягких» маслах может достигать 10 %, в дешёвых маргаринах — 50 %. Присутствие транс-изомеров увеличивает риск атеросклероза и связанных с ним сердечно-сосудистых заболеваний. Полученные в процессе катаболизма таких маргаринов транс-кислоты могут встраиваться в фосфолипиды клеточных мембран, изменяя при этом их физические свойства, что может быть причиной метаболических и функциональных расстройств.
Под действием света, кислорода и влаги жиры подвергаются пероксидному окислению и расщеплению. Легче всего окисляются непредельные жирные кислоты, входящие в состав жира. Кислород, присоединяясь по двоной связи, образует пероксиды. Далее происходит разрыв углеродной цепи по месту бывшей связи, образуются альдегиды и кислоты с меньшим числом атомов углерода, имеющие неприятный запах и вкус прогорклого жира.
Воски. Представляют собой сложные эфиры высших одноатомных спиртов алифатического (реже ароматического) ряда и высших жирных кислот. Кроме того, природные воски содержат свободные спирты с четным числом атомов углерода n = 26…32, высшие жирные кислоты с числом атомов углерода n = 14…34, а также алканы с нечетным числом атомов углерода n = 21…37. Общее количество этих примесей может достигать 50 %.
Воски составляют около 80 % всех липидов растений и выполняют в основном защитную функцию, предохраняя органы и ткани от потери тепла, влаги, от механических повреждений и проникновения микроорганизмов.
В состав восков входят как обычные жирные кислоты, так и специфические: карнаубовая С23Н47СООН, церотиновая С26Н53СООН. Наиболее часто в составе восков встречаются спирты: стеариновый С18Н37ОН, цетиловый СН3(СН2)14СН2ОН, мирициловый C31H63OH и др.
Воски подразделяют на простые и сложные. К простым воскам относят эфиры высших жирных кислот и высших первичных спиртов. Сложные воски представляют собой эфиры разветвленных одно- и двухатомных спиртов и разветвленных жирных кислот или оксикислот.
В отличие от триацилглицеринов воски более устойчивы к действию света, окислителей, нагреванию; хуже гидролизуются. Универсальным свойством восков является их высокая пластичность в нагретом состоянии при температурах, значительно ниже температур плавления. Так, большинство восков имеют температуру плавления 60…64 °С, а температуру размягчения (перехода в высокопластичное состояние) около 36-38 °С. Кроме того, большинство восков плавятся, не давая твердого остатка. Именно эти свойства обусловили, в частности, широкое применение восков в качестве моделировочных материалов в ортопедической стоматологии.
