
- •БиооргаНическая химия
- •Содержание
- •1. Строение и номенклатура органических соединений. Химическая связь. Электронные эффекты
- •1.1 Введение
- •1.2 Теории строения органических соединений
- •Основные положения теории строения органических соединений а.М. Бутлерова
- •Алкены Алкадиены Алкины
- •1.4 Номенклатура органических соединений
- •1.5 Изомерия органических соединений
- •1.6 Электронное строение атома углерода, гибридизация
- •1.7 Сопряженные системы
- •1.8 Электронные эффекты (индуктивный и мезомерный)
- •1.9 Кислотность и основность органических соединений
- •2. Общая характеристика реакций органических соединений.
- •2.1 Общая характеристика химических реакций
- •2.2 Радикальные реакции
- •2.3 Реакции электрофильного присоединения
- •2.5 Нуклеофильные реакции
- •2.6 Окислительно-восстановительные реакции (овр)
- •3. Поли- и гетерофункциональные соединения, участвующие в процессах жизнедеятельности
- •3.5. Классы гетерофункциональных соединений
- •3.6 Гетерофункциональные производные бензола как лекарственные средства
- •4. Биологически важные гетероциклические соединения
- •5. Аминокислоты, пептиды, белки
- •5.3 Пептиды.
- •5.5 Пространственное строение полипептидов и белков
- •6. Углеводы: моно, ди- и полисахариды
- •6.4 Олиго- и полисахариды
- •7. Нуклеотиды и нуклеиновые кислоты
- •7.1. Нуклеозиды.
- •7.2. Нуклеотиды.
- •8. Липиды и низкомолекулярные биорегуляторы
- •8. 1 Простые омыляемые липиды
- •8.2. Сложные омыляемые липиды
- •8.3 Неомыляемые липиды или низкомолекулярные биорегуляторы
- •9. Практикум лабораторный
- •9.1. Правила техники безопасности при работе в химической лаборатории
- •9.2. Общие закономерности реакционной способности органических соединений
- •3. Строение и свойства биополимеров
- •Литература
- •Биоорганическая химия Учебное пособие
3.6 Гетерофункциональные производные бензола как лекарственные средства
Среди монофункциональных производных бензола особое место занимает производное с карбоксильной группой — бензойная кислота, применяемая в медицине в виде натриевой соли (натрия бензоат) как отхаркивающее средство.
Бензойная кислота в свободном виде встречается в некоторых смолах и бальзамах, а также клюкве, бруснике, но чаще содержится в связанном виде, например, в виде N-бензоильного производного аминоуксусной кислоты C6H5CONHCH2COOH, называемого гиппуровой кислотой. Гиппуровая кислота образуется в печени при взаимодействии бензойной и аминоуксусной кислот, выводится с мочой. В клинической практике по количеству гиппуровой кислоты в моче больных (после приема бензоата натрия) судят об эффективности обезвреживающей функции печени.
К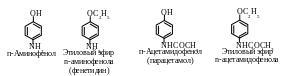 ак
гетерофункциональное соединение,
п-аминофенол образует производные по
каждой функциональной группе в отдельности
и одновременно по двум функциональным
группам. п-Аминофенол ядовит. Интерес
для медицины представляют его производные
— парацетамол, фенацетин, оказывающие
анальгетическое (обезболивающее) и
жаропонижающее действие.
ак
гетерофункциональное соединение,
п-аминофенол образует производные по
каждой функциональной группе в отдельности
и одновременно по двум функциональным
группам. п-Аминофенол ядовит. Интерес
для медицины представляют его производные
— парацетамол, фенацетин, оказывающие
анальгетическое (обезболивающее) и
жаропонижающее действие.
п-Аминобензойная кислота (ПАБК) и ее производные.
Эфиры ароматических аминокислот обладают общим свойством — способностью в той или иной степени вызывать местную анестезию, т.е. потерю чувствительности. Особенно заметно это свойство выражено у пара-производных. В медицине используют анестезин (этиловый эфир ПАБК) и новокаин (-диэтиламиноэтиловый эфир ПАБК). Новокаин применяют в виде соли (гидрохлорида), что связано с необходимостью повышения его растворимости в воде.
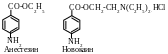
п-Аминобензойная кислота является фактором роста микроорганизмов и участвует в синтезе фолиевой кислоты (витамин В), при недостатке или отсутствии которой микроорганизмы погибают.
Сульфаниловая кислота (п-аминобензолсульфокислота) легко получается при сульфировании анилина, существует в виде диполярного иона. Амид сульфаниловой кислоты (сульфаниламид), известный под названием стрептоцид, является родоначальником группы лекарственных средств, обладающих антибактериальной активностью и называемых сульфаниламидами (сульфамидами). Их антибактериальное действие основано на том, что они являются антиметаболитами по отношению к п-аминобензойной кислоте, участвующей в биосинтезе фолиевой кислоты в микроорганизмах. Амид сульфаниловой кислоты имеет структурное сходство с п-аминобензойной кислотой и может мешать биосинтезу фолиевой кислоты, что ведет к гибели бактерий. Избирательность бактериального действия сульфаниламидов основана на том, что фолиевая кислота в человеческом организме не синтезируется. Таким образом, сульфаниламиды блокируют метаболические реакции, существенные для определенных бактерий (пневмококки, стрептококки и др.), и в то же время не влияют на организм человека.
Салициловая кислота относится к группе гидроксибензойных кислот. Как о-гидроксибензойная кислота она легко декарбоксилируется при нагревании с образованием фенола.
Салициловая кислота растворима в воде, дает интенсивное окрашивание с хлоридом железа(III) (качественное обнаружение фенольной гидроксильной группы). Она оказывает анти-спазматическое, жаропонижающее и антигрибковое действие, но как сильная кислота (рКа 2,98) вызывает раздражение пищеварительного тракта и поэтому применяется только наружно. Внутрь применяют ее производные – соли или эфиры. Салициловая кислота способна образовывать производные по любой функциональной группе. Практическое значение имеют салицилат натрия, сложные эфиры по СООН-группе (метилсалицилат, фенилсалицилат (салол)) и ОН-группе – ацетилсалициловая кислота (аспирин). Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике, поэтому используется также в качестве материала для защитных оболочек некоторых лекарственных средств, которые не стабильны в кислой среде желудка.
Салициловая кислота впервые была получена путем окисления салицилового альдегида, содержащегося в растении таволге (род Spireae). Отсюда и ее первоначальное название — спировая кислота, с которым связано название аспирин (начальная буква «а» обозначает ацетил). Ацетилсалициловая кислота в природе не найдена.
Из других производных салициловой кислоты большое значение имеет п- аминосалициловая кислота (ПАСК) как противотуберкулезное средство. ПАСК является антагонистом п-аминобензойной кислоты, необходимой для нормальной жизнедеятельности микроорганизмов. Другие изомеры таким действием не обладают. м-Аминосалициловая кислота является высокотоксичным веществом.
Типовые задачи и их решение
Задача ХVI. В качестве противовоспалительных средств используются ацетилсалициловая кислота и салициламид. При участии каких групп салициловой кислоты образуются эти производные?
Р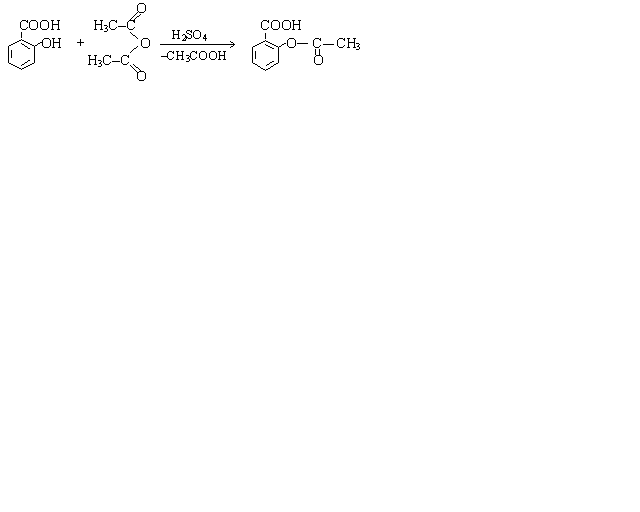 ешение.
Салициловая кислота – гетерофункциональное
соединение, содержащее карбоксильную
и гидроксильную группы. Ацетилсалициловая
кислота (аспирин) — сложный эфир,
образованный уксусной кислотой и
фенольной гидроксигруппой салициловой
кислоты. Синтезировать аспирин можно
при взаимодействии салициловой кислоты
и ангидрида уксусной кислоты в присутствии
кислотного катализатора (например,
H2SO4).
ешение.
Салициловая кислота – гетерофункциональное
соединение, содержащее карбоксильную
и гидроксильную группы. Ацетилсалициловая
кислота (аспирин) — сложный эфир,
образованный уксусной кислотой и
фенольной гидроксигруппой салициловой
кислоты. Синтезировать аспирин можно
при взаимодействии салициловой кислоты
и ангидрида уксусной кислоты в присутствии
кислотного катализатора (например,
H2SO4).
салициловая кислота уксусный ангидрид ацетилсалициловая кислота (аспирин)
Салициламид (амид салициловой кислоты) можно получить путем взаимодействия карбоксильной группы салициловой кислоты с аммиаком. Сначала образуется аммониевая соль салициловой кислоты. Это связано с легкостью образования аммониевого иона NH4+. Перенос протона от кислоты к аммиаку (сильному основанию) осуществляется быстрее, чем нуклеофильная атака атома углерода карбоксильной группы молекулой аммиака (нуклеофилом). При нагревании аммониевой соли выделяется молекула воды и образуется амид салициловой кислоты.
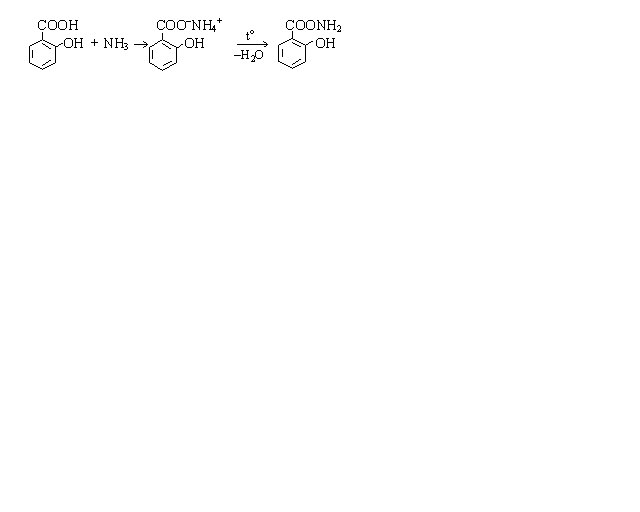
салициловая кислота аммониевая соль салициловой кислоты салициламид
Задачи для самостоятельного решения:
3.1. В состав кетонных тел входит ацетондикарбоновая кислота: HОOC–CH2–СО–CH2–COOH. Находится ли карбонильная группа в сопряжении с карбоксильной группой? Напишите уравнение реакции этой кислоты с гидроксиламином и этанолом (в присутствии кислоты).
3.2. Какое из соединений: 2-гидрокси-5-метилгексаналь или 5- гидрокси-2-метилгексаналь — сосуществует в кислой среде со своей циклической формой? Напишите схему реакции.
3.3. Важное значение для медицины имеют производные 2- пирролидона – лактама ГАМК (-аминомасляной кислоты). Приведите схему образования этого циклического соединения.
3.4. Какое количество вещества (моль) этанола необходимо ввести в реакцию, чтобы получить полный этиловый эфир лимонной кислоты? Приведите соответствующее уравнение реакции.
3.5. Бензиловый эфир бензойной кислоты (бензилбензоат) С6Н5СООСН2С6Н5 — противочесоточное средство. Какие продукты образуются в результате реакции гидролиза этого сложного эфира в щелочной среде? Напишите уравнение реакции.
