
- •Курсовая работа
- •Пояснительная записка
- •Аннотация
- •Содержание
- •Введение
- •1. Литературный обзор
- •1.1. Производство ацетона брожением крахмала
- •1.2. Производство ацетона из изопропилового спирта
- •1.3. Неполное окисление изопропилового спирта в паровой фазе
- •1.4. Неполное окисление изопропилового спирта в жидкой фазе
- •1.5. Окисление вторичных спиртов в кетоны
- •1.6. Другие методы получения ацетона
- •2. Общая часть
- •2.1. Физические свойства
- •2.2. Химические свойства
- •2.3. Технические характеристики ацетона
- •2.4. Производство ацетона в промышленности
- •2.5. Применение
- •2.6. Лабораторное применение
- •2.7. Токсичность
- •3. Экспериментальная часть
- •3.1. Идентификации ацетона
- •3.2. Анализ результатов
- •Список использованной литературы
3. Экспериментальная часть
В результате анализа литературного материала было решено синтезировать ацетон согласно методу, представленному в литературе.
Окисление вторичных спиртов в кетоны.

Ацетон получают из изопропилового спирта по реакции:
3CH3 - CHOH - CH3 + K2Cr2O2 + 4H2SO4 → 3CH3 - CO-
CH3 + Cr2(SO4)3 + K2SO4 + 7H2O
Оборудование:
водяная баня
термометр
химические весы
обратный холодильник
колба круглодонная 200 мл
двурогий форштосс
капельная воронка 100 мл
мерный цилиндр 100 мл
мерный цилиндр 50 мл
химический стакан 100 мл
колба Вюрца 200 мл
колба коническая 50 мл
аллонж
Реактивы:
изопропиловый спирт 20 мл
дихромат калия 22,8 г
серная кислота (d= 1,84 г/см3)
Ход работы:
1) Включили водяную баню.
2) Мерным цилиндром отмерили 20 мл изопропилового спирта, поместили его в круглодонную колбу ёмкостью 200 мл. Затем в колбу вставляют двурогий форштосс, соединенный с обратным холодильником и капельной воронкой.
3) На весах взвесили 22,8 г дихромата калия и растворили его в небольшом стакане в 60 мл воды, воду предварительно нагрели, так как дихромат калия плохорастворим в холодной.
4) Мерным цилиндром отмерили 20 мл концентрированной серной кислоты. Осторожно, при перемешивании, прилили кислоту к дихромату.
5) Небольшую часть полученного раствора хромовой смеси поместили в капельную воронку, оставшуюся часть поместили на водяную баню, в целях избежания кристаллизации дихромата при остывании и осторожно, небольшими (по 1-2 мл), прибавили в колбу, постепенно приливая в воронку горячий раствор дихромата калия (установка на рис.2).
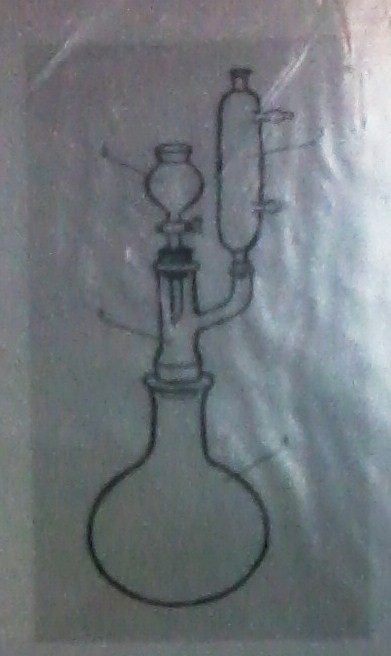
Рис. 2. Установка для получения ацетона при окислении вторичных спиртов в кетоны.
1 – колба круглодонная; 2 – двурогий форштосс; 3 – капельная воронка; 4 – обратный холодильник;
Сразу начинается реакция окисления, сопровождающаяся выделением теплоты и сильным разогревом реакционной смеси. Последующие порции хромовой смеси приливали постепенно, при постоянном перемешивании и охлаждении колбы в холодной воде.
6) Когда хромовая смесь будет прибавлена, колбу нагревают на кипящей водяной бане в течение 10 мин.
7) Затем реакционную смесь в колбе охладили до комнатной температуры.
8) перелили смесь в колбу Вюрца с нисходящим холодильником (установка на рис.3).

Рис. 3. Установка для получения ацетона при окислении вторичных спиртов в кетоны:
1 – колба круглодонная; 2 – термометр; 3 –обратный холодильник; 4 – аллонж; 5 - колба коническая;
9) Отогнали ацетон на водяной бане в предварительно отведенную колбочку, собирая фракцию, кипящую при 55 - 58ºС.
10) В результате эксперимента получили 8,2 г ацетона, методический выход около 10 г.
11) Рассчитаем теоретический выход:
3CH3 - CHOH - CH3 + K2Cr2O2 + 4H2SO4→ 3CH3 - CO-
CH3 + Cr2(SO4)3 + K2SO4 + 7H2O.
Плотность изопропилового спирта 0, 7851 г/мл, Vсп= 20 мл, Mсп= 60 г/моль:
mсп= p*V= 0, 7851*20= 15, 702 г.
υсп= m = 15, 702= 0,2617 моль
υац= υсп= 0, 2617 моль, Мсп= 58 г/моль
mсп= Мац*υсп= 58*0, 2167= 15, 178 г
Теоретический выход составляет 15, 178 г.
Полученный выход ацетона составляет 54% от теоретического выхода.
