
- •1. Классификация полупроводниковых материалов.
- •1. Явления поляризации в диэлектриках. Виды поляризации. Диэлектрическая проницаемость и диэлектрические потери.
- •4. Стеклообразные диэлектрики, их свойства и применение.
- •5. Неполярные, полярные и термостойкие органические диэлектрики.
- •6. Конструкционные металлические сплавы на основе Fe, Al, Cu
- •7. Композиционные листовые пластмассы. Материалы для оснований печатных плат вч и свч диапазонов.
- •2.5. Композиционные, наполненные пластмассы
- •2.5.2. Наполнители
- •2.5.3. Пластмассы с листовым наполнителем
- •2.5.4. Листовые материалы для производства печатных плат
- •8. Сегнетоэлектрики
- •12. Керамика, особенности структуры и основные характеристики установочной и конденсаторной керамики.
- •2. Керамика
- •3.3.2. Конденсаторная керамика
- •14. Зонная структура металла, концентрация и подвижность носителей заряда в металле.
- •15. Эпитаксиальный рост пленок полупроводника.
- •16 Анализ p–n перехода, физика работы диода.
- •18. Ионная имплантация примесей в полупроводник.
- •22. Ионно-плазменное осаждение тонких пленок.
- •27.Усилительные каскады на биполярных и полевых транзисторах.
- •1.2 Эквивалентные схемы резисторного каскада на различных частотах
- •31 Ескд. Виды и комплектность конструкторской документации.
- •33. Конструктивные, технологические и эксплуатационные требования к эс
- •34. Стадии и этапы проектирования электронных средств и разработки технической документации.
- •35. Особенности проектирования эс
- •39. Унифицированные базовые конструкции и их влияние на качество и себестоимость.
- •IV. Унификация.
- •41. Защита рэс от атмосферных воздействий.
- •42. Защитные покрытия, их классификация и основные характеристики. Виды и материалы покрытий.
- •44. Обеспечение надежности рэс в процессе проектирования и производства рэс.
- •45. Статистический ряд и его обработка при управлении качеством
- •46. Международные стандарты по управлению качеством.
- •47. Математическая модель биполярного транзистора, ее основные элементы
- •50. Структура и состав сапр. Состав и возможности современных пакетов проектирования рэс.
- •54. Топологическое проектирование рэс (компоновка, размещение, трассировка), как задачи структурной оптимизации.
- •57. Амплитудная модуляция
- •58. Обобщенная трехточечная схема автогенератора
- •58. Транзисторные автогенераторы
- •1.5 Кварцевые автогенераторы
- •61. Физическая сущность процесса детектирования амплитудно-модулированных сигналов
- •В этом случае ток, протекающий через диод будет иметь им-
- •1.4 Схемы диодных детекторов Различают последовательную (рис. 2.5) и параллельную (рис. 2.6) схемы построения диодных детекторов.
- •1.5 Нелинейные искажения в детекторе больших амплитуд
- •1.6 Линейное детектирование в амплитудных детекторах
- •Тогда ток, протекающий в цепи диода, равен
- •Определим среднее значение тока в цепи диода
- •Пусть на вход детектора подан ам- сигнал
- •Определим коэффициент детектирования
- •С учетом выражений (2.6) и (2.4) запишем
- •64. Принцип факсимильной передачи сообщений.
- •65. Типизация технологических процессов. Типовые и групповые технологические процессы.
- •69.Типы и свойства нефольгированных и фольгированных диэлектриков, используемых для изготовления печатных плат.
- •70. Методы изготовления пп по субтрактивной технологии.
- •71. Методы изготовления пп по аддитивной технологии
- •74. Методы изготовления мпп
- •4.3.1.1. Метод металлизации сквозных отверстий
- •4.3.1.2. Метод открытых контактных площадок
- •4.3.1.3. Мпп с выступающими выводами
- •4.3.1.4. Метод попарного прессования
- •4.3.1.5. Метод послойного наращивания
- •4.3.2. Мпп прецизионные на фолыированном основании
- •4.3.4. Мпп прецизионные на нефольгированном основании
- •4.3.5. Мпп изготовленные методом пафос
- •75. Металлизация диэлектриков
- •77. Схемы технологических процессов
- •80. Методы и технология монтажной пайки.
- •81. Пайка одиночной и двойной волной припоя.
- •82. Конвекционная пайка. Температурный профиль пайки. Инфракрасная пайка.
- •83. Производственные погрешности, причины возникновения и законы распределения.
- •84. Задачи технологической подготовки рэс. Стандарты единой системы технологической подготовки производства и их классификация
- •Прогрессивных технологических процессов (тп),
- •Основные функции тпп. Задачи тпп, решаемые на стадиях проектирования
- •88. Изготовление деталей из керамических материалов.
- •Дополнительные операции.
- •89. Теплопроводность (кондуктивный перенос тепла)
- •3.1. Закон Фурье
- •3.2. Тепловые коэффициенты. Тепловые сопротивления. Метод электротепловых аналогий
- •3.3. Теплопередача цилиндрической, однородной стенки (трубы)
- •91. Конвективный теплообмен. Закон Ньютона-Рихмана.
- •92. Теплообмен излучением. Перенос тепла излучением.
- •Закон Ламберта -Этот закон определяет значение плотности потока излучения е в зависимости от его направления по отношению к равномерно излучающей поверхности тела.
- •93. Влагообмен в рэс Первый и второй закон Фика.
- •97. Классификация систем охлаждения рэа
- •11.2.1. Контактный способ охлаждения
- •11.2.2. Естественное воздушное охлаждение
- •11.2.3. Принудительное воздушное охлаждение
- •11.2.4. Жидкостные системы
6. Конструкционные металлические сплавы на основе Fe, Al, Cu
Fе-C
Диаграмма состояния сплава железо-углерод отображает фазовый состав и структуру сплава в зависимости от температуры и от соотношения компонентов Fe и C.
Чистое железо металла серебристого цвета с температурой плавления 1539 °С, плотностью 7,86 г/м3. Оно известно в двух полиморфных модификациях и : -железо с ОЦК решеткой существует в двух температурных интервалах - от 1392 до 1539 °С (иногда эту ОЦК модификацию обозначают - железом) и при температуре ниже 911 °С. До температуры 768 °С - железо - ферромагнитно, а при температуре 768 °С, которую называют точкой Кюри, происходит магнитное превращение, т.е. железо переходит из ферромагнитного состояния в парамагнитное. - железо существует при температурах 911-1392 °С; оно парамагнитно. Кристаллическая решетка - железа - гранецентрированная кубическая решетка (ГЦК). Железо обладает большим сродством к кислороду, углероду, азоту, сере, фосфору и другим элементам. С металлами железо образует твердые растворы замещения, с углеродом, азотом, водородом - твердые растворы внедрения.
Углерод является неметаллическим элементом. Температура плавления 3500 °С. Углерод полиморфен. В обычных условиях он находится в виде модификации графита, но может существовать и в виде мета стабильной модификации алмаза.
Растворимость углерода в и модификациях железа различна: в -железе его растворяется не более 0,023 %, в -железе значительно больше (до 2,14 %). Сплав железа с углеродом образует твердые растворы, химические соединения и механические смеси. Максимальная растворимость углерода в железе, когда образуются твердые растворы, составляет 2,14 %(сталь), а при содержании выше 2,14 % С (чугун). При затвердевании чугун имеет в своей структуре хрупкую эвтектику, плохо обрабатываемую давлением, но обладающую хорошими литейными свойствами. Рассматривать те сплавы, в которых содержание углерода менее 2,14 %.
В сплаве Fe – C существуют твердые растворы – феррит, аустенит и химическое соединение - цементит Fe3C.
Феррит (от латинского слова Ferrum - железо) - твердый раствор внедрения С в -железе. Различают высокотемпературный -феррит с предельной растворимостью углерода 0,1 % и низкотемпературный -феррит с растворимостью углерода 0,02 %. Прочность (в = 250 МПа) и твердость (НВ =80 - 90), 0,2 =120 МПа, высокую пластичность (=40 %), магнитен, тепло- и электропроводен. На диаграмме состояния Fe – C (рис. 1.1) область чистого высоко- и низкотемпературного феррита ограничена линиями AHN и GPQ соответственно.
Аустенит - твердый раствор внедрения С в -железо. Обозначается аустенит A или Fe (С). Предельная растворимость углерода в аустените 2,14 %. Аустенит - немагнитен, имеет большую твердость и прочность, чем феррит, обладает пониженной упругостью и хорошей вязкостью. На диаграмме состояния Fe - C аустенит ограничен линией NJESG.
Цементит - это химическое соединение - карбид железа Fe3C. Имеет очень сложную ромбоэдрическую кристаллическую решетку с плотной упаковкой атомов. Температура плавления около 1250 °С. Аллотропических превращений не испытывает, но при низких температурах слабо ферромагнитен. Магнитные свойства цементит теряет при 217 °С. К характерным особенностям цементита относятся очень высокая твердость (>800 НВ) и чрезвычайно низкая, практически нулевая, пластичность, что обусловлено, вероятно, сложностью строения кристаллической решетки.
Цементит является неустойчивым соединением и может распадаться на железо и углерод в виде графита. Состав цементита - 75 % (атомн.) Fe и 25 % (атомн.) С или 6,67 % (по массе) С - остальное железо.

При 1147 °С (линия ЕСF) протекает эвтектическая реакция ЖеАе+Ц, в результате которой образуется эвтектическая смесь из аустенита и цементита, называемая ледебуритом. Реакция протекает у всех сплавов, систем, содержащих углерода более 2,14 %.
При 727 °С (горизонталь РSK) протекает эвтектоидная реакция АsФр + Ц, в результате которой образуется эвтектоидная смесь из феррита и цементита, которая называется перлитом.
Укажем на характерные точки на диаграмме сплава Fe - С. Точка А (1539 °С) на диаграмме соответствует температуре плавления чистого железа, а точка Д (1250 °С) - температуре плавления цементита Fe3c. Точки N (1392 °С) и G (911 °С) соответствуют полиморфному превращению -железа в -железо. Точка Е (1147 °С) характеризует предельную растворимость углерода в - железе (2,14 % С).
Процесс кристаллизации сплавов начинается по достижении температур, соответствующих линии АВСД (линия ликвидус), а конец затвердевания - температурам соответствующих линии AHJE (линия солидус).
Сплавы, содержащие не более 0,02 % С называют техническим железом. Сплавы, содержащие углерод до 0,8 %, называют доэвтектоидными сталями. Сплав с содержанием 0,8 % С называется эвтектоидной сталью. Сплавы, содержащие углерод от 0,8 % до 2,14 %, называются заэвтектоидными сталями.
C увеличением содержания углерода в стали снижается плотность, растут удельное электрическое сопротивление и коэрцитивная сила, понижаются теплопроводность, остаточная индукция и магнитная проницаемость.
Лучше всего обрабатываются резанием стали с содержанием углерода 0,3 0,4 %.
С увеличением углерода снижается технологическая пластичность - способность деформироваться в холодном состоянии. Обычно способность стали к штампуемости оценивается отношением о, 2/в. Для сталей глубокой вытяжки это отношение должно находиться в пределах 0,65 0,7. Такими свойствами обладают стали с содержанием 0,08 0,1 % С (до 0,4 % Мn и не более 0,03 % Si).
Хорошо свариваются стали с содержанием углерода до 0,3 %. Стали с большим содержанием С требуют применения специального подогрева и замедленного охлаждения.
Сера является вредной примесью в стали. С железом она образует химическое соединение FeS, которое практически нерастворимо в Fe в твердом состоянии, но растворимо в жидком металле. Соединение FeS образует с железом легкоплавкую эвтектику (температура плавления 988 °С), которая образуется при очень малом содержании серы. Поэтому содержание серы в стали в зависимости от качества не должно превышать 0,035 + 0,06 %.
Фосфор может растворяться в и - железе и при высоком содержании (более 1,0 %) образует фосфид железа Fe3P. Растворяясь в феррите, фосфор искажает кристаллическую решетку, увеличивая предел прочности на растяжение и предел текучести, но сильно снижает пластичность и вязкость. Каждые 0,01 % Р повышают порог хладоломкости примерно на 25 °С. Фосфор, как и сера, является вредной примесью для большинства сталей и содержание Р не должно превышать в сталях 0,025 0,08 %. Однако допускается содержание S и Р до 0,1 0,2 % в сталях, обрабатываемых на токарных станках-автоматах.
Все химические элементы, содержащиеся в стали, разделяют на 4 вида:
постоянные, примеси Mn, Al, Si применяемые в качестве раскислителей при производстве стали, а также сера и фосфор, полностью освободиться от которых при массовом производстве невозможно;
скрытые примеси (0, N, Н), присутствующие в любой стали в очень малых количествах;
случайные примеси, попадающие в сталь из шихты (Cu, As и др.), содержание и вид этих примесей зависит от вида руды, из которой выплавляют сталь;
легирующие элементы, специально вводимые в сталь в определенных концентрациях с целью изменения ее строения и свойств.
В зависимости от химического состава конструкционные стали общего назначения разделяются на углеродистые и легированные. К углеродистым сталям относятся сплавы системы Fe - C, у которых содержание постоянных (Mn, Si, P, S) и случайных примесей (Cr, Ni, Cu) незначительно, а легирующие элементы отсутствуют. Легированными сталями называют такие, в которые вводятся легирующие компоненты Cr, Mo, W, Ni, Mn, V, Ti и др.
По содержанию легирующих элементов легированные стали подразделяются на низколегированные (содержание легирующих элементов 5 %), среднелегированные (5 10 %), высоколегированные (блее 10 % ).
Износостойкость, коррозионная стойкость, выносливость (усталостная прочность), жаропрочность характеризуют долговечность.
Al
Аюминий и его сплавы занимают одно из ведущих мест среди конструкционных материалов, применяемых для изготовления деталей РЭС.
Алюминий - элемент III группы периодической системы элементов, порядковый номер 13, атомная масса 26,98, температура плавления технического алюминия 657 °С, высокой чистоты 680 °С. Алюминий имеет ГЦК - решетку с периодом а=4,0412 Нм. Плотность алюминия 2,7 т/м3, удельное электрическое сопротивление 2,610-8 Омм, коэффициент линейного расширения в диапазоне 20 100 °С, 23,9 10-6 °С-1, модуль упругости 71000 МПа. Алюминий не имеет полиморфных превращений, обладает большим сродством к кислороду, в результате чего на воздухе покрывается тонкой пленкой окиси алюминия. Беспористая плотная пленка защищает поверхность алюминия от дальнейшего окисления. Алюминий растворяется в щелочах, в соляной и серной кислотах; органические и азотная кислоты на него не действуют.
На рис представлена левая часть диаграммы состояния Al - Cu, на основе которой формируется большинство конструкционных деформируемых сплавов.
Температура плавления алюминия 657 °С, меди 1083 °С. Эвтектический сплав содержит 33 % Cu и имеет температуру плавления 548 °С. Область однофазного твердого раствора А1-Си ограничена линиями АВD. Из диаграммы следует, что растворимость меди в алюминии при нормальной температуре составляет около 0,5 %, а с повышением температуры до эвтектической - 5,7 %. Сплавы с содержанием меди 0,5-5,7 % можно перевести в однофазную структуру -твердого раствора путем нагрева выше линии ВD, выдержки при этой температуре и быстром охлаждении до комнатной температуры, т.е. закалить. После закалки сплавы имеют сравнительно невысокую прочность (в, 0,2) и высокую пластичность (, ).
Процесс распада твердого раствора проходит в течение 4-5 суток, который называется старением. После старения предел прочности значительно возрастает и достигает 400 МПа. После закалки в первые часы скорость упрочнения значительно меньше, чем в последующие. Начальный период старения после закалки называется инкубационным и имеет важное технологическое значение, так как сплав обладает большой способностью к пластической деформации. Закаленные образцы можно подвергать разнообразным технологическим операциям, связанным с деформацией (гибке, отбортовке и т.д.) Через 23 часа способность к пластической деформации начинает резко уменьшаться и эти операции становятся неосуществимыми.
Рассмотрим процессы, протекающие в сплаве Al - Cu при старении. При естественном (при 20 °С) или низкотемпературном искусственном старении (ниже 100-150 °С) после закалки не наблюдается распада твердого раствора с выделением избыточной фазы; при этих температурах атомы меди перемещаются только внутри кристаллической решетки -твердого раствора на весьма малые расстояния и собираются по плоскостям (100) в двумерные пластинчатые образования или диски, так называемые зоны Гинье -Престона (ГП-1). Зоны ГП-1 имеют протяженность 30-60 А и толщиной 510 А. Содержание меди в зонах повышенное, но еще не отвечает формуле CuAl2. Естественно, такое состояние сплава является неустойчивым.
Н аиболее
распространенным представителем
деформируемых алюминиевых сплавов,
упрочняемых термической обработкой
является дюралюминий - сплав, шести
компонентов: алюминия, меди, магния,
марганца, кремния и железа, хотя основными
добавками являются медь (3,4 - 4,0 %),
магний (0,5-1,0 %) и марганец (0,5-1,0 %). Кремний
и железо являются постоянными примесями,
попадающими в сплав вследствие применения
недостаточно чистого алюминия.
аиболее
распространенным представителем
деформируемых алюминиевых сплавов,
упрочняемых термической обработкой
является дюралюминий - сплав, шести
компонентов: алюминия, меди, магния,
марганца, кремния и железа, хотя основными
добавками являются медь (3,4 - 4,0 %),
магний (0,5-1,0 %) и марганец (0,5-1,0 %). Кремний
и железо являются постоянными примесями,
попадающими в сплав вследствие применения
недостаточно чистого алюминия.
Основу литейных алюминиевых сплавов, применяемых для производства деталей РЭС, являются сплавы Al - Si, называемые силуминами.
Линия АЕС - ликвидус. Линия АВЕД - солидус. Точка А (657 °С) соответствует температуре плавления алюминия. Эвтектический сплав (11,7 % Si) имеет температуру плавления 577 °С. Кремний не образует с алюминием химических соединений и почти не растворяется в нем при нормальной температуре. Растворимость кремния в алюминии (образование - фазы) при 300 °С лишь 0,99 %, а при эвтектической температуре достигает 1,65 %.
Сплавы АЛ2, АЛ4, АЛ9 имеют высокие литейные свойства и обладают герметичностью изготовленных из них отливок. Сплав АЛ2 не упрочняется термической обработкой; единственным способом повышения механических свойств является модифицирование натрием путем присадки к расплаву солей NaF или NaCl. В этом случае в структуре сплава вместо избыточного кремния появляются кристаллы - раствора. Эвтектика приобретает более тонкое строение и состоит из нескольких кристаллов (Si) и - твердого раствора. Такая структура улучшает механические свойства.
Сплав АЛ2 рекомендуется применять для изготовления деталей РЭС небольших размеров и более простой формы. Это обусловлено тем, что в крупногабаритных деталях возможно появление концентрированных усадочных раковин, характерных для сплавов с малым интервалом кристаллизации.
Сплав АЛ4 применяют для изготовления средних и крупных деталей (корпусов). При этом средненагруженные детали из сплава АЛ4 подвергают только искусственному старению при Т=175 °С, а крупные нагруженные детали (корпуса) - закалке и искусственному старению.
Сплав АЛ9 применяют для изготовления средних и крупных деталей ответственного назначения (корпусов механизмов, рам несущих конструкций, стоек, литых лицевых панелей, объемных конструкций шасси и др.). Для повышения пластичности отливки подвергают закалке при температуре 535 ± 5 °С, а для повышения прочности - закалке и старению при температуре 200 °С.
Сu
Медь - химический элемент I группы периодической системы элементов; порядковый номер 29, атомная масса 63,5. Это - металл красного, а в изломе розового цвета, кристаллизуется в кубической гранецентрированной решетке с периодом а = 3,607 А, плотность чистой меди 8,9 т/м3, температура плавления 1083 °С.
Медь обладает высокой электропроводностью, теплопроводностью и пластичностью. Удельное сопротивление чистой меди при 20 °С составляющей 1,7 10-8 Ом м. Удельная проводимость меди чувствительна к примесям. Так при добавлении 0,5 % примесей Zn, Ca, Ag удельное сопротивление меди повышается на 5 %. А при том же содержании Al, Ni, Sn удельное сопротивление увеличивается на 25-40 %. Примесь серы образует с медью хрупкое соединение CuS, входящее в состав эвтектики. На электропроводность эта примесь мало влияет, но улучшает обрабатываемость резанием.
Недостатком меди является ее подверженность атмосферной коррозии с образованием окисных и сульфидных пленок. Скорость окисления быстро возрастает при нагревании, при этом прочность оцепления окисной пленки с металлом невелика. Вследствие окисления медь непригодна для слаботочных контактов.
Латунь
Латунями называют двойные или многокомпонентные сплавы на основе меди, в которых основным легирующим элементом является цинк.
Диаграмма состояния сплава Cu - Zn состоит из пяти простых перитектических диаграмм. Так как практическое применение в РЭС имеет только сплавы с содержанием цинка примерно до 50 %, то мы будем рассматривать только часть диаграммы (рис.5). Существуют следующие фазы в сплавах Cu-Zn:
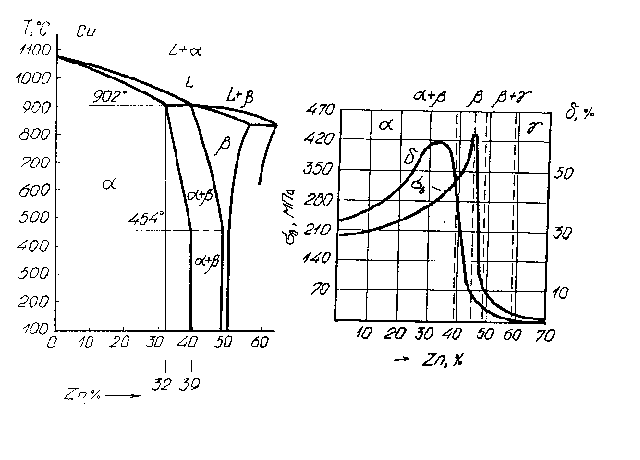 -твердый
раствор цинка в меди с кристаллической
решеткой ГЦК; растворимость цинка в
меди при комнатной температуре равна
39 %, она не изменяется практически до
454 °С и убывает до 32 %, при 902 °С.
-твердый
раствор цинка в меди с кристаллической
решеткой ГЦК; растворимость цинка в
меди при комнатной температуре равна
39 %, она не изменяется практически до
454 °С и убывает до 32 %, при 902 °С.
|
|
Прочность и пластичность сплавов зависят от количества цинка, находящегося в них, что иллюстрируется рис.5.2. Как видно из рисунка, наилучшей пластичностью обладают латуни с содержанием Zn около 3 %, а высокой механической прочностью обладают латуни с содержанием 42-45 % Zn, но пластичность при этом резко снижается. Переход через границу однофазной области (39 % Zn) резко снижает пластичность латуни.
Алюминий, никель, олово, кремний повышают прочность, коррозионную стойкость и улучшают антифрикционные характеристики. Железо, повышает температуру рекристаллизации и твердость латуни. Марганец повышает ее жаростойкость. Добавки свинца в латуни улучшают ее обработку резанием.
Двойные латуни маркируют буквой Л и числом, характеризующим среднее содержание меди в %. В многокомпонентных латунях после буквы Л, указывающей содержание меди, ставятся цифры, определяющие содержание легирующих элементов в %.
По технологическому признаку все латуни разделяют на деформируемые, из которых изготавливают листы, ленты, трубы, проволоку, прутки различного сечения и другие полуфабрикаты, и литейные латуни - для фасонного литья.
Латуни являются незаменимым материалом для изготовления деталей РЭС - наконечников, монтажных лепестков, контактов, экранов, осей, втулок, крепежных деталей, зубчатых колес и других деталей, изготавливаемых штамповкой, высадкой и со снятием стружки.
Латунь Л68 применяется для изготовления деталей холодной штамповкой и глубокой вытяжкой. Латунь Л63 используется для изготовления крепежных деталей.
Высокой коррозионной стойкостью в пресной или морской воде обладают латуни, легированные оловом, Л070-1, Л062-1, получившие название морских латуней.
Литейные латуни применяют для изготовления втулок, подшипников, гаек и других несущих деталей. Литейные латуни имеют лучшую коррозионную стойкость.
Бронзы
В недалеком прошлом бронзами называли сплавы Cu - Sn. В настоящее время к бронзам относят также сплавы меди с алюминием, кадмием, железом, бериллием, кремнием и другими элементами. Эти бронзы, не имея в своем составе дорогостоящего олова, по некоторым свойствам не уступают оловянистым, а иногда и превосходят их.
При 588 °С кристаллы - фазы претерпевают эвтектоидный распад с образованием и - фаз, а при 520 °С кристаллы твердого раствора у распадаются на фазы и .
Структура литых медно-оловянных сплавов значительно отклоняется от равновесного состояния, поэтому уже в сплавах, содержащих 5-6 % Sn и более, в литом состоянии обнаруживается -фаэа в виде эвтектоидной составляющей, что придает ей большую хрупкость. Отожженная бронза с содержанием до 14 % Sn должна состоять по структуре из однородного - раствора.
Линии ликвидус и солидус находятся на значительном расстоянии, т.е. между ними большой интервал температур, поэтому оловяниотые бронзы не обладают большой жидкотекучестью. Но высокие литейные свойства определяются исключительно малой усадкой - меньше 1 % (для сравнения усадка чугуна около 1,5%, латуни около 1,5 %, стали более 2 %), что позволяет получать из этих сплавов фасонные отливки.
П ри
содержании Sn до 5-6 % бронза обладает
хорошей пластичностью, но затем под
влиянием - фазы
пластичность резко падает. Понижение
прочности начинается при содержании
олова свыше 20 %. Оловянистые бронзы
слабо чувствительны к перегреву и
газам, свариваются и паяются, не дают
искры при ударах, немагнитны, морозостойки
и обладают хорошими антифрикционными
свойствами.
ри
содержании Sn до 5-6 % бронза обладает
хорошей пластичностью, но затем под
влиянием - фазы
пластичность резко падает. Понижение
прочности начинается при содержании
олова свыше 20 %. Оловянистые бронзы
слабо чувствительны к перегреву и
газам, свариваются и паяются, не дают
искры при ударах, немагнитны, морозостойки
и обладают хорошими антифрикционными
свойствами.
Для получения определенных свойств оловянистые бронзы легируются Zn, P, Fe, Ni, Pe и другими элементами. Цинк улучшает технологические свойства и удешевляет бронзу. Фосфор улучшает их механические, антифрикционные и литейные характеристики. Оптимальное содержание фосфора около 0,5 %. Железо повышает механические свойства, но ухудшает технологические характеристики и антикоррозионные свойства. Ni при содержании до 1 % повышает механические свойства и коррозионную стойкость. Свинец значительно повышает антифрикционные свойства и обрабатываемость резанием, но снижает механические свойства.
Бронзы маркируют начальными буквами Бр, затем следуют буквы, показывающие, какие легирующие элементы содержат бронзы, а потом цифрами указывают содержание этих элементов в процентах. Оловянистые бронзы разделяют на обрабатываемые давлением - до 6 % Sn и литейные - свыше 6 % Sn. В таблице 5.3 приведены механические свойства некоторых оловянистых и безоловянистых бронз, обрабатываемых давлением.
Алюминиевые бронзы по структуре являются твердыми растворами замещения с пределом растворимости Al 9,4 %. Двойные алюминиевые однофазные бронзы БрА5, БрА7 отличаются высокой прочностью и пластичностью. Алюминиевые бронзы морозостойки, не магнитны, не дают искры при ударах. По коррозионной стойкости они превосходят латуни и оловянистые бронзыДля улучшения прочностных характеристик бронзу подвергают старению при 250-300 °С в течение 2-3 ч после закалки при 950 °С.
Бериллиевые бронзы являясь дисперсионно-твердеющими сплавами, обладают высокими механическими, упругими, физическими и хорошими технологическими свойствами. Отличаются высокой коррозионной стойкостью, жаропрочностью, циклической прочностью; они устойчивы при низких температурах, не магнитны, не дают искры при ударах. Закалку бериллиевых бронз осуществляется при температуре 750 – 790 С. Бериллиевые бронзы БрБ2, БрБ2, 5 применяют для изготовления пружин, пружинящих деталей ответственного назначения
Бериллиевые бронзы обычно содержат никель и марганец. Кремниевые бронзы превосходят оловянистые бронзы по коррозионной стойкости, механическим, антифрикционным и упругим свойствам.
