
- •Общие методические указания
- •Химическая посуда и ее предназначение
- •Работа 1 определение молярной массы эквивалента металла методом вытеснения водорода
- •Основные теоретические положения
- •Математически закон эквивалентов для условной реакции вида
- •Порядок выполнения работы
- •Форма 1 Экспериментальные и расчетные данные
- •Давление насыщенного водяного пара при различных температурах
- •Контрольные задания Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 2 основные классы неорганических соединений
- •Основные теоретические положения
- •Оксиды – это соединения, состоящие из двух элементов, одним из которых является кислород. Образование названия оксида (его номенклатура) подчиняется следующим правилам:
- •Химические свойства кислот
- •Химические свойства солей
- •Перевод кислых (основных) солей в среднюю соль
- •Порядок выполнения работы
- •Получение и свойства гидроксидов
- •Получение и свойства кислот
- •Контрольные задания Вариант 1
- •Вариант 3
- •Вариант 4
- •Порядок выполнения работы
- •Часть 1. Определение изменения энтальпии растворения безводной соли
- •Изменение температуры калориметра для процесса растворения cоли (указать название соли)
- •Часть 2. Определение изменения энтальпии реакции нейтрализации сильной кислоты сильным основанием
- •Экспериментальные и расчетные данные для процесса нейтрализации
- •Часть 1. Определение изменения энтальпии растворения безводной соли
- •Форма 4 Экспериментальные и расчетные данные для процесса растворения соли (указать название соли)
- •Часть 2. Определение изменения энтальпии реакции нейтрализации сильной кислоты сильным основанием
- •Контрольные задания
- •Определение константы скорости и энергии активации реакции окисления йодоводородной кислоты пероксидом водорода
- •Основные теоретические положения
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Контрольные задания Вариант 1
- •Вариант 7
- •Титульный лист
- •Метрологическая карта средств измерения
- •Приложение 3 Интегральные энтальпии растворения солей в воде при 25 0с
- •Приложение 4
- •Изменение энтальпии нейтрализации 1 моль эквивалентов
- •Сильной кислоты сильным основанием при различных
- •Температурах
- •Библиографический список
- •Третьяков ю.Д. Практикум по неорганической химии: Учеб. Пособие. – м.: Академия, 2004.
- •Химия Лабораторный практикум
- •Часть 1
Форма 1 Экспериментальные и расчетные данные
№ опыта |
Масса навески металла m , г |
Уровень воды в бюретках V, см3 |
Объем выделившегося водорода VH2 , см3 |
Температура опыта Т, К |
Давление в лаборатории Р, кПа |
Давление водорода Р H2 , кПа |
Объем Н2 при н.у. V 0H2 , см3 |
Молярная эквивалентная масса металла МЭ , г/моль |
Относительная атомная масса Аr |
Относительная погрешность П, % |
|
Начальный V1 |
Конечный V2 |
||||||||||
1 2 |
|
|
|
|
|
|
|
|
|
|
|
Обработка экспериментальных данных
1. Объем водорода, который выделился по реакции
Ме + Н2SO4 = МеSO4 + Н2
при физических условиях, установившихся в лаборатории в день проведения эксперимента, определяют по формуле
![]() ,
см3.
(2)
,
см3.
(2)
2. Поскольку водород в эвдиометре собирают над водой, то по закону Дальтона измеренное при помощи барометра давление равно сумме давлений чистого водорода и насыщенного водяного пара:
![]() .
.
Тогда расчет парциального давления водорода следует вести по формуле
![]() ,
кПа. (3)
,
кПа. (3)
Значения
![]() при различных температурах приведены
в табл. 2.
при различных температурах приведены
в табл. 2.
3. Объем водорода
при н.у.
![]() определяют, используя выражение
объединенного газового закона:
определяют, используя выражение
объединенного газового закона:
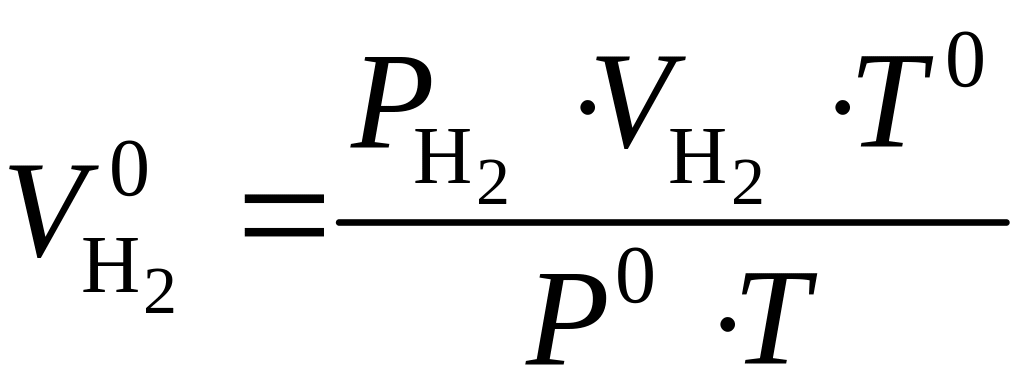 ,
см3,
(4)
,
см3,
(4)
где VН![]() –
объем
водорода, рассчитанный по формуле (2),
см3;
Т °
– температура при н.у., равная 273 К;
Р°
– парциальное давление водорода при
н.у., равное 101,325 кПа.; Т
– температура в лаборатории, К;
–
объем
водорода, рассчитанный по формуле (2),
см3;
Т °
– температура при н.у., равная 273 К;
Р°
– парциальное давление водорода при
н.у., равное 101,325 кПа.; Т
– температура в лаборатории, К;
![]() – парциальное
давление
водорода в лабораторных условиях,
рассчитанное по формуле (3), кПа.
– парциальное
давление
водорода в лабораторных условиях,
рассчитанное по формуле (3), кПа.
4.
Молярную массу эквивалента металла
![]() определяют, исходя из закона эквивалентов,
по уравнению
определяют, исходя из закона эквивалентов,
по уравнению
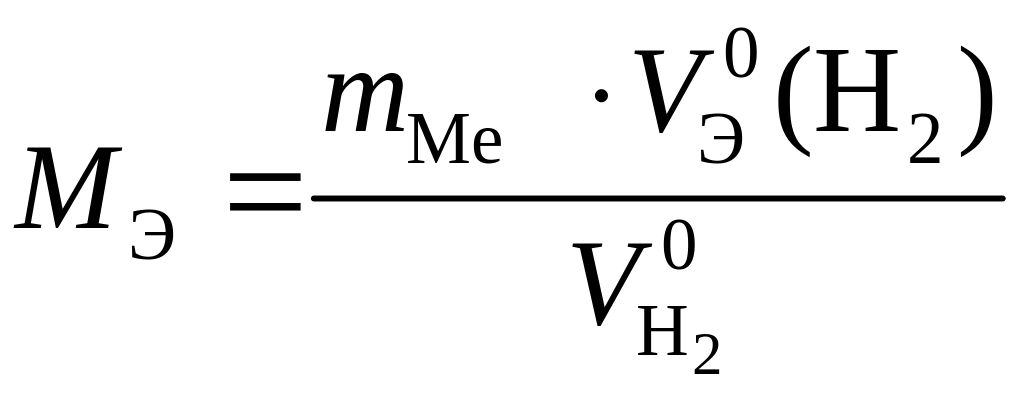 ,
г/моль,
,
г/моль,
где
mMe
– масса
навески
металла, г; V![]() – объем
водорода при н.у.,
рассчитанный по формуле (4), г/моль;
– объем
водорода при н.у.,
рассчитанный по формуле (4), г/моль;
![]() –
молярный
эквивалентный объем водорода, равный
11 200
мл/моль.
–
молярный
эквивалентный объем водорода, равный
11 200
мл/моль.
5. Относительную атомную массу исследуемого металла определяем по формуле
Аr = МЭ · В,
где В – валентность металла.
6. Находят среднее значение Аr параллельных опытов по формуле
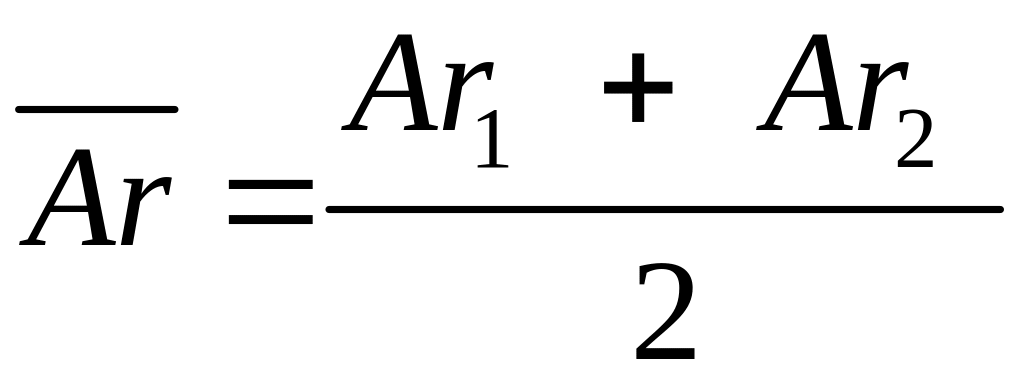 .
.
7. Идентифицируют металл по Периодической системе элементов Д.И. Менделеева и рассчитывают относительную погрешность определяемой величины по формуле (1):
П
=
 100 %.
100 %.
8. Заполняют таблицу формы 1, метрологическую карту средств измерения и формулируют выводы.
Таблица 2
Давление насыщенного водяного пара при различных температурах
Температура, 0С |
Давление пара, Па |
Температура, 0С |
Давление пара, Па |
Температура, 0С |
Давление пара, Па |
0 5 9 10 11 12 13 14 |
611 872 1148 1228 1312 1402 1497 1598 |
15 16 17 18 19 20 21 22 |
1705 1817 1937 2064 2197 2338 2406 2644 |
23 24 25 26 27 28 29 30 |
2810 2984 3168 3361 3538 3780 4005 4242 |
