- •Общие методические указания
- •Химическая посуда и ее предназначение
- •Работа 1 определение молярной массы эквивалента металла методом вытеснения водорода
- •Основные теоретические положения
- •Математически закон эквивалентов для условной реакции вида
- •Порядок выполнения работы
- •Форма 1 Экспериментальные и расчетные данные
- •Давление насыщенного водяного пара при различных температурах
- •Контрольные задания Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Вариант 6
- •Вариант 7
- •Вариант 8
- •Вариант 10
- •Вариант 11
- •Вариант 12
- •Вариант 13
- •Вариант 14
- •Вариант 15
- •Работа 2 основные классы неорганических соединений
- •Основные теоретические положения
- •Оксиды – это соединения, состоящие из двух элементов, одним из которых является кислород. Образование названия оксида (его номенклатура) подчиняется следующим правилам:
- •Химические свойства кислот
- •Химические свойства солей
- •Перевод кислых (основных) солей в среднюю соль
- •Порядок выполнения работы
- •Получение и свойства гидроксидов
- •Получение и свойства кислот
- •Контрольные задания Вариант 1
- •Вариант 3
- •Вариант 4
- •Порядок выполнения работы
- •Часть 1. Определение изменения энтальпии растворения безводной соли
- •Изменение температуры калориметра для процесса растворения cоли (указать название соли)
- •Часть 2. Определение изменения энтальпии реакции нейтрализации сильной кислоты сильным основанием
- •Экспериментальные и расчетные данные для процесса нейтрализации
- •Часть 1. Определение изменения энтальпии растворения безводной соли
- •Форма 4 Экспериментальные и расчетные данные для процесса растворения соли (указать название соли)
- •Часть 2. Определение изменения энтальпии реакции нейтрализации сильной кислоты сильным основанием
- •Контрольные задания
- •Определение константы скорости и энергии активации реакции окисления йодоводородной кислоты пероксидом водорода
- •Основные теоретические положения
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Контрольные задания Вариант 1
- •Вариант 7
- •Титульный лист
- •Метрологическая карта средств измерения
- •Приложение 3 Интегральные энтальпии растворения солей в воде при 25 0с
- •Приложение 4
- •Изменение энтальпии нейтрализации 1 моль эквивалентов
- •Сильной кислоты сильным основанием при различных
- •Температурах
- •Библиографический список
- •Третьяков ю.Д. Практикум по неорганической химии: Учеб. Пособие. – м.: Академия, 2004.
- •Химия Лабораторный практикум
- •Часть 1
гМИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ
ГОУ ВПО «ЧЕРЕПОВЕЦКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ»
Факультет общих математических
и естественнонаучных дисциплин

ХИМИЯ
Лабораторный практикум
Часть 1
Учебное пособие
Череповец
2010
Р
ББК 24 УДК 54 Х 46
Одобрено УМС ГОУ ВПО ЧГУ, протокол № 7 от 18.03.10 г.
Химия: Лабораторный практикум: Учеб. пособие. Ч. 1 / Котенко Г.А., Калько О.А. , Балицкий С.Н., Кузнецова Ю.С. и др. – Череповец: ГОУ ВПО ЧГУ, 2010. – 91 с. – ISBN 978 – 5 – 85341 – 386 – 3.
В учебном пособии представлены лабораторные работы по важнейшим разделам курса химии.
Пособие соответствует Государственному образовательному стандарту и учебным программам курсов общей и неорганической химии для студентов химических и нехимических специальностей вузов.
Рецензенты: В.А. Котенко, канд. техн. наук, доцент (ГОУ ВПО ЧГУ); Т.А. Окунева, канд. техн. наук, доцент (ГОУ ВПО ЧГУ)
Научный редактор: В.А. Котенко, канд. техн. наук, доцент
©
ISBN 978 – 5 – 85341 –
386 – 3
Введение
Лабораторный практикум предназначен для студентов специальностей, в учебных планах которых содержатся дисциплины «Химия», «Общая химия», «Общая и неорганическая химия», «Неорганическая химия». Он охватывает важнейшие разделы типовой программы указанных курсов. В часть 1 включены работы по следующим темам: «Основные законы химии», «Классы неорганических соединений», «Энергетика химических процессов», «Химическая кинетика».
Лабораторные работы включают в себя цель работы, основные теоретические положения, порядок выполнения работы и контрольные задания.
При выполнении лабораторных работ студенты знакомятся с измерительными приборами, с некоторыми методами исследования, а также с основными приемами обработки экспериментальных результатов.
Опыты выполняются студентами индивидуально: каждый получает задание и оформляет отчет по своим результатам, что формирует у обучаемых самостоятельность в решении поставленных задач.
Общие методические указания
Приступая к лабораторному практикуму, студент должен ознакомиться с инструкциями по охране труда в химической лаборатории (ИОТ 037-2008). Преподавателем проводится первичный инструктаж студентов согласно следующим положениям:
Строго запрещается принимать пищу в помещении лаборатории.
Запрещается пробовать на вкус химические вещества, пить из химической посуды.
Запрещается уносить реактивы общего пользования на свое рабочее место.
Запрещается использовать грязную посуду, а также посуду, имеющую трещины или отбитые края.
Запрещается оставлять без присмотра работающие установки, включенные электронагревательные приборы, спиртовки.
Все опыты следует проводить только на лабораторном столе.
Рабочее место необходимо содержать в чистоте и порядке.
Перед применением реактива внимательно прочитайте этикетку на склянке и убедитесь, что выбрали нужный реагент.
Пробки от склянок кладите на стол только внешней поверхностью.
Все реактивы добавляются только в необходимом объёме и в строго определенной последовательности согласно ходу работы.
Пролитую случайно на стол жидкость следует немедленно убрать.
При отборе жидкости при помощи пипетки используйте резиновую грушу.
Включение и выключение электроприборов производите, держась только за вилку.
При попадании химических веществ на открытые участки кожи промойте их струей воды из-под крана в течение 15 мин.
По окончании эксперимента использованную посуду моют водопроводной, а затем ополаскивают дистиллированной водой.
Использованные фильтры, спички, обертки и пр. выбрасывайте в мусорное ведро.
При проведении лабораторных работ используются различные приборы (эвдиометр, калориметр и т.д.), металлическое оборудование (держатели для пробирок, штативы и пр.), разнообразная химическая посуда (см. табл. 1).
Таблица 1
Химическая посуда и ее предназначение
Химическая посуда |
Предназначение |
1 |
2 |
Посуда общего назначения |
|
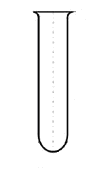
Пробирки
|
Для проведения химических реакций и нагрева веществ |
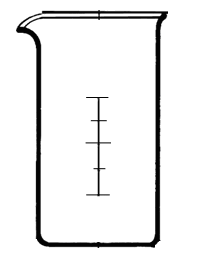
Стеклянные химические стаканы
|
|
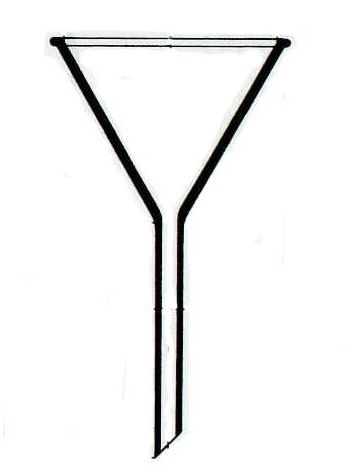
Воронки
|
Для аккуратного внесения веществ в сосуд и фильтрования |
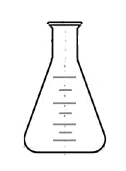
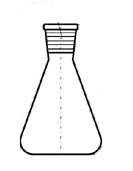
Конические колбы (колбы Эрленмейера)
|
Для проведения химических реакций и нагрева веществ |
Продолжение
1 |
2 |
Посуда специального назначения |
|
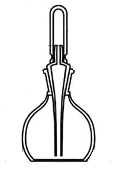
Капельницы
|
Для капельного дозирования веществ |
Мерная посуда (при измерении объемов глаз наблюдателя должен находиться на одной линии с нижним мениском жидкости – меткой) |
|
Мерные цилиндры
|
Для неточного измерения определенного объема жидкости |
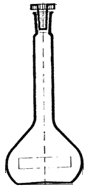
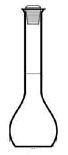
Мерные колбы
|
Для точного измерения определенного объема жидкости и приготовления растворов |
Окончание
1 |
2 |
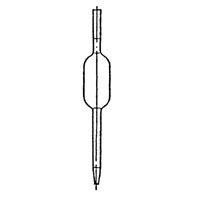
Пипетки Мора
|
Для точного отбора и переноса определенного объема жидкости |
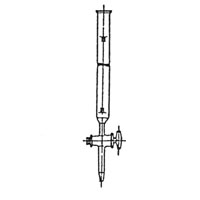
Бюретки
|
Для точного отбора и дозирования растворов |
Фарфоровая посуда |
|
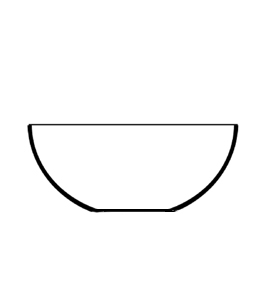
Фарфоровые чашки
|
Для нагрева и выпаривания веществ |
Требования к оформлению отчета
Лабораторная работа выполняется студентом индивидуально. По проведенным экспериментам оформляется отчёт, включающий в себя титульный лист (см. прил. 1). В отчете также должны присутствовать следующие основные разделы:
1. Цель работы.
2. Порядок выполнения работы (включает краткое описание хода работы, рисунок установки, химические реакции, протекающие в экспериментах).
3. Таблицы экспериментальных и расчетных данных (формы таблиц, как правило, приведены в описании работы).
4. Обработка результатов (записывают общий вид формул, после чего подставляют в них численные значения, указывают единицы измерения рассчитанных величин, определяют погрешности экспериментальных величин).
Относительную погрешность величины П следует рассчитывать по формуле (1):
П
=
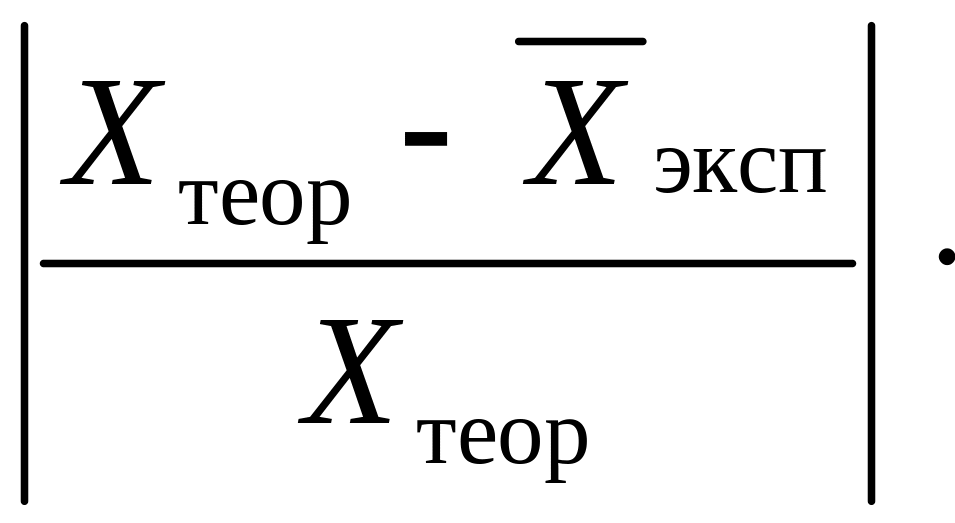 100 %, (1)
100 %, (1)
где
Хтеор
– теоретическое (истинное) значение
измеряемой величины;
![]() эксп
– среднее значение результатов опыта
измеряемой величины.
эксп
– среднее значение результатов опыта
измеряемой величины.
5. Метрологическая карта средств измерения (см. прил. 2). В карту заносят только те приборы, которыми были произведены измерения в данной лабораторной работе.
6. Выводы (на основании поставленной цели формулируют вывод с указанием найденных величин и обсуждением полученных результатов).
7. Список литературы (записывают не менее двух источников).
8. Ответы на контрольные вопросы (оформляются на отдельном листе, вариант задания указывается преподавателем).