
- •Учебно-практическое пособие Введение
- •Глава 1. Строение и основные свойства металлов
- •1.1.Кристаллическое строение твердых тел
- •1.2. Кристаллизация
- •1.3. Дефекты кристаллической решетки
- •1.3.1. Точечные дефекты
- •1.3.2. Линейные дефекты кристаллической решетки
- •1.3.3. Поверхностные дефекты
- •1.4. Методы изучения структуры металлов
- •Контрольные вопросы:
Учебно-практическое пособие Введение
Материаловедение является прикладной наукой о строении и свойствах технических материалов, основной задачей которой является установление связи между их составом, структурой и свойствами, а также их изменение при различных внешних воздействиях (тепловом, механическом, химическом и т.д.) В настоящее время в качестве современных технических материалов используются практически все элементы периодической системы Менделеева.
Современное машиностроение является основным потребителем производимых металлов (металлы и сплавы составляют 85 – 95% от массы машин). В станкостроении, судостроении, автомобильной промышленности из металлов изготовляют огромное число деталей машин и приборов.
Используемые в технике металлы принято подразделять на две основные группы – черные и цветные. К черным металлам относятся железо и его сплавы (чугун, сталь, ферросплавы). Остальные металлы и их сплавы составляют группу цветных.
В основу классификации черных металлов положен их химический состав. В общем случае черные металлы - это сложные системы, которые помимо железа и углерода содержат разнообразные примеси (серу, азот, фосфор, кремний и др.), вносимые в металл из исходного сырья в процессе производства, а также металлы, целенаправленно добавляемые с целью придания сплаву определенных свойств.
По содержанию углерода черные металлы делят на две основные группы: стали (менее 2,14% углерода) и чугуны (более 2,14% углерода). Это количественное различие связано с особенностями модификаций железа и структурой металла.
Наряду с черными металлами важное значение имеют в технике цветные металлы. Это объясняется рядом важных физико-химических свойств, которыми не обладают черные металлы. Наиболее широкое применение нашли в самолетостроении, радиотехнике, электронике и других отраслях промышленности такие материалы как медь, алюминий, магний, никель, титан, вольфрам, германий и другие.
Особое развитие за последние 50 лет получило производство синтетических материалов – пластмасс, которые наряду с другими неметаллическими материалами используют в конструкциях машин и механизмов взамен металлов и сплавов.
В последнее время особое распространение получили композиционные материалы. Это материалы, состоящие из двух компонентов и более, объединенных различными способами в монолит и сохраняющими при этом индивидуальные особенности.
Глава 1. Строение и основные свойства металлов
1.1.Кристаллическое строение твердых тел
Для описания атомно-кристаллической структуры материалов пользуются понятием пространственной или кристаллической решетки. Она представляет собой воображаемую пространственную сетку, в узлах которой расположены атомы (ионы) образующие кристалл. Т.е. атомы располагаются в определенном порядке, который периодически повторяется в 3-х измерениях и составляют пространственную решетку. Следует отметить, что атомы (частицы) твердого тела стремятся к такому расположению в пространстве, чтобы энергия их взаимодействия была минимальна.
В кристаллической решетке можно выделить элемент объема (рис.1.1.), состоящий из минимального количества частиц, многократным переносом (трансляцией) которого можно построить весь кристалл. Этот элементарный объем называется элементарной ячейкой. Имеется относительно небольшое количество типов кристаллических решеток.
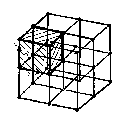
Рис.1.1. Элементарная ячейка
кристаллической решетки
Наиболее часто встречающиеся: объемноцентрированная – Fe- α, Cr, W (на одну ячейку приходится 9 атомов); гранецентрированная – Fe- γ, Al, Cu (14 атомов на ячейку); гексагональная - Mg, Zn (17 атомов на ячейку) (Рис.1.2.). Существуют также ромбоэдрическая, тетрагональная и т.д.
Соответствующая структура кристаллических решеток объясняется типом связей между частицами, т.е. природой сил удерживающих частицы в узлах кристаллической решетки.
Связь между атомами осуществляется электростатическими силами, т.е. по природе связь едина – имеет электрическую природу, но в разных кристаллах может осуществляться различный тип связи: ионная, ковалентная, полярная, металлическая.
Вследствие неодинаковой плотности атомов в различных кристаллографических направлениях (число атомов, приходящееся на то или иное плоское сечение кристаллической решетки, неодинаково) у кристаллов возникает свойство анизотропии, т.е. многие свойства (физические, механические) будут различными в разных направлениях. Анизотропными являются практически все кристаллы, изотропными можно считать стекло, пластмассу.
Кристаллическая решетка характеризуется следующими величинами:
Период решетки – расстояние между центрами соседних частиц. Для кубической решетки – а;для гексагональной а и с (Рис.1.2.)
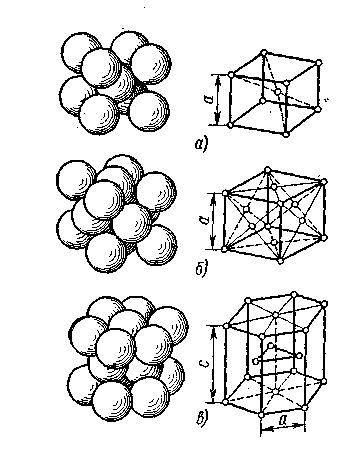
Рис.1.2. Элементарные кристаллические ячейки:
а - кубическая объемноцентрированная;
б - кубическая гранецентрированная;
в – гексагональная плотноупакованная
Координационное число – показывает количество атомов, находящихся на наиболее близком и равном расстоянии от любого выбранного атома в решетке.
Атомный радиус – расстояние между центрами ближайших атомов (он может меняться в зависимости от различных факторов).
Следует отметить еще одну важную особенность кристаллической структуры некоторых материалов. Для некоторых элементов периодической системы характерно наличие двух или трех типов кристаллических решеток.
Это объясняется тем, что у этих элементов происходит перекристаллизация в твердом состоянии, которая называется вторичной кристаллизацией. Наличие разного кристаллического строения вещества при различных температурах называется полиформизмом или аллотропией. Полиморфные превращения сопровождаются выделением или поглощением тепла, а также изменением свойств металла, изменением его объема и растворимости (например углерода в железе). Различные аллотропические состояния называют модификациями. Каждой модификации свойственно оставаться устойчивой лишь в пределах определенного для данного металла интервала температур. Кристаллические модификации обозначаются малыми буквами греческого алфавита a, b, g, которые в виде индекса добавляются к символу обозначающему элемент Fe-a, Fe-g, Ti-a, Ti-g. Буква a обозначает модификацию существующую при самой низкой температуре.
Явление полиформизма в металлах имеет большое практическое значение. Благодаря полиформизму железа, например, имеется возможность широкого изменения свойства сплавов на основе железа (сталей) посредством термической обработки (закалки, отжига).
