
- •Развитие теплофизики и атомистики в XIX веке.
- •Опыты Румфорда
- •Развитие теории мкт в хiх веке.
- •Открытие внешнего фотоэффекта
- •Открытие внешнего фотоэффекта
- •Разработка метода спектрального анализа
- •Создание периодической системы элементов
- •Спектральные серии атома водорода
- •Открытие рентгеновских лучей
- •Открытие электрона
- •Открытие радиоактивности
- •Открытие зависимости массы электрона от скорости
- •Электромагнитная теория материи
- •Исследования природы
Развитие представлений об атомистической картине строения вещества.
Древняя греция.
Желаные объяснить всё многообразиенаблюдаемых вещей некоторой единой основой, а также изучение делимости привело древних греческих мыслителей к основанию атомистики. Основные принципы учения Демокрита: «Из ничего не происходит ничего . Всё изменения происходят блягодаря соединению и разложению частей. Ничего не совершается случайно, но всё совершается по какому-нибудь основанию и с необходимостью. Не существует ничего кроме атомов и пустого пространства. Атомы бесконечны по числу и бесконечно разнообразны по форме. В своём бесконечном движении в пустом пространстве атомы, действуя друг на друга, служат началом образования мира. Бесчисленные миры образуются и снова исчезают одни рядом с другими и одни после других. Различие между атомами происходит от различия их атомов в числе, величине форме и порядке». Демокрит назвал пространство пустым. Некоторые считают, что это связано с тем, что в то время была развита абстрактная геометрия в которой небыло ничего лишнего, а были только геометрические фигуры и пустота, поэтому демокрит и говорил о пустоте и фигурах, а не о той пустоте, которая между атомами в современном представлении.
Первый век до нашей эры.
Эпикур.
В эллинистический период получила дальнейшее развитие атомистическая гипотеза. Одним из самых блестящих представителей афинской натурфилософии был Эпикур. Учение Эпикура о природе основывалось на концепции атомов Демокрита, однако, в его изложении атомная гипотеза получила дальнейшее развитие. Атомы Демокрита – это по существу чисто геометрические образы, они характеризуются лишь формой и объемом. У Эпикура атомы обладают весом, плотностью. Само представление об атомах вводится из хорошо известных фактов. Так, вода испаряется, потому что под действием солнца и ветра от неё отрываются невидимые мельчайшие частицы. Рука медной статуи у городских ворот, к которой прикасаются в поцелуе губы входящих в город, заметно тоньше другой руки, т.к. при поцелуе губы уносят частицы меди.
Атомы, по Эпикуру, находятся в беспорядочном непрерывном движении. Это представление сохранилось до наших дней и лежит в основе современной молекулярно-кинетической теории. Теория Эпикура была изложена в поэтической форме известным римским поэтом и философом Лукрецием Каром в поэме «О природе вещей»:
«... тела существуют, которых Встречи, движения, строй, положения их и фигуры Могут огонь порождать, а, меняя порядок, меняют Также природу, и нет ни с огнем у них сходства, ни с вещью,
Кроме того, никакой, способною к чувствам направить Нашим тела и касаньем своим осязанье затронуть». ...........................................................................................
«Вот посмотри: всякий раз, когда солнечный свет проникает В наши жилища, и мрак прорезает своими лучами, Множество маленьких тел в пустоте ты увидишь, которые Мечутся взад и вперёд в лучистом сиянии света...»
...........................................................................................
«Можешь из этого ты уяснить себе, как неустанно Первоначала вещей в пустоте необъятной мятутся».
Эта модель непрерывно движущихся пылинок аналогична современной картине броуновского движения: видимое движение пылинок возникает от невидимых столкновений с атомами:
«...Кроме того, потому обратить тебе надо вниманье На суматоху в телах, мелькающих в солнечном свете, Что из неё познаешь ты материи также движенья, Происходящие в ней потаенно и скрыто от взора, Ибо увидишь ты там, как много пылинок меняют Путь свой от скрытых толчков и опять отлетают обратно...» .....................................................................................
«Так, исходя от начал, движение мало-помалу Наших касается чувств, и становится видимым также Нам и в пылинках оно, что движутся в солнечном свете, Хоть не заметны толчки, от которых оно происходит».
Одним из ключевых моментов эпикурейского атомизма является учение о том, что многообразие атомов не бесконечно, но бесконечно число атомов каждого сорта:
«Первоначала вещей, как теперь ты легко убедишься, Сходные между собой по своим однородным фигурам, Неисчислимы совсем. Ибо хоть и положены грани Разнице в формах, должны похожие первоначала Или бесчисленны быть, иль материи вся совокупность Будет конечною...»
Эпикур и Лукреций считали, что одним только механическим детерминизмом невозможно объяснить всё разнообразие явлений природы вплоть до возникновения жизни. Поэтому они допускали небольшие случайные отклонения атомов в неопределенных местах, в неопределенные моменты времени («... не в положенный срок и на месте, дотоль неизвестном ...»). Так впервые в истории науки в научный анализ наряду с необходимостью вводится понятие о случайности, т.е. о вероятностном характере поведения физических объектов.
В основе учения Эпикура-Лукреция лежит материалистический принцип сохранения:
« Из ничего не творится ничто по божественной воле...»
А вот как описывает Лукреций представления эпикурейцев о бесконечном пространстве:
«Нет никакого конца ни с одной стороны у Вселенной... Где бы ты ни был, везде с того места, что ты занимаешь, Все бесконечной она остается во всех направленьях».
И, наконец, приведем исключительно точное замечание Лукреция о времени:
«...И неизбежно признать, что никем ощущаться не может Время само по себе, вне движения тел и покоя...»
Эпикур пронаблюдал проуновское движение, и подумав что так движутся этомы постоил довольно провильную картину строения вещества.
В XVII веке зародилось представление о том, что теплота является формой движения частиц, составляющих тело. Однако в XVIII веке повсеместное распространение получила теория теплорода. По этой теории существует некая невесомая и даже, может быть, невещественная материя – теплород. Простое присутствие теплорода в теле обусловливает его нагревание. Чем больше теплорода в теле, тем выше его температура. Контакт нагретого и холодного тела приводит к перетеканию теплорода от первого ко второму, в результате чего температура выравнивается.
Одним из тех, кто, несмотря на укрепление позиций сторонников теплорода, пытался развивать кинетическую теорию теплоты, был Даниил Бернулли. Он считал воздух состоящим из мельчайших частиц, движущихся «чрезвычайно быстро в различных направлениях». Он утверждал, что скорость движения частиц воздуха возрастает с ростом температуры, и объяснял тем самым увеличение упругости воздуха при нагревании. Замечателен окончательный вывод Д. Бернулли о том, что «упругости находятся в отношении, составленном из квадрата скоростей частиц и первой степени плотностей», что полностью соответствует основному уравнению молекулярно-кинетической теории газов в современном изложении:
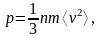
где
p
– давление газа; n
– атомная плотность (концентрация),
т.е. количество атомов (молекул) в единице
объема газа; m
– масса одного атома (молекулы);
 – средний квадрат скорости молекул.
Так Д. Бернулли вошел в историю физики
как один из основателей кинетической
теории газов.
– средний квадрат скорости молекул.
Так Д. Бернулли вошел в историю физики
как один из основателей кинетической
теории газов.
К числу основоположников кинетической теории газов, значительно опередивших свое время, относится и другой представитель российской науки – М. В. Ломоносов. В 1730 году он был принят в московскую Славяно-греко-латинскую академию, в 1735-36 гг. учился в университете при Петербургской Академии наук, а в 1736-41 гг. – за границей, в Марбурге, у известного ученого, ученика Лейбница Христиана Вольфа, и во Фрейбурге, где его образованием руководил ученый и инженер Генкель. В 1741 году Ломоносов вернулся в Петербург, в Академию наук, где и протекала вся его дальнейшая научная деятельность.
Попав в университет при Петербургской Академии наук, а затем за границу, Ломоносов смог овладеть современной ему наукой. При этом, однако, он обнаружил, что в науке того времени не было единства. В ней существовали различные течения, и Ломоносов был поставлен перед выбором, к какому из них примкнуть. Как уже упоминалось, борьба в то время шла в основном между картезианцами – последователями Декарта, и ньютонианцами – сторонниками Ньютона. Картезианцы отвергали существование в природе пустоты. Они считали, что все пространство заполнено материей, являющейся некой идеальной жидкостью, которая находится в вечном движении. В результате движения в материи образуются отдельные частицы, из которых составляются тела. Частицы бывают различных сортов, например, частицы вещества, из которых построены все тела, и частицы другого рода, заполняющие поры между частицами вещества. В частности, такими частицами являются частицы эфира. Взаимодействие между телами или между частицами возможно только при непосредственном контакте в виде удара, толчка или давления. Концепция же Ньютона, как мы знаем, предполагала, что тела воздействуют друг на друга посредством дальнодействующих сил, мгновенно действующих на расстоянии через пустоту.
Когда в Академию пришел Ломоносов, то, несмотря на победу ньютонианцев, отголоски этого спора были еще слышны. В частности, противником дальнодействия был Эйлер. Конечно, у картезианцев и ньютонианцев было много общего. И для тех и для других был характерен механистический взгляд на явления природы. В своем большинстве, как картезианцы, так и ньютонианцы верили в атомистическое строение вещества.
Ломоносову пришелся по душе механистический количественный подход к объяснению явлений природы, но, что касается вопроса о дальнодействии, то Ломоносов сразу же стал противником «притягательных» сил, действующих на расстоянии. И в дальнейшем все его научное творчество несло на себе печать этого отрицательного отношения.
Научные интересы Ломоносова распространялись на значительную часть современных ему естественнонаучных исследований, в частности, исследований в области химии. В отличие от физики химия в первой половине XVIII века еще не сформировалась как одна из естественных наук. Большую роль в становлении химии сыграли работы Бойля, в которых начало формироваться понятие химического элемента. Развивая атомистическую гипотезу в химии, Ломоносов высказал предположение, что частицы, из которых состоит вещество, должны быть двух видов. Во-первых, это «элементы» – частицы, неразложимые при химических превращениях. Эти «элементы» и есть атомы. Во-вторых, имеются «корпускулы», частицы более сложные, состоящие из элементов. При этом одинаковые корпускулы одного и того же вещества состоят из одних и тех же элементов, соединенных одинаковым образом. Если при изменениях, происходящих с веществом, изменяется состав корпускул, значит, происходит химическая реакция. Таким образом, предвосхищая последующие открытия, Ломоносов по существу говорит о существовании наряду с атомами и молекул.
Второе достижение Ломоносова в области химии – это открытие неизменности общего веса веществ при химических реакциях. Химики во времена Ломоносова проповедовали гипотезу так называемого флогистона, или материи огня. Кислород, как и другие газы, составляющие воздух, еще не был известен. Поэтому образование окалины при обжиге металлов объясняли соединением металла с флогистоном, способным проникать через стенки сосуда, внутри которого находился металл. Этой точки зрения придерживался и Роберт Бойль, считавший, что подтвердил ее в следующем опыте. Свинцовый брусок взвешивался и помещался в закрытый стеклянный сосуд. Сосуд со свинцом нагревался, в результате чего свинец превращался в окалину. После этого свинец с окалиной снова взвешивался. Бойль обнаружил, что в результате обжига вес свинца увеличился, и объяснил это тем, что во время обжига через стенки сосуда внутрь него проник флогистон, который, соединившись с металлом, образовал окалину.
Ломоносов был противником теории флогистона. Он предположил, что вес окалины больше веса металла, потому что при обжиге с металлом соединился воздух, находившийся в сосуде. В 1756 году Ломоносов проделал подобный опыт. Он также прокалил в закрытом стеклянном сосуде металл. Но, в отличие от Бойля, он взвесил весь сосуд с металлом до обжига и после. Как показало взвешивание, вес сосуда с металлом не изменился. Следовательно, никакого флогистона через стенки сосуда в него не проникало. Результат этого опыта показал, что общий вес веществ, вступающих в химическую реакцию, до и после реакции остается неизменным. Этим был сделан решающий шаг в установлении закона сохранения веществ при химических реакциях.
Однако, по неизвестной причине, Ломоносов не опубликовал полученного им результата. А в 1774 году Лавуазье опубликовал работу, в которой описал проделанный им аналогичный опыт. Он так же, как и Ломоносов, показал, что вес сосуда с металлом после нагрева не изменяется. Более того, Лавуазье измерил, на сколько увеличился вес металла при нагреве, и сравнил эту величину с уменьшением веса воздуха в сосуде.
Первыми опубликованными работами Ломоносова по физике были работы по теории теплоты и газов, в которых он опирался на атомистические представления. В 1745 году в собрании Академии наук была прочитана работа Ломоносова «Размышления о причине теплоты и стужи». В этой работе Ломоносов применил общие представления об атомистическом строении вещества к тепловым явлениям. Он, опираясь на опытные факты, доказывал правоту кинетической теории теплоты и возражал против теории теплорода.
«Хорошо известно, – писал Ломоносов, – что теплота и огонь возбуждаются посредством движения. От взаимного трения руки согреваются, дерево загорается пламенем, ... железо накаляется при проковывании частыми и сильными ударами. При прекращении движения уменьшается и теплота ...». Будучи твердо уверен в том, что движение в природе не теряется и не появляется из ничего, Ломоносов заключает, что причиной теплоты должно быть движение. Это движение должно быть невидимым движением частиц, составляющих тела. «Достаточное основание для теплоты, – пишет он, – заключается во внутреннем движении материи».
Далее Ломоносов уточняет характер теплового движения частиц. Оно, по его мнению, является вращательным. Частицы (корпускулы) представляют собой шероховатые шарики, подобные зубчатым колесам и способные, сцепляясь друг с другом, передавать движение одной частицы к другой. В твердом теле шероховатые частицы соприкасаются друг с другом и непосредственно передают вращательное движение друг другу. Таким образом происходит теплопередача.
Почему же Ломоносов выдвинул гипотезу о теплоте только как о вращательном движении частиц? Ведь это предположение очень ослабило его работу. Оказывается, все дело было в том, что Ломоносов был ярым противником дальнодействующих сил и не мог прибегать к ним при рассмотрении молекулярного строения тел. А ему надо было объяснить такие противоречащие друг другу свойства, как сцепление частиц и упругость тела; связанность частиц тела и его способность к тепловому расширению. Твердое тело, состоящее из частиц, не взаимодействующих через пустоту на расстоянии, и к тому же обладающих еще и другими степенями свободы, кроме вращательных, не могло бы сохранять формы, т.е. быть твердым телом в полном смысле этого слова. Не признавая дальнодействующих сил, Ломоносов не признавал молекулярных сил, подобных силам тяготения. Поэтому он и приписал частицам твердого тела лишь вращательные степени свободы и, кроме того, в качестве причины стабильности формы твердых тел ввел в рассмотрение эфир. По его предположению, твердые тела не распадаются на части, будучи подвержены со всех сторон давлению частиц эфира.
Приняв в качестве исходной посылки гипотезу о вращательном движении молекул как причине тепла, Ломоносов выводит отсюда ряд следствий:
1. Молекулы (корпускулы) имеют шарообразную форму.
2. При более быстром вращении частиц теплота твердого тела увеличивается; при уменьшении скорости вращения – уменьшается и теплота.
3. Горячие тела должны охлаждаться при соприкосновении с холодными, т.к. частицы холодного тела замедляют движение частиц горячего тела; наоборот, холодные тела при этом нагреваются вследствие ускорения движения их частиц при контакте с частицами горячего тела.
Здесь же Ломоносов указывает, что, поскольку верхнего предела скорости частиц нет (представления о предельном характере скорости света еще не существует), то нет и верхнего предела температуры. Но «по необходимости должна существовать наибольшая и последняя степень холода, которая должна состоять в полном прекращении вращательного движения частиц». Т.е. Ломоносов утверждает существование абсолютного нуля температуры.
Ломоносов включает в свою термодинамическую систему и мировой эфир. «Мы не только говорим, – пишет он, – что такое движение и теплота свойственны и той тончайшей материи эфира, которой заполнены все пространства, ... но и утверждаем, что материя эфира может сообщать полученное от солнца теплотворное движение нашей земле и остальным телам мира и их нагревать, являясь той средой, при помощи которой тела, отдаленные друг от друга, сообщают теплоту без посредничества чего-либо ощутимого». По сути, Ломоносов задолго до Больцмана и Вина включил тепловое излучение в термодинамику.
Следующими работами по физике, опубликованными Ломоносовым, были работы по кинетической теории газов. Их было две: «Попытка теории упругой силы воздуха» и «Прибавление к размышлению об упругости воздуха», опубликованные в 1750 году в трудах Академии. В этих работах Ломоносов разработал теорию упругости воздуха, основываясь на своей модели частиц, образующих тела. Представление о том, что воздух состоит из маленьких частиц, свободно движущихся во все стороны, и что упругость его объясняется ударами этих частиц о стенки сосуда, не было совсем новым. Незадолго перед тем и Даниил Бернулли высказал подобную гипотезу.
Отличие модели Ломоносова от первых молекулярно-кинетических моделей строения газов заключалось только в механизме взаимодействия частиц. Если в этих моделях взаимодействие между атомами или молекулами рассматривалось как взаимодействие сталкивающихся упругих шариков, то Ломоносов предположил иной механизм их взаимодействия. Полагая молекулы газа простейшими объектами, Ломоносов не мог считать их упругими. Упругость молекул надо было объяснять, предполагая их сложное строение. Поэтому он принял, что молекулы газа (которые он мыслил как шероховатые абсолютно твердые шарики) отталкиваются друг от друга подобно сталкивающимся вращающимся волчкам. Вращение же молекул следовало из того, что теплота, по Ломоносову, – это вращательное движение частиц тела. Ломоносов указывает на ряд свойств воздуха, подтверждающих его теорию. Показав, что согласно его модели газ должен следовать закону Бойля-Мариотта, он далее отмечает, что это не совсем верно. Для достаточно сжатых газов этот закон не будет точно выполняться. Ломоносов правильно указывает на причину этого – конечные размеры корпускул газа. Вопрос об отступлении газов от закона Бойля-Мариотта был рассмотрен количественно гораздо позже, только во второй половине XIX столетия Ван-дер-Ваальсом.
Современники не пошли по пути, указанному Д. Бернулли и Ломоносовым. В теории теплоты, как уже было сказано, воцарился теплород.
Развитие теплофизики и атомистики в XIX веке.
К концу XVIII века тепло уже активно использовалось в промышленности. Ещё в 1705 году Ньюкоменом в Англии был создан простейший пароатмосферный двигатель. В 1763 году усовершенствованием двигателя Ньюкомена занялся Джеймс Уатт, который завершил эту работу к 1774 году, а в 1784 году разработал универсальную паровую машину с непрерывным вращением.
Однако физические принципы, управляющие работой паровой машины, оставались непонятыми. Вообще к концу XVIII века физики не очень продвинулись в понимании природы теплоты. Кинетическая теория теплоты М. В. Ломоносова и Д. Бернулли была забыта, в физике «царствовал» теплород, а исследования в области теплофизики сводились в основном к определению термических коэффициентов расширения твёрдых тел и изучению свойств газов.
Опыты Румфорда
Успехи экспериментальной теплофизики и, прежде всего, калориметрии, казалось, свидетельствовали в пользу теплорода. Химики объясняли горение и окисление выделением теплорода. Теория теплорода завоевала особенно широкое признание в последней четверти XVIII века. Этому способствовало появление первых законов сохранения. Если теплород был некоторой жидкой субстанцией, его количество не должно было изменяться при перетекании от нагретого тела к холодному. Но в конце XVIII – начале XIX в. появились новые наглядные доказательства связи теплоты с механическим движением. Конечно, факт выделения тепла при трении был известен с незапамятных времён. Сторонники теории теплорода усматривали в этом явлении нечто аналогичное электризации тел трением – трение, мол, способствует «выжиманию» теплорода из тела.
Первым, кто попытался осмыслить это явление более глубоко, был Бенджамен Томпсон, ставший с 1790 года графом Румфордом. Наблюдая в 1798 году в мюнхенских военных мастерских высверливание каналов в пушечных стволах, он отметил, что при этом выделяется большое количество тепла. Откуда могло браться это тепло? Единственное решение могло бы состоять в том, что в стружках содержится меньше теплорода, чем в сплошной отливке, и избыток его выделяется при сверлении. Но тогда стружку было бы легче нагреть, чем сплошной металл, т.е. у стружки теплоёмкость была бы меньше, чем у сплошного металла; но это решительно противоречило опыту.
Чтобы подробнее исследовать это явление, Румфорд проделал ряд опытов по сверлению канала в цилиндре, выточенном из пушечного металла. В высверленный канал помещали тупое сверло, плотно прилегающее к стенкам канала, и приводили его во вращение. Румфорд проводил этот опыт, погружая цилиндр и сверло в сосуд с водой. В процессе сверления вода нагревалась и спустя некоторое время закипала. Непонятным образом сверлением можно было добыть неограниченное количество тепла. Это никак не укладывалось в модель перетекающего с места на место теплорода.
А. Эйнштейн и Л. Инфельд замечают: «В истории физики часто встречаются такие испытания, которые способны произвести приговор о жизни или смерти теории, они называются crucis (решающими) экспериментами. … Такой решающий эксперимент был произведен Румфордом; он нанес смертельный удар субстанциональной теории теплоты».
В результате произведенных опытов Румфорд пришел к выводу, что теплота не могла быть получена за счет «выжимания» теплорода из металла. «Обсуждая этот предмет, – писал Румфорд, – мы не должны забывать учета того самого замечательного обстоятельства, что источник теплоты, порожденный трением, оказался в этих экспериментах явно неисчерпаемым. Совершенно необходимо добавить, что это нечто, которое любое изолированное тело или система тел может непрерывно поставлять без ограничения, не может быть материальной субстанцией; и мне кажется чрезвычайно трудным, если не совершенно невозможным, создать какую-либо точную идею о чем-то, что в состоянии возбуждаться и передаваться подобно тому, как возбуждается и передается в этих экспериментах теплота, если только не допустить, что это что-то есть движение».
Так Румфорд пришёл к выводу, что теплота является формой движения. Опыты по получению теплоты трением повторил Хэмфри Дэви. Он плавил лёд трением двух кусков льда друг о друга. Дэви пришёл к выводу, что следует оставить гипотезу теплорода и рассматривать теплоту, как колебательное движение частиц материи.
Исследование превращения работы сил трения в тепло создало предпосылки для отрицания теории теплорода. Однако вопреки результатам опытов Румфорда теория теплорода просуществовала еще значительное время. Для того чтобы прийти к закону сохранения и превращения энергии, необходимо было исследовать и процессы превращения теплоты в работу, которые являлись основой функционирования тепловых машин.
Начало XIX века ознаменовалось важными открытиями в химии, стимулировавшими развитие атомистики. Это было открытие закона постоянства состава и закона кратных отношений. Закон постоянства состава был сформулирован в 1801 году французским химиком Прустом. Пруст обнаружил, что процентное содержание компонентов в сложных веществах постоянно и от вещества к веществу изменяется скачком. Закон постоянства состава и скачкообразное изменение весового содержания компонентов в различных соединениях простых веществ подсказывали идею о неизменяемых мельчайших частичках вещества, вступающих во взаимодействие друг с другом в сложных соединениях. Эта мысль была высказана и подробно обоснована Джоном Дальтоном. В 1803 году Дальтон, руководствуясь атомистической гипотезой, ввёл закон кратных отношений и доказал его на примере углеводородных соединений – метана и этилена. Закон кратных отношений утверждает, что если два элемента могут образовать несколько химических соединений, то весовые количества одного из элементов, приходящиеся на одно и то же количество другого элемента в различных соединениях, относятся, как целые числа. Дальтон ввёл фундаментальное понятие атомного веса и, приняв за единицу атомного веса массу атома водорода (1 а. е. м.), определил атомные веса некоторых элементов.
В 1811 году итальянский физик и химик Амедео Авогадро существенно расширил атомистические представления, предложив молекулярную гипотезу строения вещества. По его предположению, молекула вещества – это наименьшая частица, сохраняющая его химические свойства; но она может состоять из нескольких атомов, которые являются мельчайшими частицами химических элементов. Следует также отметить и чрезвычайно оригинальную и плодотворную гипотезу Проута, согласно которой атомы всех химических элементов являются комбинациями атомов водорода.
В 1819 году французские физики Пьер Луи Дюлонг и Алексис Терез Пти эмпирически установили, что произведение удельной теплоёмкости и атомного веса для простых веществ в кристаллическом состоянии является практически постоянной величиной. Так как молярная масса простых веществ пропорциональна их атомному весу, то открытая Дюлонгом и Пти закономерность означала, что молярная теплоёмкость всех простых веществ в твёрдом состоянии одинакова. Сами Дюлонг и Пти не могли дать исчерпывающего объяснения этому факту, равно как и указать границы применимости подмеченной закономерности. Закон Дюлонга и Пти в дальнейшем неоднократно оказывался в центре внимания физиков вплоть до создания основ квантовой теории твёрдого тела.
В общей обстановке эмпиризма лишь два исследования теоретического характера, выполненные в первой четверти XIX столетия, стоят особняком. Первое исследование носило математический характер и оказало существенное влияние на развитие математической физики. Оно было выполнено французским математиком Жаном Батистом Жозефом Фурье и было посвящено вопросу передачи тепла. Его работа «Аналитическая теория тепла» (1822 г.) содержала математическую теорию теплопроводности, которой Фурье занимался с 1807 года. Фурье установил, что поток тепла через поперечное сечение стержня пропорционален не просто разности температур, как считалось ранее, а разности в расчете на единицу длины (т.е. градиенту температуры). Согласно Фурье, количество теплоты Q, протекающей через поверхность площади S за время t, определяется соотношением
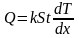 ,
,
где
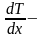 градиент
температуры в одномерном случае, k
– коэффициент теплопроводности,
зависящий от свойств среды. Опираясь
на полученный закон, Фурье вывел
дифференциальное уравнение теплопроводности
градиент
температуры в одномерном случае, k
– коэффициент теплопроводности,
зависящий от свойств среды. Опираясь
на полученный закон, Фурье вывел
дифференциальное уравнение теплопроводности
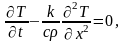
где Т=Т(x,t) – температура; k – коэффициент теплопроводности; c – удельная теплоёмкость; – плотность вещества. Фурье разработал методы интегрирования полученного уравнения при заданных граничных условиях для некоторых частных случаев. С этой целью он применил разложение искомой функции Т(x,t) в ряд по тригонометрическим функциям (ряд Фурье). Возникшая в математике по этому поводу дискуссия оказалась плодотворной, и в математическую физику прочно вошли ряды и интеграл Фурье. В своей теории Фурье рассматривал распространение тепла, как течение некоторой жидкости. Впрочем, для применения данного математического формализма большего и не требовалось. Поэтому его теория казалась очередным достижением теории теплорода.
