
- •О. А. Голубчиков
- •Органический практикум
- •Санкт-Петербург
- •Нии химии сПбГу – 2012
- •Оглавление
- •Предисловие
- •1. Общие правила и методы работы
- •1.1. Планирование работ и ведение рабочего журнала
- •1.1.1. Форма ведения записей в лабораторном журнале
- •1.1.2. Пояснения к составлению таблиц
- •1.1.3. План экспериментальной работы. Отчет о выполнении работы
- •1.2. Правила техники безопасности в лаборатории органического синтеза
- •1.2.1. Общие правила работы
- •1.2.2. Правила обращения с ядовитыми и едкими веществами
- •1.2.3. Правила при работе с огнеопасными веществами
- •1.2.4. Правила при работах, которые могут сопровождаться взрывами или выбросами веществ
- •1.2.5. Правила обращения со стеклом
- •1.3. Основные методы выделения и очистки органических соединений
- •1.3.1 Перекристаллизация Принцип метода
- •Подбор растворителя
- •Практика проведения перекристаллизации
- •Обесцвечивание горячих насыщенных растворов
- •Фильтрование с отсасыванием
- •Сушка органических веществ
- •Определение температуры плавления вещества
- •Контрольные вопросы
- •1.3.2. Перегонка органических жидкостей
- •1.3.2. Простая перегонка при атмосферном давлении
- •Перегонка при уменьшенном давлении (под вакуумом)
- •Перегонка с водяным паром
- •Фракционная перегонка и перегонка с дефлегматором
- •Контрольные вопросы
- •1.3.3. Хроматография
- •Газо-жидкостная хроматография
- •Тонкослойная и бумажная хроматография
- •Нуклеофильное замещение у sp3-гибридизованного атома углерода
- •Нуклеофильное замещение у sp2-гибридизованного карбонильного углерода
- •Контрольные вопросы
- •2.1.2. Бромистый изопропил
- •Примечания:
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.1.3. Ацетанилид (метод а)
- •2.1.4. Ацетанилид (метод б)
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.1.5. Ацетилсалициловая кислота (аспирин)
- •Пояснения к синтезу
- •Контрольные вопросы
- •Пояснения к синтезу
- •2.2. Электрофильное замещение в ароматическом ряду
- •2.2.1. Основные теоретические положения
- •2.2.2. Нитротолуолы (смесь изомеров)
- •Хроматографическое определение изомерного состава нитротолуолов
- •Пояснения к синтезу
- •Контрольные вопросы
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.2.4. Cульфаниловая кислота
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.3. Восстановление нитросоединений
- •2.3.1. Основные теоретические положения
- •Восстановление металлами в присутствии растворов электролитов
- •Восстановление в кислой среде металлами
- •Пути восстановления нитросоединений в зависимости от pH среды Восстановление в кислой среде
- •Восстановление в щелочной среде
- •Восстановление в щелочной среде растворами сульфидов. Селективное восстановление полинитросоединений
- •Определение конца реакции
- •Выделение продуктов реакции
- •Меры предосторожности при работе с ароматическими аминами
- •2.3.2. Анилин
- •Выделение анилина из реакционной смеси
- •2.3.3. Выделение и идентификация аминов
- •Пояснения к синтезу
- •Экстракция органических веществ из водных растворов
- •Контрольные вопросы
- •2.3.4. Мета-Нитроанилин
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.4. Получение и превращения диазосоединений
- •2.4.1. Основные теоретические положения
- •Получение ароматических диазосоединений
- •Механизм диазотирования
- •Факторы, влияющие на скорость диазотирования
- •Контроль диазотирования
- •Формы диазосоединений
- •Превращения диазосоединений Азосочетание
- •Реакции солей диазония с выделением азота
- •2.4.2. Йодбензол
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.4.5. Метилоранж
- •Примечания к синтезу
- •Метиловый оранжевый:
- •2.4.6. Кислотный оранжевый (-нафтолоранж)
- •Азосочетание
- •2.4.7. Резорциновый желтый (тропеолин)
- •Азосочетание
- •2.4.8. Спектрофотометрическое определение содержания красителя в растворе
- •2.4.9. Пояснения к синтезам азокрасителей
- •Контрольные вопросы
- •2.5. Окисление
- •2.5.1. Основные теоретические положения
- •2.5.2. Бензойная кислота (из толуола)
- •Примечание
- •2.5.3. Бензойная кислота (из бензилового спирта)
- •Пояснения к синтезам бензойной кислоты (2.5.2 и 2.5.3)
- •Контрольные вопросы
- •2.5.4. Масляный альдегид (бутаналь)
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.5.5. Бензальдегид
- •Пояснения к синтезу
- •Контрольные вопросы
- •3. Синтез гетероциклических соединений
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Бензимидазол
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Хинолин (синтез Скраупа)
- •Пояснения к синтезу
- •Фенилизоиндолизин
- •Пояснения к синтезу
- •Фенотиазин
- •Пояснения к синтезу
- •5,10,15,20-Тетрафенилпорфирины
- •5,10,15,20-Тетрафенилпорфирин
- •Пояснения к синтезу
- •Хроматографическая очистка тетрафенилпорфирина
- •5,10,15, 20-Тетракис(4-нитрофенил)порфирин
- •Пояснения к синтезу
- •5,10,15,20-Тетракис(4-бромфенил)порфирин
- •Приложение
- •Список рекомендуемой литературы
Перегонка с водяным паром
Для отгонки многих органических соединений широко пользуются перегонкой с водяным паром. Этот прием применим, когда требуется отогнать нерастворимые в воде органические вещества от неорганических солей или отделить летучие с парами воды соединения от нелетучих. Установка для перегонки с паром изображена на рис. 7.
Колба-парогенератор (2) должна быть заполнена водой не более чем наполовину. Нижний конец предохранительной трубки (1) должен быть погружен в воду. Если произойдет закупорка системы, например, забьется конец вводной трубки (5) или закристаллизовавшийся продукт забьет трубку холодильника, вода будет подниматься по предохраняющей трубке. В этом случае необходимо, соблюдая предосторожность, убрать газовую горелку из-под парообразователя, отсоединить резиновую трубку (3) от перегонной колбы и устранить причину закупорки.
В качестве перегонной обычно используют круглодонную колбу емкостью не менее 500 мл. Она должна быть поставлена наклонно и заполнена не более чем на 1/3 своего объема. Перед началом отгонки перегонную колбу осторожно подогревают горелкой, чтобы избежать накопления в ней конденсата. Трубка (5), по которой водяной пар поступает в колбу (4), доходит почти до дна колбы. Вводимый в колбу водяной пар увлекает с собой образующиеся над поверхностью жидкости пары органического вещества и уносит их в холодильник (7). В холодильнике пары конденсируются, и жидкость через алонж (8) стекает в приемник (9).
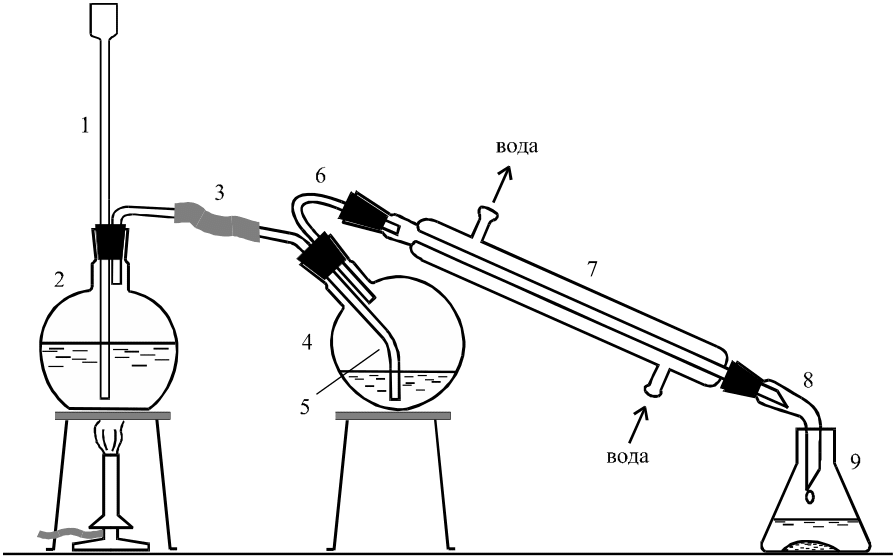
Рис. 7. Схема установки для перегонки с водяным паром: 1 – предохранительная трубка, 2 – колба-парогенератор, 3 – соединительная резиновая трубка, 4 – перегонная колба, 5 – трубка для ввода водяного пара, 6 – выводная трубка, 7 – прямой водяной холодильник; 8 – алонж, 9 – приемная колба
Если дистиллят застывает в холодильнике, то время от времени выключают охлаждающую воду, продолжая пропускать пар через холодильник. При этом вода в рубашке холодильника разогревается и закристаллизовавшееся вещество плавится. Следует избегать проскока пара через холодильник. Это приводит к попаданию ядовитых паров в помещение лаборатории.
Отгонку ведут до тех пор, пока стекающий дистиллят не становится прозрачным. По окончании перегонки, потушив горелку под парообразователем, нужно снять зажим между сосудами (2) и (4) во избежание перетягивания содержимого колбы в парообразователь.
Причину перегонки с водяным паром объясняет закон Дальтона, согласно которому общее давление смеси газов равно сумме парциальных давлений компонентов.
Несмешивающиеся вещества при нагревании в герметически закрытом сосуде образуют насыщенные пары, парциальные давления которых зависят только от температуры и теоретически равны давлению паров чистых компонентов. Иначе говоря, в 1 м3 смеси насыщенных паров содержится одновременно такое же количество каждого компонента, какое заключалось бы в 1 м3 насыщенного пара каждого из компонентов, взятого в чистом виде. Общее давление над жидкой смесью в этом случае равно сумме парциальных давлений паров всех ее компонентов.
Рассмотрим конкретный пример. При 98,4 С давление насыщенного пара анилина составляет 43, а воды – 717 мм. рт. ст. Анилин практически не растворяется в воде так же, как вода в анилине. Поэтому суммарное давление паров над смесью воды с анилином при этой температуре равно атмосферному: 43 + 717 = 760 мм. рт. ст. Если давление насыщенного пара жидкости равно атмосферному, она кипит. Следовательно, смесь анилина с водой закипит при температуре ниже, чем температура кипения чистой воды. Для справки, температура кипения чистого анилина равна 184 С.
Уравнение идеального газа (pv = nRT) в приложении к анилину (А) и воде (В) имеет вид: pAv = (mA/MA)RТ и pВv = (mВ/MВ)RТ соответственно. Здесь v – объем смеси паров, Т – температура, R – газовая постоянная, mA и mB – массы, МA и МB – мольные массы, рA и рB – парциальные давления паров анилина и воды соответственно.
Принимая во внимание, что объем, занимаемый парами воды и анилина, одинаков, получим:
mA/mВ = (pAMA)/(pВMВ) = (4393)/(71718) = 1/3,23.
Это значит, что в парах на одну весовую часть анилина приходится 3,23 весовые части воды, т. е. содержание анилина в равновесной смеси паров должно составлять 23,6 %. В реальных условиях соотношение анилин : вода значительно меньше, так как при быстром пропускании водяного пара через реакционную массу давление пара анилина не успевает достичь равновесного значения. Кроме того, анилин, хотя и мало, но все-таки растворим в воде (в 100 г воды растворяется 3,4 г при 20 и 6,4 г при 90 С). Поэтому применять закон Дальтона для системы вода – анилин можно только с известными оговорками.
