
- •Закон эквивалентов.
- •Предмет и содержание химической кинетики. Основные определения и понятия.
- •Гомогенные и гетерогенные процессы. Скорость их протекания.
- •Зависимость скорости процессов от концентрации реагирующих веществ. Закон действия масс (здм).
- •Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса. Энергия активации.
- •Зависимость скорости реакции от площади поверхности взаимодействия (гетерогенный процесс).
- •Зависимость скорости реакции от катализатора. Механизм его действия.
- •Обратимые и необратимые процессы. Химическое равновесие. Кинетическое условие химического равновесия.
- •Константа равновесия. Зависимость от различных факторов.
- •Смещение химического равновесия. Принцип Ле Шателье.
- •Общая характеристика растворов.
- •Способы выражения концентрированных растворов.
- •Растворы электролитов. Электролитическая диссоциация и механизм её протекания. Диссоциация кислот, солей и оснований.
- •Слабые электролиты. Константа диссоциации, степень диссоциации. Закон разбавления Оствальда. Определение концентрации ионов в слабых электролитов.
- •Произведение растворимости для труднорастворимых солей.
- •Ионное произведение воды. Водородный (рН) и гидроксильный (рОн) показатели.
- •Сильные электролиты. Активность ионов. Ионная сила электролитов. Определение концентрации ионов в сильных электролитах.
- •Гидролиз солей. Константа гидролиза и степень гидролиза.
- •Овр. Метод электронно-ионных схем для написания овр.
- •Комплексные соединения.
- •Современная теория строения атома.
- •Квантовые числа (n,l,m,s).
- •Многоэлектронные атомы. Принцип Паули. Правило Хунда. Правило Клечковского.
- •Периодический закон и таблица Менделеева. Электронная структура атомов.
- •Периодичность свойств элементов по таблице Менделеева. Энергия ионизации. Энергия сродства к электрону. Электроотрицательность. Степень окисления и ионные радиусы.
- •Значение периодического закона.
- •Основные характеристики химической связи: длина связи, прочность связи, направленность связи (валентные углы).
- •Квантово-механическое объяснение химической связи (на примере молекулы н2).
Закон эквивалентов.
Вещества
взаимодействуют друг с другом в
количествах, пропорциональных их
эквивалентам, или массы (объемы)
реагирующих веществ пропорциональны
их эквивалентным массам (объемам):
![]()
Эквивалентом (Э) химического элемента называется такое его количество, которое соединяется (замещает) с 1 моль атомов водорода или Ѕ моль атомов кислорода, выражается в молях (М).
Эквивалентная
масса
(М Э ) – масса одного эквивалента
вещества, выраженная в граммах.
Эквивалент
водорода
равен его молю атомов, т.е.
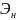 =1М,
а эквивалентная масса водорода равна
1 г/моль.
=1М,
а эквивалентная масса водорода равна
1 г/моль.
Эквивалент
кислорода
равен Ѕ моль атомов кислорода, т.е.
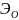 = 1/2 M, а эквивалентная масса кислорода
равна 8 г/моль.
= 1/2 M, а эквивалентная масса кислорода
равна 8 г/моль.
Эквивалентным
объемом
( )
называется объем, занимаемый при данных
условиях одним эквивалентом газообразного
вещества.
)
называется объем, занимаемый при данных
условиях одним эквивалентом газообразного
вещества.
Эквиваленты и эквивалентные массы простых веществ рассчитываются по формуле:
![]()
Эквивалентом сложного вещества называется такое его количество, ко- торое может замещать, присоединять или быть каким-либо другим способом эквивалентно одному иону водорода в кислотно-основных или ионообменных реакциях или одному электрону в окислительно-восстановительных реакциях.
![]()
![]()
![]()
![]()
Предмет и содержание химической кинетики. Основные определения и понятия.
Раздел химии, изучающий механизм и скорость протекания химических реакций, называется химической кинетикой.
Одной из задач химической кинетики является установление элементарных взаимодействий, которые определяют действительный путь физико-химического процесса.
Объектом изучения химической кинетики является система. Система – совокупность материальных объектов, находящихся во взаимодействии мысленно или фактически выделенные из окружающей среды.
Системы бывают: гомогенные, гетерогенные.
Гомогенная система – все вещества в одной фазе и между ними нет поверхностей раздела.
Гетерогенная система – вещества находятся в различных фазах и между ними есть поверхности раздела.
Фаза – однородная часть системы одинаковая по составу и свойствам в различных её точках и отделённая от других частей поверхностями раздела.
Гомогенные и гетерогенные процессы. Скорость их протекания.
Гомогенная система – все вещества в одной фазе и между ними нет поверхностей раздела.
Гетерогенная система – вещества находятся в различных фазах и между ними есть поверхности раздела.

Зависимость скорости процессов от концентрации реагирующих веществ. Закон действия масс (здм).
Скорость реакций зависит от природы реагирующих веществ, концентрации или парциальных давлений (для газов), температуры, давления, присутствия катализатора, от величины поверхности взаимодействия.
ЗДМ: скорость гомогенной реакции при постоянной температуре прямо пропорциональна произведению концентраций (давлений) реагирующих веществ, возведенных в степень, с показателями, равными стехиометрическим коэффициентам, стоящим в уравнении реакции.
