
Хлоропрен
Среди хлорсодержащих мономеров получивших широкое применение в производстве синтетических каучуков и пластмасс наиболее важным является хлоропрен:
Хлоропрен – жидкость с температурой кипения 59,4 0С с характерным запахом, в воде растворяется плохо, но смешивается со многими органическими растворителями. Хлоропрен горюч и токсичен. При малых концентрациях вызывает раздражение слизистых оболочек. В промышленности его получают двумя способами:
Из углеводородов С4 нормального строения, а именно бутадиен-1,3 или бутан-бутеновой фракции
Из ацетилена через промежуточное образование винилацетилена.
Первый способ. Проводят газофазное хлорирование углеводородов С4 при Т=400 0С. При хлорировании дивинила Т=270-320 0С. Берут избыток углеводорода:

Реакционные газы на выходе из хлоратора быстро охлаждают и направляют в отпарную колону, где происходит отделение хлорорганических продуктов от непрореагирующего углеводорода и хлороводорода возвращают в процесс. Образующиеся хлорорганические продукты – смесь моно- и дихлорбутенов подвергают ректификации с целью разделения моно- от дихлорпроизводных. Монохлорпроизводные затем подвергаются пиролизу при Т=600 0С. При этом образуются дивинил и бутены в смеси с НCl. Всю эту смесь возвращают в процесс на хлорирование. Смесь дихлорпроизводных подвергают изомеризации в присутствии солей меди – чаще всего нафтенат меди в жидкой фазе:

1,4 дихлоризобутен-2 изомеризуется в 3,4- дихлорбутен-1,который направляется в секционированный реактор,в котором проводят дегидрохлорирование при нагревании в присутствии 20% р-ра NaOH или КОН в хлорпрен:

Хлорпрен отделяют от непрореагировавших продуктов и подвергают ректификации.
Второй способ. Хлорпрен получается жидкофазным гидрохлорированием винилацетилена, предварительно полученного димеризацией ацетилена
1)

кат 35-50% раствор хлоридов меди(I) или хлорида аммония в соляной кислоте.
Побочная реакция:
Образование высших полимеров ацетилена
Образование продуктов гидратации
Образование продуктов гидрохлорирования ацетилена и винилацетилена
2) Гидрохлорирование ацетилена с образованием хлоропрена:
T = 60-80oC t= 15сек
Далее происходит гидротация винилацетилена с образованием метилвинил кетона
Димеризация хлорпрена с образованием циклических соединений
Механизм реакции предложен Карозерсом, катализатор- CuCl

образуется 4 хлорбутадиен1,2,который изомеризуется в хлорпрен
Долгопольский и сотрудники полагают что гидрохлорирование винилацетилена происходит через образование промежуточного комплекса соединения винилацетилена с компонентами катализатора,в процессе комплексообразования важную роль играет хлорид меди (I), поэтому его концентрация определяет производительность катализатора, повысить которую можно за счет повышения в нем содержания хлорида меди и соляной кислоты. Однако с увеличением кислотности катализатора усиливается образование побочных продуктов. Во избежание побочного образования 1,3 дихлорбутена-2 хлорпрен непрерывно выводят из зоны реакции. Сырой продукт стабилизируют пирокатехином 0,5-1% и подвергают ректификации. Выход хлоропрена достигает 80%, образуется 1,4дихлорбутен-2,дегидрохлорированием его превращают в хлорпрен. Т=250-270о С

Реакцию проводят в г/ф на селикагеле или каолине с выходом хлорпрена 67-75%.
Технологическая схема в мет. стр 59. кирпичников стр 86
Изобутилен(2 метилпропен) – при нормальных условиях бесцветный газ с неприятным запахом, нерастворяется в воде, растворяется в этиловом спирте и диэтиловом эфире. Изобутилен применяют для получения полиизобутилена и бутилкаучука,а также для производства изопрена методом конденсации изобутилена с формальдегидом,кроме того изобутилен используют в качестве добавки к смазочным маслам,для пропитки в качестве электроизоляционных материалов.
Методы получения:
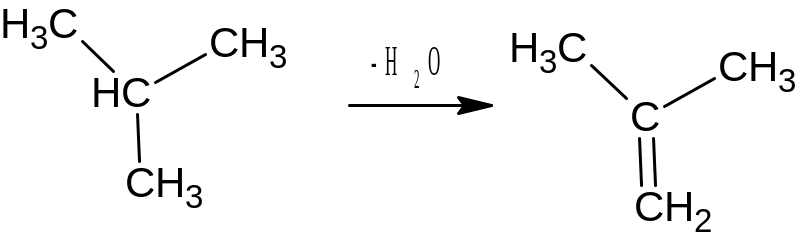
Дегидротацией изобутанола при Т= 380о С

Выделение изобутилена из бутанбутеновой фракции газов крекинга. Этот способ экономически выгоден.
Дегидрирование изобутана. Дегидрирование проводят в присутствии алюмо хромового катализатора при Т=500-550оС
Смесь бутенов не может быть разделена простой ректификацией из за близости Ткип , поэтому используют химические методы разделения:
Выделение изобутелена из фракции С4 с помощью серной кислоты.
Выделение изобутелена из фракции С4 на ионообменных смолах.
Выделение изобутелена из фракции С4 при помощи низших спиртов.
Первый метод разделения. При обработки смеси бутенов серной кислотой при Т=35-40о С нормальные бутены не вступают в реакцию, реагирует только изобутилен с образованием третбутил серной кислоты:
Побочно образуется небольшое количество полимеров:
Гидролиз третбутил серной кислоты приводит к образованию третбутанола:
который тут же дегитратируется в изобутилен:
Схема выделения изобутилена
Гидролиз и дегидротация осуществляется в колонне регенераторе,в котором пропускают водяной пар,из верхней части колонны отбирают изобутилен,содержащий примеся третбутанола, полимера и др побочных веществ. Изобутилен отделяют от примесей и конденсируют. Из нижней части колонны выходит 45% серная кислота, которую регенерируют упариванием до исходной 65% кислоты. Выход изобутилена -90-95% от поступившей на разделение.
2 метод разделения -более совершенный . Проводят прямую гидратацию на катионите КУ-2 в третбутанол, Т= 90-100оС,Р=1-1,5МПА
Достоинства:
1) Не используется кислота,т.е отсутствует коррозионно-активная среда.
2) Нет стадии регенерации кислоты
3) Возможно многократное использование КУ-2
4) Высокая частота получаемого изобутена
Затем третбутанол на том же катализаторе при Т=100-105оС и Р= 0,34МПа дегидратируется в изобутилен
3 метод разделения. Метанол избирательно образует с изобутиленом метилтретбутиловый эфир.
Процесс проводят в присутствии ионитных катализаторов, затем проводят разложение по обратимой реакции в присутствии катализаторов кислотного типа при Т=100-3000С, Р=1 МПа. Для подавления побочных реакции разложение ведут при разбавлении водяным паром. Перспективный способ.
4 метод разделения. Дегидрирование изобутанола. У нас в стране изобутилен получают дегидрированием изобутанола, катализатор Al-Cr, Т=550-5800 С
Обьемная скорость 120-150 час -1
Термодинамика дегидрирования изобутанола аналогично ДГ н- бутана. Процесс ДГ изобутана идет пи более низкой температуре,что обьясняет более низкой энергии связи С-Н у третичного атома углерода. Процесс проводят в псевдоожиженном слое катализатора, выход изобутилена на пропущенный изобутан достигает 38-42% при селективноси 80%
Изобутан-изобутеленовая фракцию выделяют из контактного газа дегидрирования,аборбцией и ректификацией, разделение изобутан-изобутеленовой фракции осуществляется серной кислотой.
Изобутилен полученный этим методом в 5 раз дешевле, чем полученный дегидрированием изобутанола оксосинтезом.
