
- •Процессы переноса в биологических системах. Биоэлектрогенез
- •Перенос молекул (атомов) через мембраны. Уравнение Фика
- •Уравнение Нернста—Планка. Перенос ионов через мембраны
- •Активный транспорт. Опыт Уссинга
- •Равновесный и стационарный мембранные потенциалы. Потенциал покоя
- •Потенциал действия и его распространение
Потенциал действия и его распространение
Все живые клетки при действии различных раздражителей (химических, механических, температурных и пр.) способны переходить в возбужденное состояние. Опыт показывает, что возбужденный участок становится электроотрицательным по отношению к покоящемуся, что является показателем перераспределения ионных потоков в возбужденном участке. Реверсия потенциала при возбуждении кратковременна, и после окончания возбуждения через некоторое время вновь восстанавливается исходный потенциал покоя. Общее изменение разности потенциалов на мембране, происходящее при возбуждении клеток, называется потенциалом действия. На рис. 4 представлен потенциал действия гигантского аксона кальмара, обозначены отдельные стадии изменения потенциала. В частности, для клетки характерен так называемый запаздывающий потенциал, когда в течение некоторого времени на мембране существует даже меньший потенциал, чем потенциал покоя.
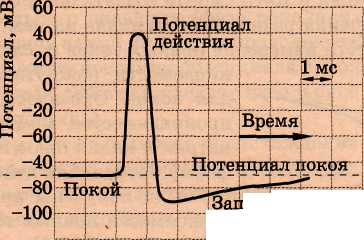
Было показано, что возбуждение связано с увеличением электропроводности клеточной мембраны. При этом временная зависимость электропроводимости повторяла форму потенциала действия. Чтобы решить вопрос, для каких ионов изменяется проницаемость мембраны, следует обратить внимание, что потенциал действия приводит к кратковременному возрастанию потенциала внутри клетки). Отрицательный относительно внешней среды потенциал становится положительным. Если по уравнению Нернста (11.38) вычислить равновесные потенциалы на мембране аксона кальмара, то получим соответственно для ионов К+, Na+ и С1~ величины -90, +46 и -29 мВ. Так как при изменении проницаемости мембраны для какого-либо иона этот ион будет проникать через нее, стремясь создать равновесное состояние, то числовые данные показывают, что внутрь клетки проникают ионы Na+, создавая там положительный потенциал. Следовательно, при возбуждении клетки в начальный период увеличивается проницаемость мембран именно для ионов натрия. «Натриевая теория» возникновения потенциала действия была предложена, разработана и экспериментально подтверждена А. Ходжкином и А. Хаксли, за что в 1963 г. они были удостоены Нобелевской премии.
Измерить проницаемость мембран для какого-либо иона (иначе говоря, электропроводимость или сопротивление мембраны для того иона) можно, если на основании закона Ома найти отношение тока к напряжению, или наоборот. Практическая реализация такой задачи осложняется тем, что проницаемость (электрическое сопротивление мембраны при возбуждении изменяется со временем. Это приводит к перераспределению электрического напряжения в цепи, и разность потенциалов на мембране изменяется. Ходжкин, Хаксли и Катц смогли создать опыт с фиксацией определенного значения разности потенциала на мембране. Это позволило им провести измерение ионных токов и, следовательно, проницаемости (сопротивления) мембран ля ионов. Оказалось, что отношение проницаемостей мембраны для ионов натрия и Калия практически повторяет форму потенциала действия.
ПРАКТИКА
Физические процессы
в биологических мембранах
Уравнение Фика
![]()
где J — плотность потока диффундирующего вещества,
D — коэффициент диффузии,
![]() - производная
от концентрации диффундирующего
вещества по направлению х
(проекция
градиента
концентраций на направление х).
- производная
от концентрации диффундирующего
вещества по направлению х
(проекция
градиента
концентраций на направление х).
Уравнение Теорелла
![]()
Здесь
![]() -электрохимический
потенциал;
-электрохимический
потенциал;
![]()
— подвижность, где R — молярная газовая постоянная.
Средняя величина смещения молекулы вещества в растворе
x = 2Dt,
где D — коэффициент диффузии, t — время.
Характерное время установления равновесной концентрации
![]()
Здесь V — объем клетки; S — площадь поверхности клеточной мембраны:
![]()
где Р — коэффициент проницаемости мембраны для данного вещества,
l - толщина мембраны,
К — коэффициент распределения вещества.
Формула Нернста
![]()
Здесь
![]() —
равновесный мембранный потенциал,
—
равновесный мембранный потенциал,
СоиС1— концентрации данного иона снаружи и внутри клетки,
F — постоянная Фарадея,
Z — валентность иона.
Уравнение Голъдмана—Ходжкина—Катца

где
![]() —
мембранный потенциал,
—
мембранный потенциал,
РK, PNa, PCl— проницаемости мембраны для оответствующих ионов,
[К+]о, [Na+]0, [Сl -] концентрации ионов снаружи клетки,
[K+]j, [Na+]i [Cl-]I — концентрации этих же ионов внутри нее.
Потенциал поля заряда q в электролите
![]()
где
r
— расстояние,
![]() — дебаевский радиус экранирования.
— дебаевский радиус экранирования.
В общем случае, когда в растворе присутствует несколько ионов,

где Zt — валентность иона, ci— концентрация соответствующего иона, — диэлектрическая проницаемость растворителя.
