
- •Оглавление
- •Биохимия белков, состав, функции Роль аминокислот в организме
- •Классификация
- •Биологические функции белково-пептидных веществ.
- •Физико-химические свойства белков
- •Уровни структурной организации белков Первичная структура
- •Вторичная структура
- •Третичная структура
- •Четвертичная структура
- •Способность белков к специфическим взаимодействиям
- •Самосборка белков и надмолекулярных структур
- •Витамин, структура, функции Описание
- •Особенности жирорастворимых витаминов
- •Ретинол (витамин а)
- •Кальциферол (витаминD)
- •Токоферол (витаминE)
- •Нафтохиноны (витамин к)
- •Особенности водорастворимых витаминов
- •Аскорбиновая кислота (витамин с)
- •Витамин проницаемости (Витамин р)
- •Биотин (витамин н)
- •Тиамин (витамин в1)
- •Рибофлавин (витамин в2)
- •Никотиновая кислота (витамин рр, ниацин, витамин в3)
- •Пиридоксин (витамин в6)
- •Пантотеновая кислота (витамин в5)
- •Фолацин (витамин в9)
- •Фолиевая кислота
- •Цианокобаламин (витамин в12)
- •Цикл Кребса (Цикл трикарбоновых кислот)
- •Реакции цикла трикарбоновых кислот.
- •Первая реакция цикла
- •Вторая реакция цикла
- •Третья реакция цикла
- •Четвертая реакция цикла
- •Пятая реакция
- •Шестая реакция
- •Седьмая реакция
- •Восьмая реакция
- •Биоэнергетика цикла трикарбоновых кислот
- •Регуляция превращения пирувата в ацетил-СоА и цикла трикарбоновых кислот
Фолиевая кислота
Широко распространена в растительном и животном мире. Наиболее богатые ее источники - печень, почки и зеленые листья растений, особенно салаты из пищевой зелени (напр., салата, шпината). Она синтезируется растениями, многими бактериями и грибками. Фолиевая кислота легко разрушается при кулинарной обработке продуктов. В процессе изготовления первых блюд овощи и мясо теряют около 70-90% этого витамина. велики потери также при консервировании продуктов.
Цианокобаламин (витамин в12)
Принадлежит к веществам с высокой биологической активностью. В этом витамине нуждаются все животные организмы. Основное значение этого витамина - в его антианемическом действии, к тому же он оказывает существенное влияние на процессы обмена веществ - белков, синтез аминокислот, нуклеиновых кислот, пуринов, участвует в процессах кроветворения. У детей стимулирует рост и вызывает улучшение их общего состояния. В чистом виде представляет собой красное кристаллическое вещество в виде игл или призм без вкуса и запаха. Теряет свою активность под действием света. Суточная потребность - 3 мкг. Невозможность использования в организме В12 возникает в результате атрофии железистых клеток дна желудка, продуцирующих гастромукопротеин, который является обязательным компонентом, обеспечивающим усвоение этого витамина организмом. Глистные иннвазии могут полностью захватить витамин В12 и лишить организм. При потреблении белого хлеба, в котором мало клетчатки, необходимой для нормального существования микрофлоры, а также имеются дрожжи пекарские, синтез витамина В12 будет нарушен. Результатом может стать анемия и малокровие.
Цикл Кребса (Цикл трикарбоновых кислот)
У аэробных организмов (животные, растения, многие микроорганизмы) пируват подвергается превращению — окислительному декарбоксилированию с образованием ацетил-СоА. Этот активированный ацетильный комплекс далее полностью окисляется до С02и Н20, вовлекаясь в так называемый цикл трикарбоновых кислот (ЦТК). Этот цикл известен также под названием цикла лимонной кислоты или цикла Кребса в честь Ганса Кребса (лауреата Нобелевской премии 1953 г.), определившего последовательность реакций цикла. Сущность цикла и заключается в окислительном разложении ацетильного остатка, в результате чего освобождаемая энергия запасается в виде АТР. Хотя цикл трикарбоновых кислот мы рассматриваем во взаимосвязи с катаболизмом углеводов, однако его роль в метаболизме веществ гораздо шире. Он выполняет следующие функции:
1. Интегративную — объединяет пути катаболизма углеводов, жиров и белков; во всех аэробных организмах он выступает в роли центрального метаболического пути углерода.
2. Амфиболическую — выполняет не только катаболическую функцию распада ацетильных остатков, но и анаболическую, поскольку субстраты цикла используются для синтеза других веществ.
3. Энергетическую — совместно с цепью переноса электронов является основным поставщиком химической энергии в форме АТР.
Окислительное декарбоксилирование пирувата с образованием ацетил-СоА и реакции цикла трикарбоновых кислот осуществляются в клеточных органеллах — митохондриях. Биохимические функции цикла указывают на то, что ацетат и любой компонент цикла должны быть хорошими источниками энергии и их можно употреблять с пищей как ценные энергетические вещества, лишь бы они, поступив в клетку, могли достигнуть ферментной системы, находящейся в митохондриях. Однако основным источником энергии аэробных организмов является углеводный материал, из которого она извлекается в ходе совместных процессов гликолиза и цикла трикарбоновых кислот. Сопряжение этих путей происходит на уровне превращения пируват —> ацетил-СоА, катализируемого пируватде-гидрогеназным комплексом. В ходе реакции происходит окислительное декарбоксилирование α-оксокислоты (прирувата) и образование тиоэфира:

Окислительное декарбоксилирование пирувата. Пируватдегид-рогеназный комплекс представляет собой мультиферментную систему, включающую три фермента, каждый из которых катализирует определенную стадию окислительного декарбоксилирования.
Таблица № 1: Пируватдегидрогеназный комплекс
|
Фермент |
Число цепей в молекуле |
Кофактор |
Катализируемая реакция |
|
Пируватдегидрогеназный компонент |
24 |
ТРР |
Декарбоксилирование пирувата |
|
Дигидролипоил-трансацетилаза |
12 |
Липоамид |
Окисление С2-фрагмента и перенос наCoA-SH |
|
Дегидролипоил-дегидрогеназа |
12 |
FAD |
Регенерирование окисленной формы липоамида |
В процессе окислительного декарбоксилирования принимают участие пять кофакторов: тиаминпирофосфат (ТРР), липоамид, CoA-SH, FAD, NAD и три фермента: пируватдегидрогеназа, трансацетилаза и дигидролипоилдегидрогеназа.
На первой стадии пируват соединяется с ТРР и подвергается декарбоксилированию. На второй стадии гидроксиэтильная группа, связанная с ТРР, окисляется с образованием ацетильной группы и одновременно переносится на липоамид. Окисление катализируется дигидролипоилтрансацетилазным компонентом. Липоамид представляет собой остаток липоевой кислоты, присоединенный к специфической лизиновой боковой цепи трансацетилазного компонента:
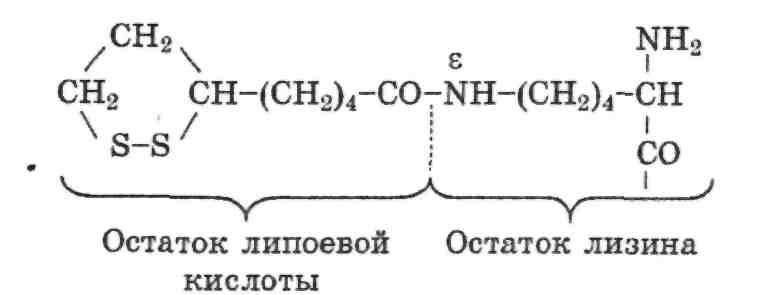
Окислителем в реакции служит S-S-группа липоамида, восстанавливающаяся в SH-группы:
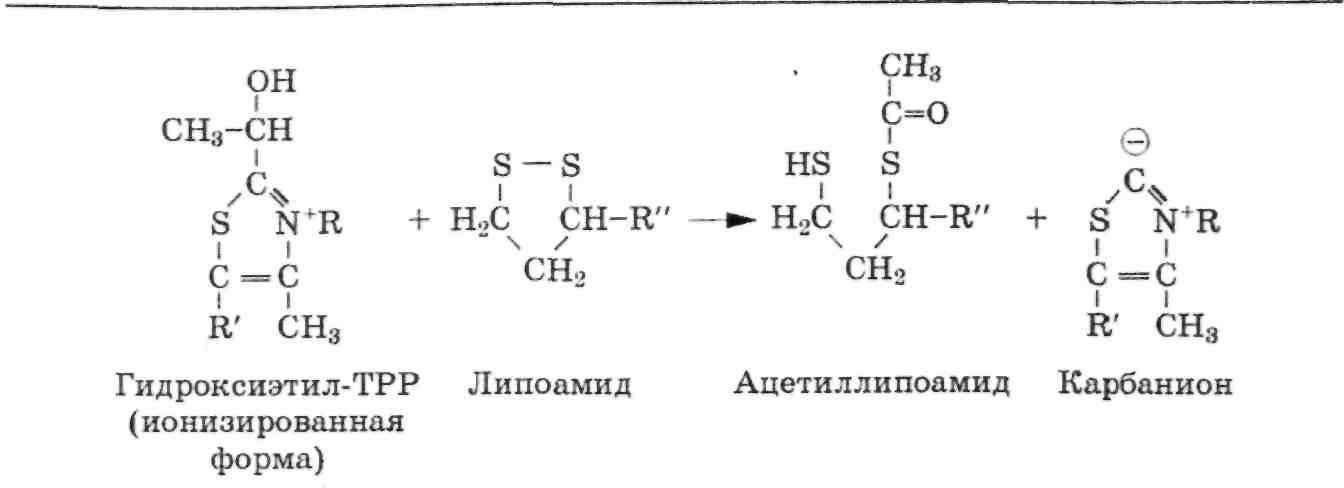
Затем ацетильная группа переносится с ацетиллипоамида на СоА, образуя ацетил-СоА:
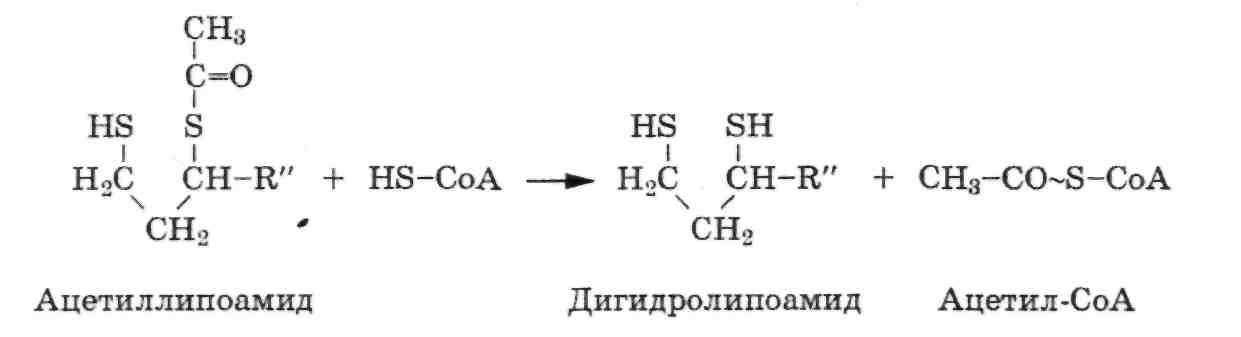
При переходе ацетильной группы на СоА сохраняется богатая энергией тиоэфирная связь.
На третьей, завершающей, стадии происходит восстановление окислительной формы липоамида. Реакция катализируется дигидролипоилдегидрогеназным компонентом:
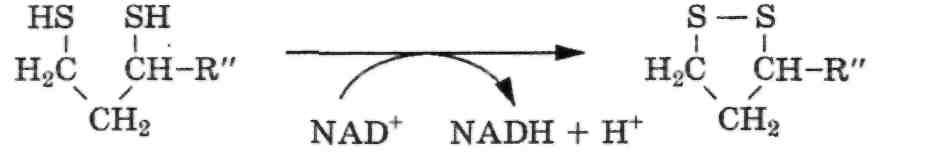
Все промежуточные продукты окислительного декарбоксилирования пирувата прочно связываются с комплексом. Скорость их превращения весьма тонко регулируется: она подавляется АТР и NADHи возрастает в присутствииADPиNAD+.
