
Уравнение Шредингера.
В
классической механике основной задачей
является нахождение ускорения тела в
любой момент времени а (t),
если известны все силы F(t),
действующие на тело:
![]()
В
квантовой механике основная задача
ставится совершенно иначе. Требуется
найти некоторую волновую функцию
Ψ(x,y,z),
если известно для квантовой частицы, в
каком силовом поле она находится.
Уравнение для волновой функции Ψ(x,y,z)
и называется уравнением Шредингера:
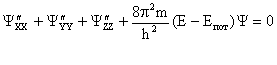 .
.
Это
дифференциальное уравнение второго
порядка в частных производных. Здесь:
![]()
![]() -
вторая производная от волновой функции
-
вторая производная от волновой функции
![]() по аргументу – координате Х (аналогично
по аргументу – координате Х (аналогично
![]() - частные производные по другим
пространственным координатам), m-
масса частицы, Е - её полная энергия,
- частные производные по другим
пространственным координатам), m-
масса частицы, Е - её полная энергия,
![]() -
потенциальная энергия квантовой частицы.
Для электрона в атоме Епот
= -к * Q
/ r
, где к = 9*109
Н*м2/Кл2
- коэффициент пропорциональности в
законе Кулона, Q
- заряд ядра атома, r
- расстояние от ядра. На рис.1 приведен
график зависимости потенциальной
энергии электрона в атоме от расстояния
до ядра.
-
потенциальная энергия квантовой частицы.
Для электрона в атоме Епот
= -к * Q
/ r
, где к = 9*109
Н*м2/Кл2
- коэффициент пропорциональности в
законе Кулона, Q
- заряд ядра атома, r
- расстояние от ядра. На рис.1 приведен
график зависимости потенциальной
энергии электрона в атоме от расстояния
до ядра.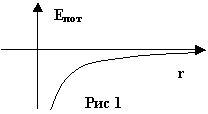
Упрощения.
а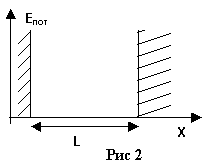 )
Будем рассматривать только одномерный
случай (движение только вдоль оси Х).
Тогда уравнение упрощается:
)
Будем рассматривать только одномерный
случай (движение только вдоль оси Х).
Тогда уравнение упрощается:
![]()
(это уже обыкновенное дифференциальное уравнение)
б)
электрон может находиться в ограниченной
области 0
![]() .
Характер зависимости
.
Характер зависимости
![]() при
этом заменяется «прямоугольной ямой»
с бесконечными стенками. Внутри «ямы»
при
этом заменяется «прямоугольной ямой»
с бесконечными стенками. Внутри «ямы»
![]() ,
вне «ямы» -
,
вне «ямы» -
![]() 1[1].
1[1].
Тогда уравнение Шредингера сводится к дифференциальному уравнению:
![]()
Запись
![]() означает, что волновая функция является
функцией, зависящей, от координаты Х.
Точно такое же по структуре уравнение
было рассмотрено для гармонических
колебаний:
означает, что волновая функция является
функцией, зависящей, от координаты Х.
Точно такое же по структуре уравнение
было рассмотрено для гармонических
колебаний:
![]()
Поэтому
по аналогии с уравнением гармонических
колебаний, для которого решением
являлась гармоническая функция:
![]() запишем
общее решение для уравнения Шредингера:
запишем
общее решение для уравнения Шредингера:
![]() , где
, где
![]()
![]() и
и
![]() -
это так называемые постоянные
интегрирования. Их следует найти из
граничных условий:
-
это так называемые постоянные
интегрирования. Их следует найти из
граничных условий:
![]()
![]()
а)
![]() следовательно
следовательно
![]()
Отсюда
![]()
б)
![]()
Отсюда
при
![]() :
:
![]() или
или
![]() ,
или
,
или
![]()
Так
как
![]() ,
то
,
то
![]()
Таким образом, получается условие квантования энергий электрона в атоме.
![]()
![]() ,где n
- главное квантовое число.
,где n
- главное квантовое число.
Вывод: В отличие от теории Бора полученные условия квантования энергий не требует введения каких либо дополнительных постулатов.
Анализ решения
1).
Если подставить в формулу все значения
при L
= 0,1 м расстояние между уровнями (Е2
- Е1)
равно 10-37Дж
![]() 10-16эВ.
Такие разности энергий мы просто не
воспринимаем и макромир для нас ощущается
не дискретным, а непрерывным.
10-16эВ.
Такие разности энергий мы просто не
воспринимаем и макромир для нас ощущается
не дискретным, а непрерывным.
2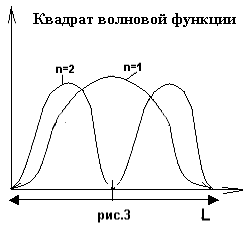 ).
При L=10-10
м аналогично
получается Е2
- Е1
4
эВ. Это значение примерно соответствует
энергии фотонов видимого света. И мы
отчетливо можем различать такие энергии
и тем самым можем «отразить» дискретную
природу микромира.
).
При L=10-10
м аналогично
получается Е2
- Е1
4
эВ. Это значение примерно соответствует
энергии фотонов видимого света. И мы
отчетливо можем различать такие энергии
и тем самым можем «отразить» дискретную
природу микромира.
3).
Вид волновой функции:
![]() .
Квадрат волновой функции, умноженный
на приращение ∆х |
.
Квадрат волновой функции, умноженный
на приращение ∆х |
![]() *∆х|
- характеризует вероятность нахождения
частицы в области ∆х. Приведенный на
рисунке 3 график представляет характер
распределения электронов в потенциальной
яме при различных значениях главного
квантового числа n.
Значение L/2
соответствует по теории Бора первому
Боровскому радиусу.
*∆х|
- характеризует вероятность нахождения
частицы в области ∆х. Приведенный на
рисунке 3 график представляет характер
распределения электронов в потенциальной
яме при различных значениях главного
квантового числа n.
Значение L/2
соответствует по теории Бора первому
Боровскому радиусу.
