
- •Под редакцией в.В. Колпаковой
- •I. Органические соединения азота
- •Нитросоединения
- •2). Реакции, связанные с подвижностью α-атомов водорода.
- •3). Реакции с минеральными кислотами.
- •3. Перегруппировка амидов карбоновых кислот по Гофману:
- •Физические свойства
- •2. Алкилирование аминов.
- •Реакции аминов с азотистой кислотой.
- •В случае взаимодействия n,n-диметиламинобензола с азотистой кислотой механизм реакции выглядит следующим образом:
- •Реакции аминов с карбонильными соединениями.
- •Изонитрильная проба.
- •Синтезы на основе свойств солей диазония
- •Соли диазония.
- •II. Органические соединения серы введение
- •Соединения двухвалентной серы тиоспирты
- •Синтетические способы получения
- •Физические свойства
- •Химические свойства
- •Сульфиды
- •Способы получения
- •Химические свойства сульфокислот и их функциональных производных
- •Эфиры серной кислоты
- •Контрольные вопросы
- •11.1 Синтез и реакции меркаптанов (тиоспирты)
- •11.2 Способы получения и химические свойства ароматических сульфокислот
Химические свойства сульфокислот и их функциональных производных
1. Кислотные свойства.
Сульфокислоты по силе сравнимы с серной кислотой. При реакции с металлами, их оксидами и гидроксидами, а также с аммиаком и аминами образуют соли.
RSO3H + NaOH → RSO3Na + H2O
Соли сульфокислот, имеющие длинноцепочечный гидрофобный радикал, являются анионактивными поверхностно-активными веществами (АПАВ). Необходимым компонентом, практически, всех, выпускаемых в России стиральных порошков, является алкил-бензолсульфонат натрия RC6H4SO3Na (торговое название «сульфонол»).
Сплавление солей сульфокислот со щелочами – основной способ получения фенолов:
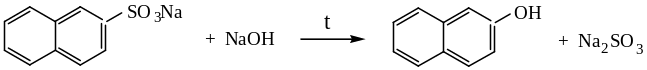
При сплавлении с цианидами образуются нитрилы:
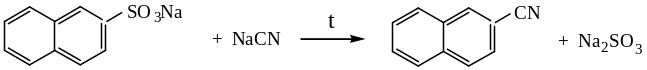
Хлорангидриды сульфокислот или сульфохлориды могут быть получены из сульфокислот действием пентахлорида фосфора:
CH3SO3H + PCl5 → CH3SO2Cl + POCl3 + HCl
метансульфохлорид
Однако обычно используют методы прямого сульфохлорирования углеводородов, различные для алифатических и ароматических соединений:
CH3CH2CH2CH3 + SO2 + Cl2 → CH3CH2CH – SO2Cl + HCl
│
CH3
бутан-2-сульфохлорид
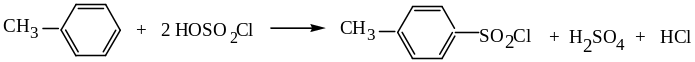
п-толуолсульфохлорид
Свойства сульфохлоридов подобны свойствам хлорангидридов карбоновых кислот. При взаимодействии со спиртами образуются эфиры сульфокислот, при реакции с аммиаком – амиды:
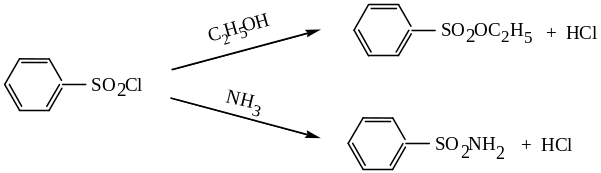
Эфиры сульфокислот – жидкости или твердые вещества. Они являются хорошими алкилирующими средствами:
 метилфенилсульфид
метилфенилсульфид
Амиды сульфокислот – кристаллические вещества, способные
растворяться в щелочах:
RSO2NH2 + NaOH → RSO2NHNa + H2O
Гипохлорит натрия замещает водород при азоте на атом хлора:
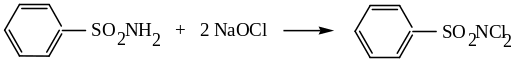
Бензолдихлорсульфамид (хлорамин Б) и подобное производное толуола (хлорамин Т) используются как мягкие дезинфектанты в медицине и пищевой промышленности.
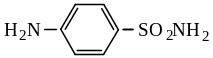
Простейшим лекарственным веществом большой группы сульфамидных препаратов является белый стрептоцид – п-амино-бензолсульфамид:
Отщепление воды от о-карбоксибензолсульфамида приводит к образованию имида, натриевое производное которого в 500 раз слаще сахара, не усваивается организмом и, практически, безвредно. Известно под названием сахарин.
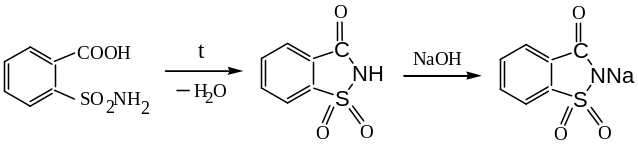
сахарин
4 При восстановлении сульфокислот образуются меркаптаны:
RSO3H + Zn + H2SO4 → RSH
5. При кипячении сульфокислот с водой отщепляется серная кислота. Эта реакция обратная сульфированию:
R – SO3H + H2O → R – H + H2SO4
6. Реакции ароматических сульфокислот по бензольному ядру.
Cульфогруппа как типичный заместитель-акцептор – ориентант II рода – дезактивирует ядро и направляет вновь вступающий заместитель в мета-положение.
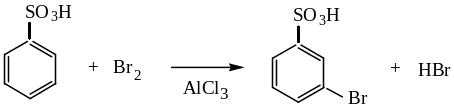
м-бромбензолсульфокислота
