
- •Под редакцией в.В. Колпаковой
- •I. Органические соединения азота
- •Нитросоединения
- •2). Реакции, связанные с подвижностью α-атомов водорода.
- •3). Реакции с минеральными кислотами.
- •3. Перегруппировка амидов карбоновых кислот по Гофману:
- •Физические свойства
- •2. Алкилирование аминов.
- •Реакции аминов с азотистой кислотой.
- •В случае взаимодействия n,n-диметиламинобензола с азотистой кислотой механизм реакции выглядит следующим образом:
- •Реакции аминов с карбонильными соединениями.
- •Изонитрильная проба.
- •Синтезы на основе свойств солей диазония
- •Соли диазония.
- •II. Органические соединения серы введение
- •Соединения двухвалентной серы тиоспирты
- •Синтетические способы получения
- •Физические свойства
- •Химические свойства
- •Сульфиды
- •Способы получения
- •Химические свойства сульфокислот и их функциональных производных
- •Эфиры серной кислоты
- •Контрольные вопросы
- •11.1 Синтез и реакции меркаптанов (тиоспирты)
- •11.2 Способы получения и химические свойства ароматических сульфокислот
3. Перегруппировка амидов карбоновых кислот по Гофману:
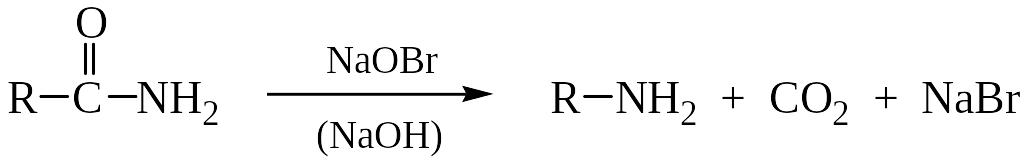
Механизм реакции состоит из следующих стадий:
а) галогенирование амида карбоновой кислоты
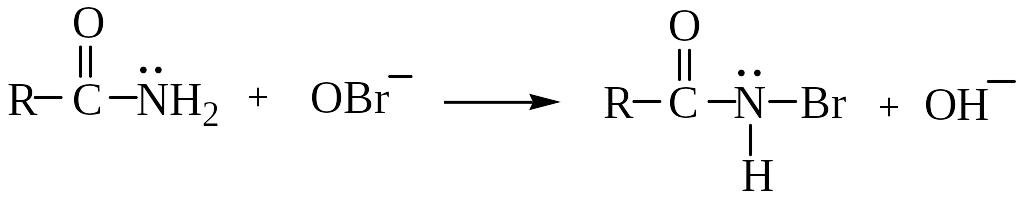
б) отрыв иона водорода гидроксил-ионом. Эта стадия облегчается электроноакцепторным влиянием атома брома, увеличивающим кислотность амида.
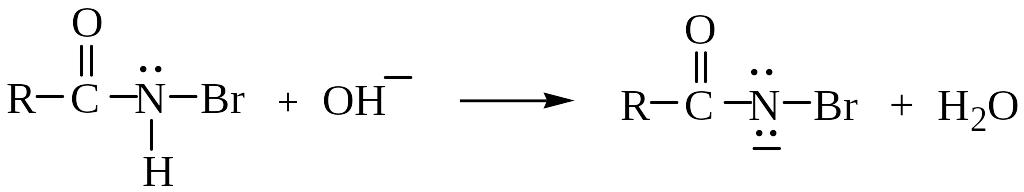
в) удаление аниона брома, приводящее к возникновению электронодефицитного атома азота и перегруппировка
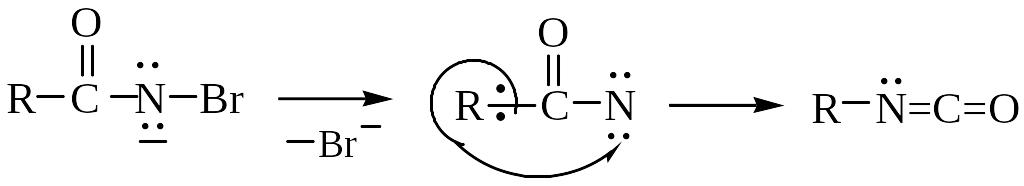
г) гидролиз изоцианата
![]()
По аналогичной схеме протекают перегруппировки азидов RCON3 (перегруппировка Курциуса) и гидрoксамовых кислот RCONHOH (перегруппировка Лоссена) в первичные амины.
4. Декарбоксилирование α-аминокислот имеет малое значение для химии, но широко распространено в биологических объектах.
При декарбоксилировании -аминокислот образуются биогенные амины, выполняющие в организме важные биологические функции. Так, получающийся при декарбоксилировании гистидина гистамин, в частности, имеет отношение к аллергическим реакциям организма.
R–CH–COOH ¾¾® R–CH2–NH2 + CO2
|
NH2
Химическое декарбоксилирование карбоновых кислот обычно протекает легко в том случае, если при -углеродном атоме имеется электроноакцепторный заместитель, поляризующий связь ССООН. В -аминокислотах такой группировкой служит +NH3-группа. Декарбоксилирование -аминокислот путь образования биогенных аминов. В живом организме этот процесс проходит под действием декарбоксилазы и пиридоксальфосфата. В лабораторных условиях реакцию осуществляют при нагревании -аминокислоты в присутствии поглотителей СО2, таких, как Ва(ОН)2. При декарбоксилировании -фенил--аланина, лизина, серина и гистидина образуются соответственно фенамин, 1,5диаминопентан (кадаверин), 2-аминоэтанол-1 (коламин) и триптамин.
Физические свойства
Метиламин, диметиламин, триметиламин и этиламин в обычных условиях – газы, следующие члены гомологического ряда – жидкости, с закономерно возрастающими температурами кипения. Низшие амины имеют неприятный запах, высшие запаха не имеют. Первичные и вторичные амины ассоциированы за счет образования водородных связей.
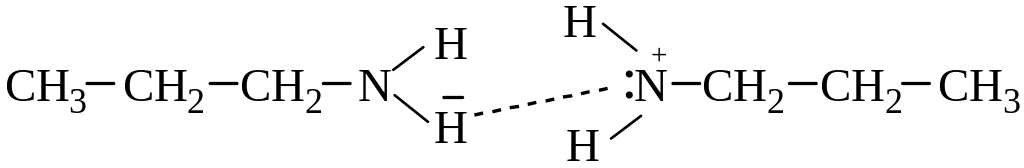
Ассоциация приводит к заметному повышению температур кипения по сравнению с соединениями с той же молекулярной массой, но не образующими водородных связей. Хорошая растворимость в воде низших аминов обусловлена образованием водородных связей с молекулами воды. Низшие амины хорошо растворимы в воде, но по мере увеличения углеводородного радикала их растворимость в воде резко уменьшается; высшие амины нерастворимы в воде.
Таблица 1. ФИЗИЧЕСКИЕ СВОЙСТВА АМИНОВ
Название |
формула |
Т.пл. / Т.кип. 0 С |
Кв |
Метиламин Диметиламин Триметиламин Этиламин Диэтиламин Триэтиламин Пропиламин Дипропиламин Трипропиламин Изопропиламин Бутиламин Изобутиламин Вторбутиламин третбутиламин Циклогексиламин Бензиламин α-Фенилэтиламин β-Фенилэтиламин Тетраметилендиамин Гексаметилендиамин Анилин N-Метиланилин N,N-Диметиланилин Дифениламин Трифениламин о-толуидин м-толуидин п-толуидин о-анизидин м-анизидин п-анизидин о-нитроанилин м-нитроанилин п-нитроанилин 2,4-динитроанилин 2,4,6-тринитроанилин о-фенилендиамин м-фенилендиамин п фенилендиамин Бензидин |
CH3NH2 (CH3)2NH (CH3)3N CH3CH2NH2 (CH3CH2)2NH (CH3CH2)3N CH3CH2CH2NH2 (CH3CH2CH2)2NH (CH3CH2CH2)3N (CH3)2CHNH2 CH3(CH2)3NH2 (CH3)2CHCH2NH2 CH3CH2CH(CH3)NH2 (CH3)3CNH2 С6H11NH2 С6H5CH2NH2 С6H5CH(CH3)NH2 С6H5CH2CH2NH2 H2N(CH2)4NH2 H2N(CH2)6NH2 С6H5NH2 С6H5NHСН3 С6H5N(СН3)2 (С6H5)2NH (С6H5)3N o-СН3С6Н4NН2 м-СН3С6Н4NН2 п-СН3С6Н4NН2 o-СН3ОС6Н4NН2 м-СН3ОС6Н4NН2 п-СН3ОС6Н4NН2 o-NО2С6Н4NН2 м- NО2С6Н4NН2 п-NO2С6Н4NН2 2,4-(NO2)2С6Н3NН2 2,4,6-(NO2)3С6Н2NН2 o-С6Н4(NН2)2 м-С6Н4(NН2)2 п-С6Н4(NН2)2 п -NН2С6Н4С6Н4NН2-п
|
- 92 / - 7,5 - 96 / 7,5 - 117 / 3 - 80 / 17 - 39 / 55 - 115 / 89 - 83 / 49 - 63 / 110 - 93 / 157 - 101 / 34 - 50 / 78 - 85 / 68 - 104 / 63 ─ / 134 - 67 / 4 ─ / 185 ─ / 187 / / 195 8 / 117 39 / 196 - 6 / 184 - 57 / 196 3 / 194 53 / 302 127 / 365 - 28 / 200 - 30 / 203 44 / 200 5 / 225 ─ / 251 57 / 244 71 / 284 114 / 307 (разл.) 148 / 332 187 / ─ 188 / ─ 104 / 251 63 / 287 142 / 267 127 / 401 |
4,4 . 10 -4 5,1 . 10 -4 0,6 . 10 -4 4,7 . 10 -4 9,5 . 10 -4 5,5 . 10 -4 3,8 . 10 -4 8,1 . 10 -4 4,5 . 10 -4
4,1 . 10 -4
0,23 . 10 -4
4,2 . 10 -10 7,1 . 10 -10 11 . 10 -10 0,7 . 10 -10
2,5 . 10 -10 4,9 . 10 -10 12 . 10 -10 3 . 10 -10 2 . 10 -10 15 . 10 -10 3,5 . 10 -14 3,2 . 10 -12 0,1 . 10 -12
3,3 . 10 -10 7,6 . 10 -10 11 . 10 -10 7,4 . 10 -13 |
Химические свойства
1. Основность аминов обусловлена способностью атомов азота присоединять протон к неподеленной паре электронов с образованием катионов аммонийного типа. Основность аминов измеряется константой равновесия реакции гидратации:
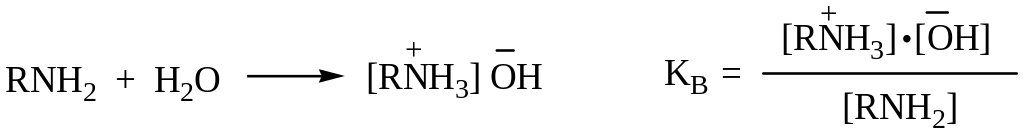
Основность амина тем выше, чем больше электронная плотность сосредоточена на атоме азота. Благодаря +I-эффекту алкильной группы алифатические амины (особенно третичные) имеют большую электрон- ную плотность на атоме N, чем аммиак, и следовательно, большую основность.
|
NH3 |
CH3NH2 |
C2H5NH2 |
(C2H5)2NH |
пиперидин
|
Кв
|
1,8 ·10-5 |
4,4 ·10-4 |
4,7 ·10-4 |
9,5 ·10-4 |
1,6 ·10-3 |
Ароматические амины вследствие сопряжения неподеленной пары электронов азота с -электронным облаком бензольного ядра являются более слабыми основаниями, причем этот эффект усиливается при введении в ароматическое кольцо электроноакцепторных группировок.
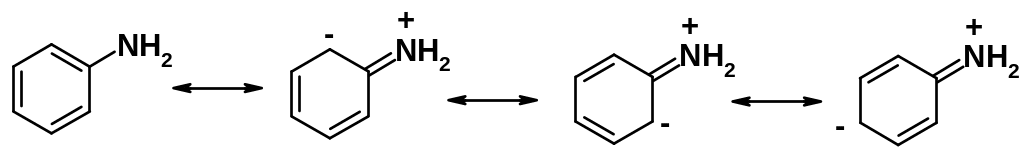
С увеличением объемов заместителей, окружающих реакционный центр вещества, возрастают пространственные препятствия для его атаки молекулой реагента. Это также относится и к протонированию аминов. В связи с этим амины, содержащие большие радикалы, проявляют более слабые основные свойства по сравнению с ожидаемыми при рассмотрении только электронных эффектов радикалов, окружающих атом азота.
