
- •Оглавление
- •1.Факторы, влияющие на растворимость газов.
- •2.Зависимость растворимости газа от температуры.
- •3.Факторы,влияющие на растворимость газов в жидкостях
- •4.Типы растворов жидкостей в жидкостях, причины их разнообразия.
- •5.Идеальные растворы. Построение их диаграммы «давление – состав», температура кипения – состав.
- •6.Вывод зависимости давления насыщенного пара смеси от состава жидкой и паровой фаз.
- •7. Реальные р-ры жидкостей неограниченно растворимые друг в друге. Причины отклонения давления паров над раствором от з-на Рауля.
- •8.Диаграммы давление –состав и температура – состав для реaльных растворов
- •9.Первый з-н Конавалова
- •10.Методы разделения смесей. Ректификация.
- •11. Диаграмма состояния р-ров ,образующих азеотропы.2й з-н Коновалова.
- •12.Диаграмма «давление – состав» и «температура – состав» Жидкости, ограниченно растворимых друг в друге.
- •13.Диаграммы “Давление-состав” и “температура-состав” для жидкостей, взаимно нерастворимых друг в друге.
- •14. Закон распределения Шилова-Нернста. Экстракция.
- •15. Трехкомпанентные системы. Графическое представление. Определение методами Розебома и Гиббса.
- •16.Диаграмма плавкости 2-х компонентных систем с огранич-ной растворимостью в твердом состоянии. Эвтектика.
- •17. Дифферинциальный термический анализ (дта)
- •18Диаграммы плавкости систем с конгруэнтно и инконгруэнтно плавящимися соединениями.
- •19.Проводимость в газах, жидкостях и твердых телах. Электропроводность удельная и эквивалентная. Основные полож-я теории сильных эл-тов. Термодтнамика р-ров сильных эл-тов.
- •20. Скорость движ-ния иона,абсолютная ск-сть движ-я иона,подвижность.
- •21. Вывод уравнения, связывающего эквивалентную электропроводность с подвижностями ионов.
- •23.Влияние различных факторов на электропроводность для р-ров сильных электролитов.
- •24.Уравнение Кольрауша для слабых и сильных электролитов. Числа переноса.
- •25. Ионная сила р-ра. Ионный радиус, ионная атмосфера. Электрофоретическое и релаксационное торможение. Эффект Вина,понятие дисперсии электропроводности.
- •26. Активности и коэффициенты активности электролитов. Вычисление средних коэффициентов активности ионов.
- •27. Кондуктометрическое титрование как метод определения точки эквивалентности при титровании, изменения состава растворов для расчета степени диссоциации, констант диссоциации.
- •28. Понятие об электродвижущих силах, полуэлементе, элементе. Термодинамический вывод уравнения для определения электродного потенциала, уравнение Нернста.
- •29. Термодинамика гальванических элементов.
- •30. Водородный скачок потенциала. Стандартные электродные потенциалы.
- •31. Виды гальванических элементов. Электроды 1-го и 2-го рода. Обратимые, необратимые цепи. Знаки эдс-элементов. Вычисление эдс обратимого гальванического элемента.
- •32. Окислительно-восстановительные электроды или редокс-элементы.
- •33. Химические цепи. Уравнение для расчета эдс.
- •34. Концентрационные цепи. Уравнение для расчета эдс
- •35. Диффузионный скачок потенциала.
- •36. Потенциометрическое титрование. Электрохимические методы определения рН растворов.
- •37. Основные понятия химической кинетики: молекулярность, скорость реакции (начальная, истинная и средняя), константа скорости.
- •38. Вывести уравнение Аррениуса. Энергия активации. Предэкспоненциальный множитель. Методы их определения.
- •39. Порядок реакции по реагенту и методы его экспериментального определения. Лимитирующая стадия химического процесса.
- •40. Вывод интегрального кинетического уравнения для необратимой и обратимой реакции первого порядка.
- •41. Вывод интегрального кинетического уравнения для необратимой реакции второго порядка.
- •42. Вывести уравнение кинетики для параллельных реакций.
- •43. Вывести уравнение кинетики для гомогенной необратимой последовательной реакции первого порядка
- •44. Вывести уравнение скорости процесса в потоке, режим идеального вытеснения в стационарных условиях.
- •45. Кинетика гомогенных реакций первого порядка, протекающих в условиях идеального перемешивания.
- •46. Теория активных соударений и расчет скорости по числу соударений.
- •47. Теория переходного состояния и вывод основного уравнения.
- •48. Связь константы скорости реакции с энтальпией и энтропией активации.
- •49.Цепные р-ии, основные понятия, основные стадии и типы р-ий.
- •50.Кинетика р-ий с неразветвленными цепями.
- •51.Вывод кинетических уравнений цепных р-ий в стационарном приближении
- •52.Пределы воспламенения и взрыва. Механизмы вопламенения.
- •53. Связь кинетики и макрокинетики при протекании экзотермических реакций (теория теплового взрыва)
- •54. Законы и кинетика фотохимических р-ий. Примеры р-ий с различным квантовым выходом. Сенсибилизированные р-ии.
- •55.Особенности кинетики р-ий в р-рах. Влияние природы р-рителя на скорость процесса, ур-ие Бренстеда.
- •56. Влияние ионной силы и давления на кинетику реакций в растворе.
- •57.Основные признаки катализа.
- •58.Общий и специфич. Кислотно-основ.Катализ.
- •59.Катализ комплексами переходных металлов и ферментатив.Катализ.
- •60.Кинетика гомогенных катал. Р-ций
- •61. Гетерогенный катализ. Понятие о катализаторах, носителях и промоторах..
- •62.Области протекания гетероген.Катал.Р-ций.
- •63.Температурная зависимость наблюдаемой скорости реакции
- •66.Кинетика гетерогенных каталитических реакций, проводимых в реакторе идеального вытеснения.
- •68.Основные теории катализа: мультиплетная, ансамблей, электронная, радикальная.
- •69. Основные принципы твердых катализаторов.
- •70.Топохимические реакции.
40. Вывод интегрального кинетического уравнения для необратимой и обратимой реакции первого порядка.
Необратимая:
а) А B (+ D) (R2),
протекающей с некой константой скорости k1 при постоянном объеме. При анализе удобно пользоваться безразмерной концентрацией αi = Сi/C(0) Запишем скорость реакции по убыли реагента А, а также в соответствии с первым постулатом кинетики (ППК)
r1 = -dCA/dt = k1CA (1.22)
С учетом начального условия, при t =0, C= C(0) и α=1, интеграл имеет вид:
![]() (1.23)
(1.23)
Откуда найдем:
α = exp(-k.t) или lnα = -k.t (1.24)
Время полупревращения, t0,5 найдем из условия α = 0,5, тогда
![]() (1.25).
(1.25).
Проверка применимости (1.23 или 1.24) выполняется путем представления экспериментальных данных в линеаризующих координатах этого уравнения, т.е. «lnα – t», при этом тангенс угла наклона полученной прямой, проходящей через начало координат (0;0), численно равен константе скорости реакции.
-lnα
|
Рис. 8. Определение константы скорости реакции (R2) по экспериментальным данным ( ○ ), представленным в координатах уравнения (1.23): tg = k |
А→В
![]() - концентрация в-ва А в момент времени
t, V объём
системы
- концентрация в-ва А в момент времени
t, V объём
системы
![]()
![]()
![]()
![]()
если t=0, x=0, то
![]()
![]()
![]() ,
c0 - исходная
концентрация, с - концентрация к моменту
времени t
,
c0 - исходная
концентрация, с - концентрация к моменту
времени t
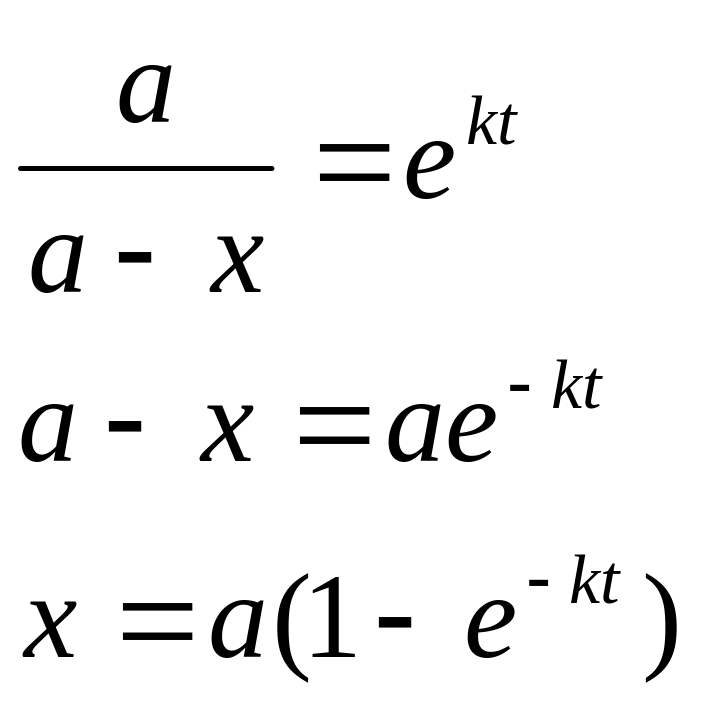
время полураспада х=а-х
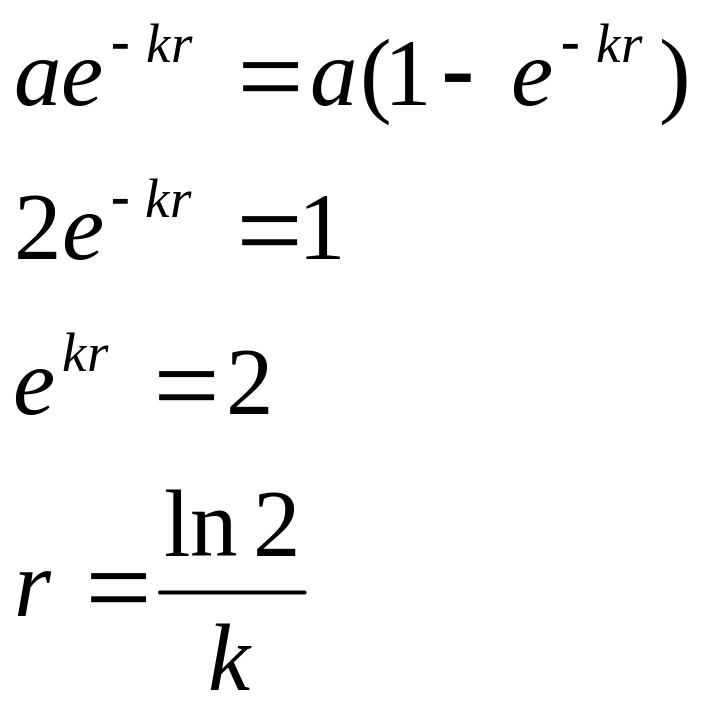 время
полураспада не зависит от количества
исходного вещ-ва
время
полураспада не зависит от количества
исходного вещ-ва
Обратимая:
k1
б) А В (R4)
k2
dCA/dt = -k1CA + k2CB (1.27)
-dCA/dt = k1CA + k2 (C(0) –CA) (1.28)
-k2 dt = dα/((1+К)α – 1), при t=0, α = 1 (1.29)
-k2 t = 1/(1+К) •ln{(1+К)α - 1} (1.30)
α = 1/(1+К) + К•exp(-k12t)/(1+К) (1.31)
поскольку α + β = 1, определим безразмерную концентрацию продукта β:
β = К/(1+К) – К•exp(-k12t)/(1+К) (1.31а)
Таким образом, равновесный выход продукта реакции 1го порядка определяется только константой равновесия
y(B)eq = βt ∞ = К/(1+К) (1.32)
Следовательно, в случае протекания обратимой реакции типа (R4) можно определить константу равновесия по экспериментальному значению максимального выхода продукта:
К = βeq/(1-βeq) (1.33)
A k1↔k2 B
![]()
Принцип независимости: если в системе одновременно протекает несколько реакций, то каждая из них независима от остальных и скорость её прямо пропорциональна концентрации реагирующих веществ.
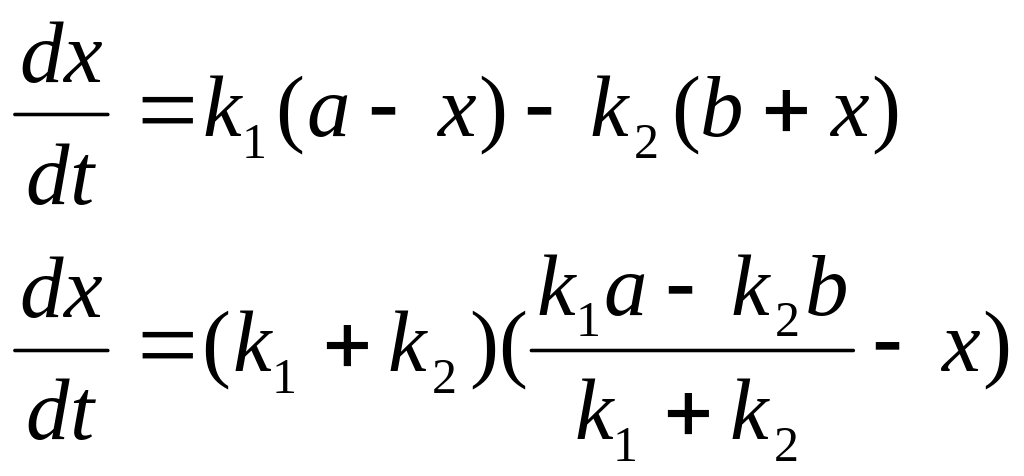
Пусть
![]()
тогда
![]()
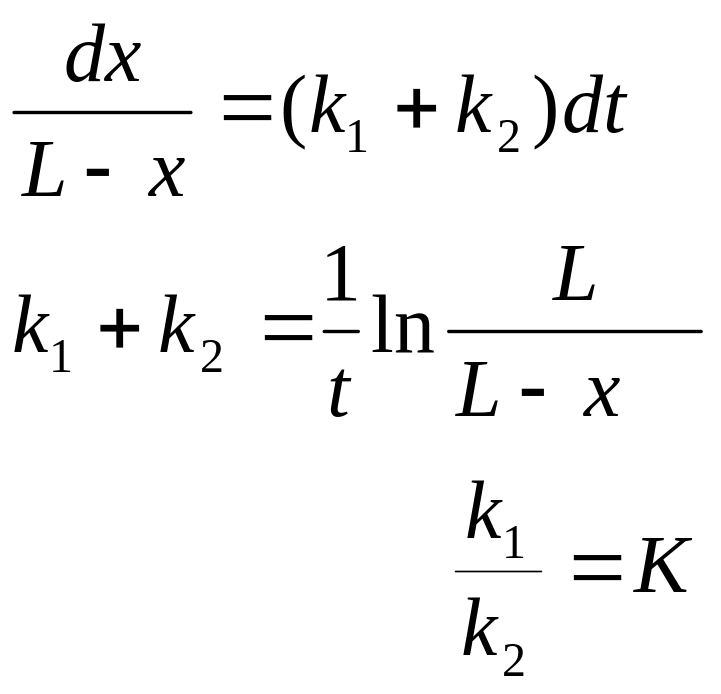
где К – константа равновесия
![]()
в момент равновесия
![]() тогда
тогда
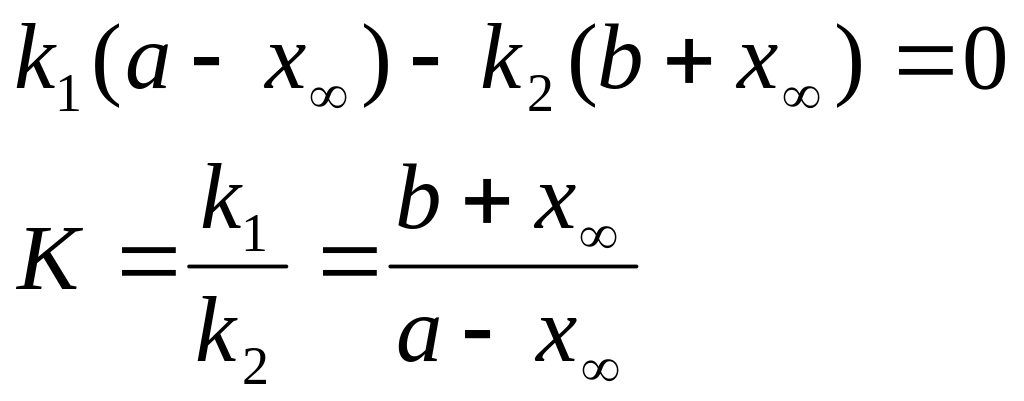
где х∞ - кол-во вещ-ва А, прореагировавшего к моменту равновесия
Если считать как необратимую , то
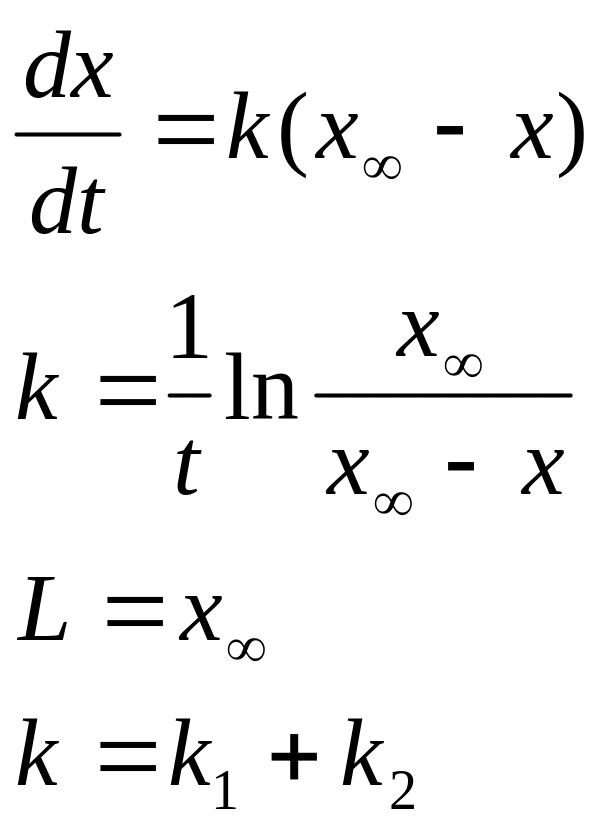
41. Вывод интегрального кинетического уравнения для необратимой реакции второго порядка.
A + B D (R3)
Запишем ее скорость по убыли реагента А, а также в соответствии с первым постулатом кинетики.
r1 = -dCA/dt = -k1CACB (1.26)
Положим для упрощения, что начальные концентрации [A] и [B] равны C(0)*.
{В случае других значений решение кинетического уравнения не изменится, но уравнение будет содержать параметр µ, учитывающий молярное соотношение реагентов}
Тогда уравнение (1.26) примет вид:
- dC/C2 = k1.dt, при t=0, C= C(0) (1.27)
решение которого имеет вид:
![]() или
или
![]() (1.28)
(1.28)
А+В→С+D+…
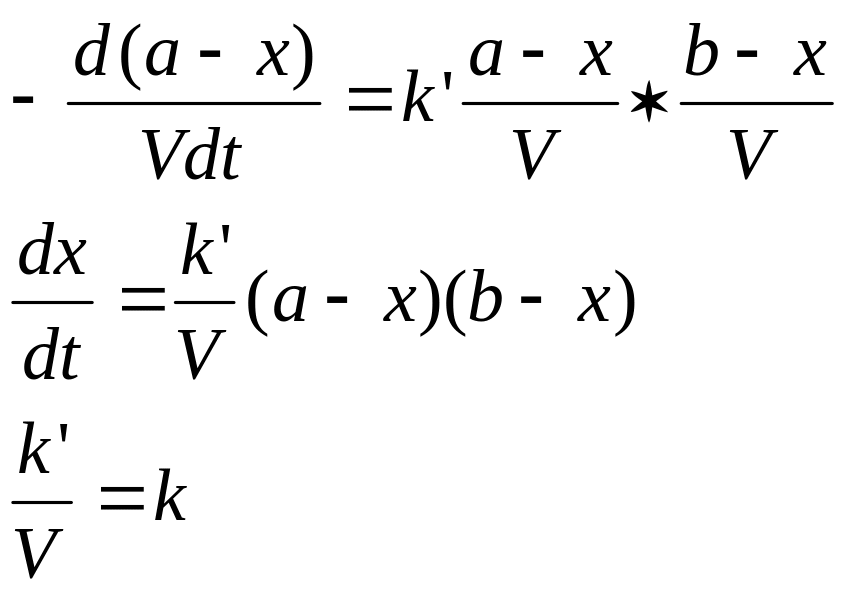 если
V=const, то
если
V=const, то
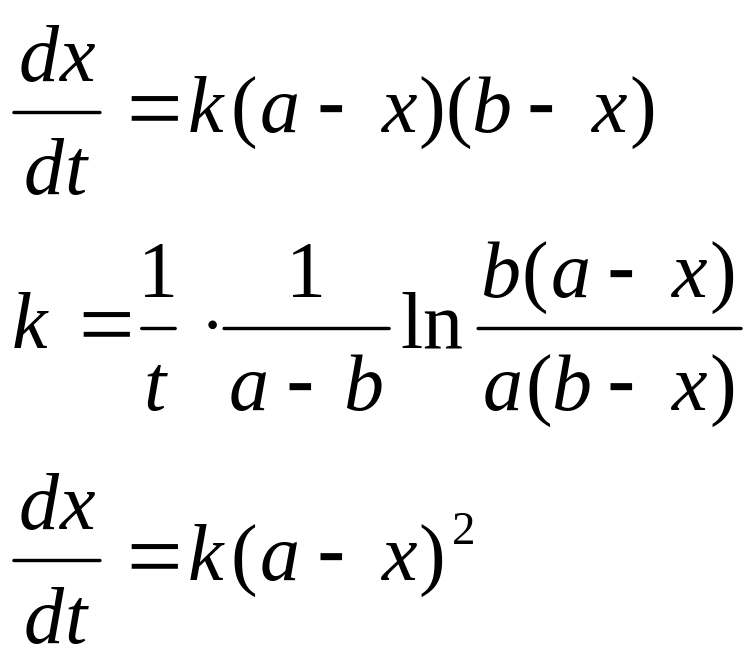 если a=b, то
если a=b, то
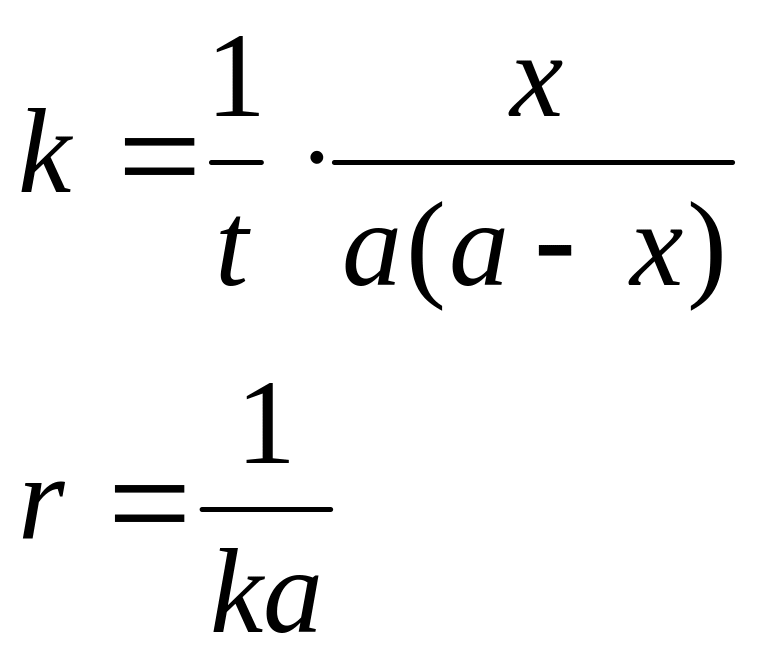 время полураспада обратно пропорционально
кол-ву исх.вещ-ва
время полураспада обратно пропорционально
кол-ву исх.вещ-ва


 t
t