
- •16. Закон Гесса. Второй закон термодинамики.
- •17. Энергия Гиббса (изобарно- изотермический потенциал ), стандартное значение энергии Гиббса.
- •37. Распространение элементов в земной коре и организмах. Биогенные элементы. Классификация элементов.
- •38.Общая характеристика элементов 7 группы.
- •39.Галогены. Физические и химические свойства. Биологическая роль.
- •40. Сравнительная характеристика водородных соединений галогенов.
- •41.Кислородные соединения галогенов.
- •42. Общая характеристика 6 группы.
- •43.Халькогены. Физические и химические свойства. Биологическая роль.
- •44.Сравнительная характеристика водородных соединений халькогенов.
- •45. Кислородные соединения халькогенов. Серная кислота, ее свойства.
- •46. Общая характеристика элементов 5 группы. Биологическая роль.
- •47. Водородные соединения элементов 5 группы. Аммиак . Строение молекулы.
17. Энергия Гиббса (изобарно- изотермический потенциал ), стандартное значение энергии Гиббса.
|
Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на принципиальную возможность протекания химической реакции; это термодинамический потенциал следующего вида:
![]()
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)
Понятие энергии Гиббса широко используется в термодинамике и химии.
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста ее энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж)
В химических процессах одновременно действуют два противоположных фактора — энтропийный (TΔS) и энтальпийный (ΔH). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (G):
![]()
Из
этого выражения следует, что
![]() ,
то есть некоторое количество
теплоты
расходуется на увеличение энтропии
(TΔS),
эта часть энергии потеряна для совершения
полезной работы,
её часто называют связанной
энергией.
Другая часть теплоты (ΔG)
может быть использована для совершения
работы, поэтому энергию Гиббса часто
называют также свободной
энергией.
,
то есть некоторое количество
теплоты
расходуется на увеличение энтропии
(TΔS),
эта часть энергии потеряна для совершения
полезной работы,
её часто называют связанной
энергией.
Другая часть теплоты (ΔG)
может быть использована для совершения
работы, поэтому энергию Гиббса часто
называют также свободной
энергией.
Характер изменения энергии Гиббса позволяет судить о принципиальной возможности осуществления процесса. При ΔG < 0 процесс может протекать, при ΔG > 0 процесс протекать не может (иными словами, если энергия Гиббса в исходном состоянии системы больше, чем в конечном, то процесс принципиально может протекать, если наоборот — то не может). Если же ΔG = 0, то система находится в состоянии химического равновесия.
Обратите внимание, что речь идёт исключительно о принципиальной возможности протекания реакции. В реальных же условиях реакция может не начинаться и при соблюдении неравенства ΔG < 0 (по кинетическим причинам).
Существует
полезное соотношение, связывающее
изменение свободной энергии Гиббса
![]() в
ходе химической реакции с её константой
равновесия
в
ходе химической реакции с её константой
равновесия
![]() :
:
![]()
Вообще говоря, любая реакция может быть рассмотрена как обратимая (даже если на практике она таковой не является). При этом константа равновесия определяется как
![]()
где
![]() —
константа
скорости
прямой реакции,
—
константа
скорости
прямой реакции,
![]() —
константа скорости обратной реакции.
—
константа скорости обратной реакции.
36.ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ КОМПЛЕКСНЫХ СОЕДИНЕНИЙ. Константа нестойкости и константа устойчивости.
В растворах КС имеет место первичная и вторичная диссоциация (в расплавах КС происходит их термическая диссоциация). Первичная диссоциация протекает по типу сильных электролитов - практически необратимо:
K4[Fe(CN)6] 4K+ + [Fe(CN)6]4-
[Co(NH3)6]Cl3 [Co(NH3)6]3+ + 3Cl-
Первичной диссоциации не подвергаются комплексы без внешней сферы: [Pt(NH3)2Cl2], [Co(NH3)3(NO3)3].
Вторичная диссоциация характеризует диссоциацию самого комплекса. Она протекает в незначительной степени, подчиняется закону действия масс. Этот процесс характеризуют константой диссоциации. Так как величина этой константы фактически определяет прочность комплекса, то ее обычно называют константой нестойкости (K ). Вторичная диссоциация протекает по типу слабого электролита - обратимо и ступенчато:
[Ag(NH3)2]+ [Ag(NH3)]+ + NH3
[Ag(NH3)]+ Ag+ + NH3
В целях упрощения формы записи обычно записывают суммарное уравнение вторичной диссоциации:
[Ag(NH3)2] Ag+ + 2NH3
Выражение константы нестойкости имеет вид:
![]()
Общая константа нестойкости комплекса равна произведению констант диссоциации по всем ступеням:
![]()
Величину, обратную константе нестойкости, называют константой устойчивости (n).
Значения констант нестойкости, приводимые в справочниках, используют для характеристики устойчивости комплексов, нахождения концентраций частиц (комплекса, комплексообразователя, лигандов) в растворе КС, для определения направленности химических реакций с участием комплексных соединений и др. Например, равновесие в реакции:
[Ag(NH3)2]Cl + 2KCN = K[Ag(CN)2] + 2KCl + 2NH3
будет смещено вправо, так как Kнест.([Ag(NH3)2]+) = 9,3·10-8, а Kнест.([Ag(CN)2]-) = 8,0·10-22, т.е. второй комплексный ион значительно прочнее первого:
![]()
Прочность комплексного иона характеризуется его константой диссоциации, называемой константой нестойкости. Для записи константы нестойкости К уравнение диссоциации составляется обычным способом (без участия молекул воды):

Аналогично составляются выражения для К3, К4, К5, К6, в которых квадратными скобками обозначены равновесные концентрации ионов.
Если справочные данные по ступенчатым константам нестойкости отсутствуют, пользуются общей константой нестойкости комплексного иона:
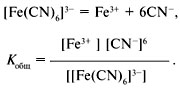
Общая константа нестойкости равна произведению ступенчатых констант нестойкости.
В аналитической химии вместо констант нестойкости в последнее время пользуются константами устойчивости комплексного иона:
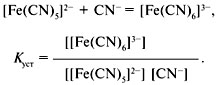
Константа устойчивости относится к процессу образования комплексного иона и равна обратной величине константы нестойкости:
Куст = 1/Кнест.
Константа устойчивости характеризует равновесие образования комплекса.
Константы нестойкости или константы устойчивости определяются различными физико-химическими методами. Использование химических методов затруднено, т.к. измерение равновесных концентраций веществ часто приводит к смещению равновесия.
Например, если вы захотите определить константу нестойкости иона [Pt(NH3)4Cl2]2+, диссоциирующего по уравнению:
[Pt(NH3)4Cl2]2+ = [Pt(NH3)4Cl]3+ + Сl–,
измеряя равновесную концентрацию свободных хлорид-ионов в растворе осаждением их при приливании раствора нитрата серебра, то начнется диссоциация иона [Pt(NH3)4Cl]3+:
[Pt(NH3)4Cl]3+ = [Pt(NH3)4]4+ + Сl–.
Поэтому измеренное количество образовавшегося хлорида серебра не будет соответствовать количеству хлорид-ионов, образующихся при равновесии с ионом [Pt(NH3)4Cl]3+.
