
Перегонка
Перегонка (дистилляция) – это процесс, в ходе которого перегоняемое вещество нагревают до кипения, образовавшийся пар отводят и конденсируют в виде дистиллята. Разделение смеси путем перегонки основано на различии состава жидкости и пара.
Этот метод применим при условии термической устойчивости перегоняемого вещества, т.е. вещество не должно разлагаться в процессе перегонки.
С помощью перегонки можно:
– разделить смесь жидкостей с различными температурами кипения;
– отделить жидкое вещество от растворенных в нем твердых или смолообразных примесей;
– отогнать летучий растворитель от очищаемого вещества.
В зависимости от свойств разделяемых веществ перегонку проводят в различных условиях:
– при атмосферном давлении;
– в вакууме;
– с водяным паром.
Исходя из различий в температурах кипения компонентов смеси, применяют простую (прямоточную) или фракционную (противоточную) перегонку, как при атмосферном давлении, так и в вакууме.
Простая перегонка при атмосферном давлении
Простая перегонка широко применяется для отгонки органических растворителей от нелетучих примесей или разделения смеси жидких веществ, сильно отличающихся друг от друга по своим температурам кипения. Удовлетворительное разделение возможно при условии, что разница в температурах кипения перегоняемых жидкостей составляет не менее 80°С.
На рис. 3.1 представлен прибор для простой перегонки, состоящий из перегонной колбы 1, насадки Вюрца, снабженной термометром 2, холодильника 3, аллонжа 4, приемникам 5, электроплитки 6, штативов 7 и лапок 8.
При простой перегонке пары кипящей жидкости из перегонной колбы поступают в холодильник, где превращаются в конденсат. В этом процессе пары и конденсат перемещаются в одном направлении, поэтому такую перегонку называют прямоточной. Разделение смеси жидкостей может происходить только на стадии испарения.
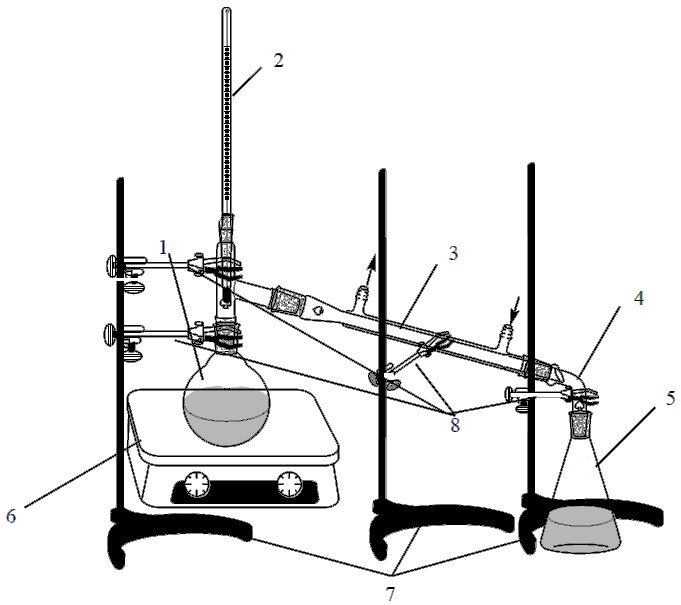
Рис.3.1. Установка для простейшей перегонки
Техника эксперимента.
Помещённую в колбу 1 жидкость (рис. 3.1) нагревают до кипения, используя в качестве источника тепла один из видов жидкостных бань (водяная, масляная, металлическая или воздушная), для равномерного нагрева и во избежание перегрева. Выбор нагревательного прибора зависит от температуры кипения перегоняемой жидкости, её горючести и взрывоопасности. Температура бани не должна превышать температуру перегоняемого вещества более чем на 25-30 °С. Пары поднимаются в насадку Вюрца и омывают шарик термометра (2), с помощью которого следят за температурой паров. Термометр 2 должен быть установлен таким образом, чтобы верхний край ртутного шарика располагался на одном уровне с нижним краем отверстия отводной трубки в шейке насадки Вюрца, где он полностью омывается парами перегоняемого вещества. Затем пары попадают в холодильник Либиха(3), из которого конденсат через алонж (4) стекает в приёмник (5).
Экстракция
Экстракцией (или извлечением) называется процесс разделения смеси веществ, основанный на различной способности компонентов смеси распределяться между двумя несмешивающимися фазами: «жидкость – жидкость», «твёрдое вещество – жидкость». Экстракция заключается в переводе вещества из одной фазы (жидкой или твёрдой) в другую жидкую фазу, называемую экстрагентом.
К экстрагентам предъявляются следующие требования:
– растворимость экстрагируемого вещества в выбранном экстрагенте должна быть высокой;
– экстрагент и экстрагируемая жидкость (в случае экстракции в системе «жидкость-жидкость») должны различаться по плотности.
Экстракция соединений из растворов (большей частью из водных) является очень важной и одной из обязательных операций в органической химии. При экстрагировании веществ из раствора распределение вещества между двумя жидкими фазами, определяется законом распределения Нернста:
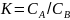
где:
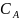 – концентрация вещества в фазе А,
– концентрация вещества в фазе А,
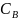 – концентрация вещества в фазе B.
– концентрация вещества в фазе B.
В состоянии равновесия отношение концентраций и вещества, которое растворено в двух несмешивающихся фазах А (экстрагент) и В (экстрагируемая жидкость), при определённой температуре является постоянной величиной К (коэффициент распределения). В приведённой форме закон Нернста применим только для небольших концентраций (идеальные условия) и в тех случаях, когда растворённое соединение имеет в обеих фазах одинаковую степень ассоциации.
Экстракция
легко осуществима, если коэффициент
распределения
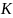 значительно
больше единицы, т.е. растворимость
данного соединения в экстрагенте гораздо
выше, чем в фазе исходного растворителя.
значительно
больше единицы, т.е. растворимость
данного соединения в экстрагенте гораздо
выше, чем в фазе исходного растворителя.
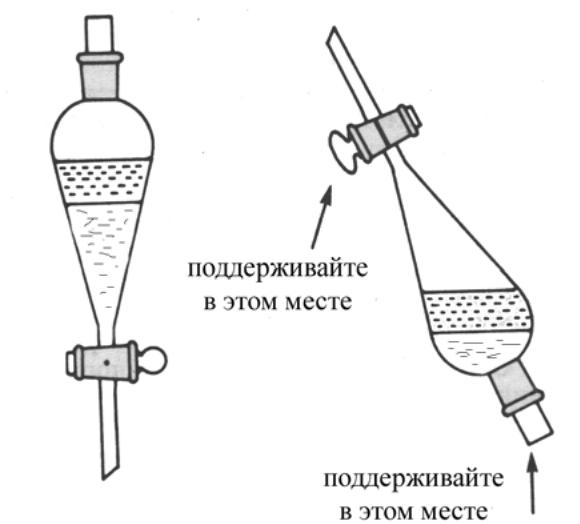
Рис.4.1. Делительная воронка
