
- •1. Технологический процесс. Основные понятия. Технологическая схема. Технологический режим. Виды технологических процессов. Периодический, непрерывный, комбинированный.
- •2. Классификация процессов разделения и очистки. Стадии очистки. Выбор метода.
- •3. Сорбционные методы очистки. Процесс очистки адсорбцией. Ионный обмен. Хроматография.
- •1. Адсорбционный метод.
- •4. Жидкостная экстракция (жэ).
- •5. Кристаллизационные процессы очистки.
- •6. Эффективность – кристаллизационных процессов очистки. Коэффициенты распределения (равновесный, эффективный)
- •7. Метод перегонки через газовую фазу. Сублимация и дистилляция.
- •8. Ректификация. Ректификационная колонна.
- •9. Очистка веществ с помощью химических-транспортных реакций.
- •10. Электрохимические процессы разделения и очистки. Электролиз. Катодное растворение. Электродиализ.
- •11. Очистка в центробежном поле. Разделение в скрещенных электрическом и магнитном полях. Разделение диффузией и термодиффузией.
- •12. Основные процессы – гетерогенных химико-технологических систем. Процессы массопередачи. Процессы теплопередачи.
- •Процесс теплопередачи:
- •13. Физико-химические основы процессов затвердевания. Основные модели роста кристаллов. Виды эпитаксии.
4. Жидкостная экстракция (жэ).
Экстракция –процесс избирательного извлечения вещества в жидкую фазу.
Абсорбция - экстракция газа жидкостью в объеме.
Выщелачивание – экстракция твердых веществ жидкостями.
Жидкостная экстракция (ЖЭ) – экстракция растворимого вещества из 1 жидкой фазы в другую.
При ЖЭ происходит процесс извлечения растворимого вещества из 1-го жид. Растворителя с помощью другого, причем растворители не должны смешиваться друг с другом.
Экстрагент – жидкость, с помощью которой проводят экстрагирования. Он может состоять растворителя, но и содержит растворитель, в котором есть реагент, который химически реагировать с извлекаемым веществом. Иногда в состав водного растворителя, из любой экстрагирует вещество вводят высаливатель – это вещество, которое имеет одноименный ион с извлекаемом веществом и уменьш. его растворимость.
Методы использования для:
1. разделения смеси 2-х веществ с концентрацией любой из них в разных растворителях.
2.экстрагирования основного компонента смеси в органический растворитель и оставления примеси в водном растворителе и наоборот.
Механизм:
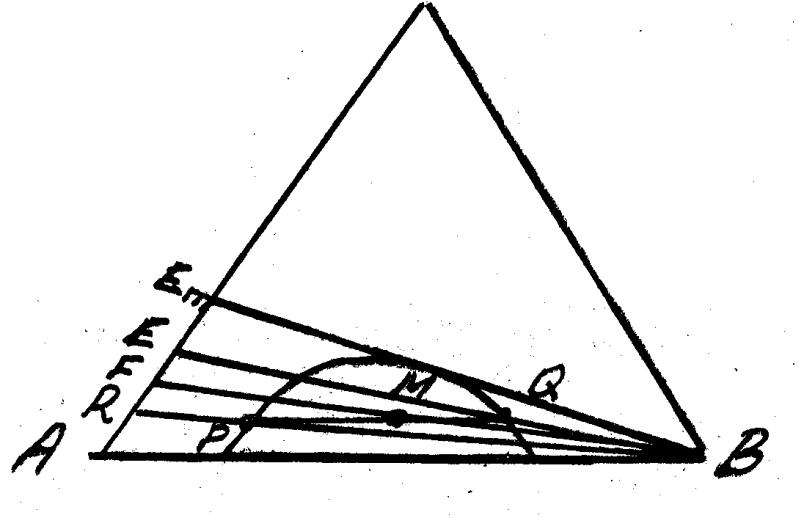
(А+С) – разделяемая смесь. В – экстрагент, который не смешивается полностью с исходной смесью, но избирательно растворяет С. F – состав, который нужно разделить.
Т., отвечает составу 3-й системы перемещения по FB.
Состав гетерогенных фаз, которые образуется в результате расслоения 3-й системы определения каннодой PQ. Фаза Q имеет больше В и называется фаза экстракта. Фаза Р имеет низкое содержание растворителя и называется фаза остатка. Разделы Р и Q, и извлекая из них растворитель, получают экстракт и рафинад и соответственно состава Е и R.
По сравнению с F,Е имеет более высокое содержание С, чем R. Если дальше добавить экстрагент к R, затем разделить фазы, промыть, то получится новый рафинат с еще более низким содержанием С.
Результат эффективности экстракции зависит от раз-в купола и от наклона канноды. Разделяемая смесь (А+С) и экстрагент В не полностью смешивается друг с жругом и разлогается по плотности, следовательно, при отслаивании произойдет расслаивание.
Лимитирующая стадия процесса – диффузия экстрагенного вещества при смешивании, поэтому для увлечения скорости перемешивают.
В производственных условиях используется непрерывный процесс экстракции, смешивания (А+С) и В производят смесителях, а разделение – в отстойниках. При этом в 1-ый смеситель непрерывно подается исходный раствор F и растворитель В, они примешивается, смесь попадает в 1-ый отстойник, далее фаза рафината поступает во 2-й смеситель, куда непрерывно подается В и т.д.
5. Кристаллизационные процессы очистки.
Кристаллизационные методы основаны на различии растворимости и диффузии примеси в жид. и тв. фазах. Применяются на конечной стадии ТП и кроме очистки от примесей достигается совершенство кристаллизационной структуры (физ. чистота).
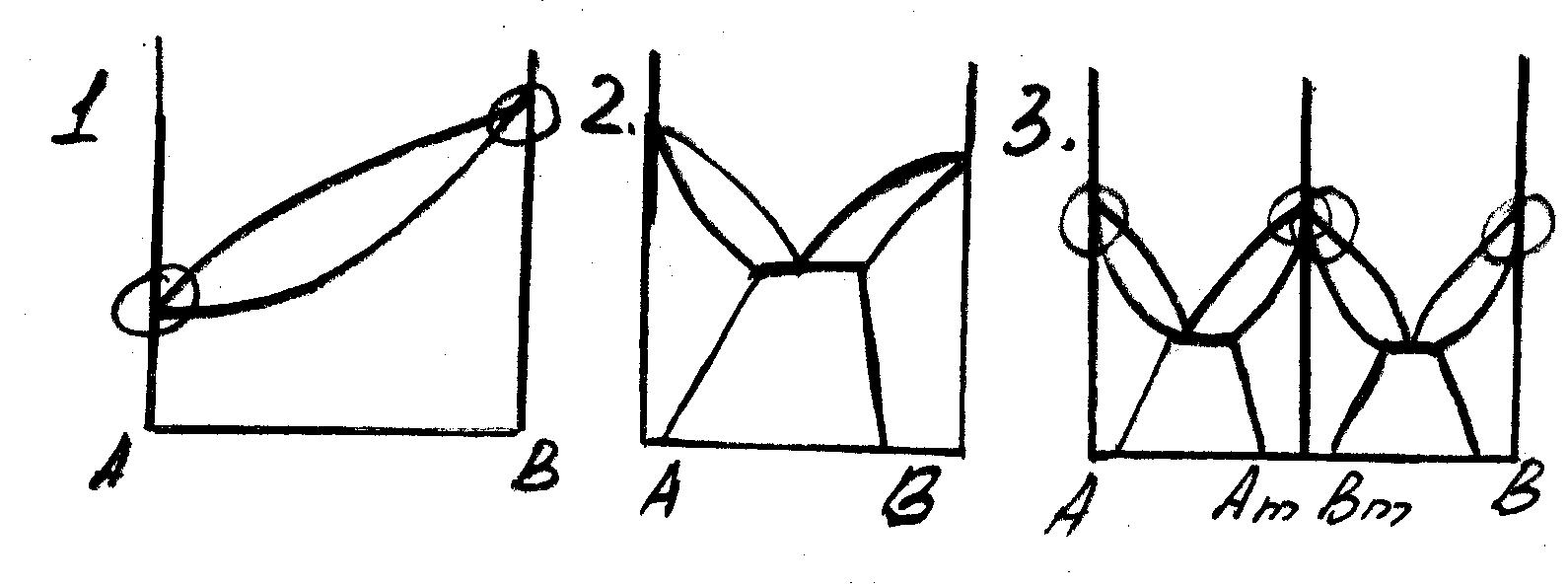
В области малых концентраций примеси диаграмму можно упростить, т.к. в углу диаграммы возле т. плавления чистого компонента различие между разными типами диаграмм пропадает. В итоге остаются 2 отрезка касательное к линиям ликвидуса и солидуса в т. плавления. Они направляются в низ, если примесь уменьшается Tпл и вверх – если увеличивается.
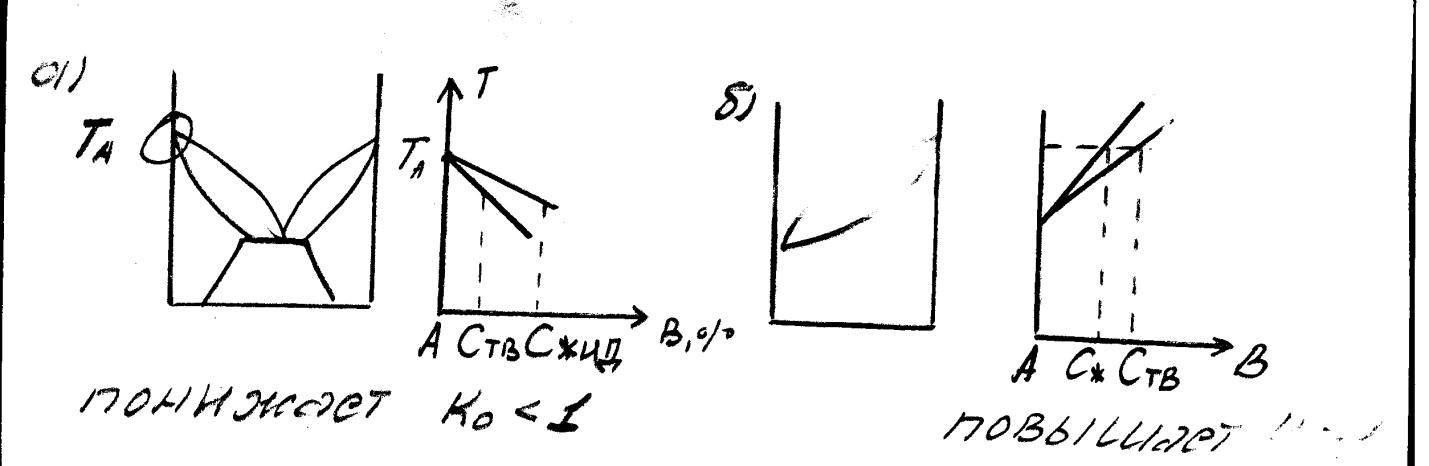
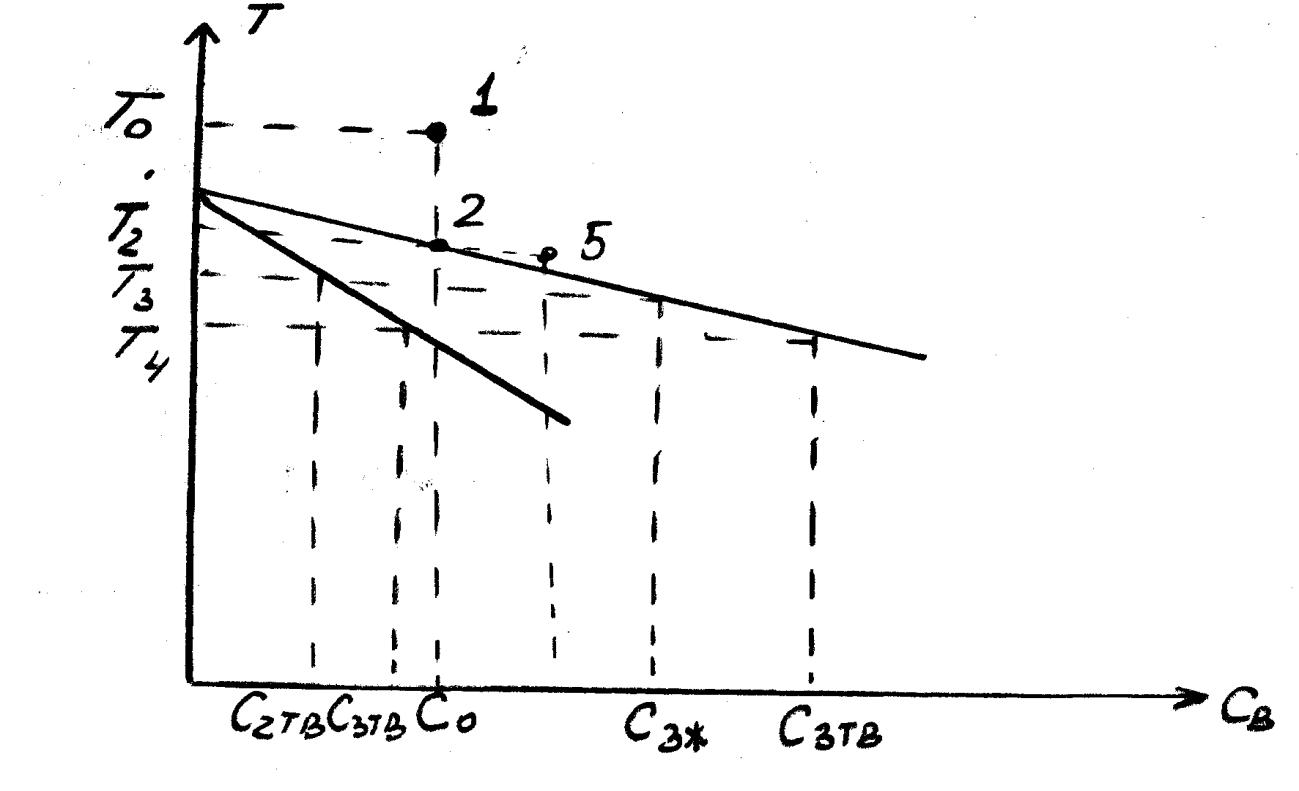
Рисунок 1.
К рис 1: Т.1 – исходное состояние системы с (СО; ТО).
При охлаждении Т.1 происходит вертикальную траекторию , которая описывает последовательные состояния системы.
Т.2 – соответствует Т начальному кристаллизации тв. Раствора, при этом образуется ТВ фаза С2тв.
При дальнейшем уменьшении Т состояние системы характеризуется 2-я т. для тв. И жид. фаз.
Т.3 - имеет состав тв. фазы С3тв и жидкой С3ж.
В Т.4 жид. фаза исчезает. система однофазна, а состав ты. Фазы должен совпадать с СО.
При дальнейшем уменьшении Т состав тв. фазы не меняется.
Закристаллизовавшейся слиток должен иметь состав = исходному. Чтобы система в любой момент времени находилась в равновесии, Т меняется от бесконечности медленно – квазистатический процесс.
В реальной системе равновесие устанавливается по средствам диффузии компонентов тв. и жид. фаз. Коэффициент диффузии (Д) в жид. больше чем в тв. фазе.
Следовательно, скорость устанавливает равновесие в расплаве намного больше, чем в кристалле. Кроме этого на границе раздела проходит процесс установления равновесия.
В реальных условиях диффузия в кристалле идет так медленно, что после уменьшении Т и кристаллизации тв. фаза остается в неравновесном состоянии.
Рассмотрим кристалл. состав 1 в реальных условиях. При уменьшении Т до Т2 возникает тв. фаза С2тв., которая более богата основным А, чем жид. фаза. В следствии этого фигуративная Т.2 сдвинется вправо и получается т.5 - это т. характеризует фигуративную точку.
Т кристаллиации Т2 выше чем Т кристаллиации т.5.
При уменьшении Т т.5. достигнет ликвидуса и твердая фаза будет иметь состав более богатый компонентом В по сравнению со слоем, который закрывается ранее. При его кристаллизации фигуративная точка опять сдвинется вправо и будет кристаллизоваться все при низкой Т, т.е. по мере роста кристалла новые нарастающие слои будут все больше обогащаться компонентом В.
Процесс кристаллизации в реальных условиях показывает, что тв. фаза кристаллизуется неоднородно по своему составу. Следовательно, кристалл галлия тв. раствор –сегрегация. Нарушение состава – сегрегационными.
2 причины, приводящие к неоднородности кристалла:
1. разница в составе твердой и жидкой фаз, находящийся в равновесии.
2. замедленность процессов выращивания в тв. фазе, т.е. диффузия.
