
Кругляк_Прогнозирование_свойств_молекулярных_веществ._Критические свойства фреонов-2018_171_стр_обложки
.pdfПоскольку атомы водорода и галогенов присутствуют как в рядах галогенпроизводных гидридов Si и Ge, так и у фреонов, значения соответствующих весов вершин, найденных при расчетах Tc фреонов, должны сохраняться. Поскольку эти атомы связаны не с атомом С, а с атомами Si и Ge, то для весов соответствующих ребер можно ожидать другие значения. Эти предположения подтверждаются нашими расчетами.
Результаты расчетов приведены в табл. 25 (рис. 9) для Si-фреонов и в табл. 26 (рис. 10) для Ge-фреонов.
Таблица 25 Галогенпроизводные гидридов Si: оптимизация весов ребер для Tc , К
на обучающей выборке из 13 Si-фреонов
|
№ |
Ключ |
|
Tc |
|
ИП |
|
|
п/п |
|
|
|
R |
|
|
|
|
Эксп. [14, 72] |
Расчет |
|
|||
|
|
|
|
|
|
|
|
|
1 |
1111 |
|
259.0998 |
263.0270 |
3.8154 |
|
|
|
|
|
|
|
|
|
|
2 |
0000 |
|
269.5000 |
272.3637 |
4.0000 |
|
|
|
|
|
|
|
|
|
|
3 |
1112 |
|
307.5000 |
310.2109 |
4.7480 |
|
|
|
|
|
|
|
|
|
|
4 |
1122 |
|
369.0000 |
364.5905 |
5.8228 |
|
|
|
|
|
|
|
|
|
|
5 |
0002 |
|
390.0000 |
387.7719 |
6.2809 |
|
|
|
|
|
|
|
|
|
|
6 |
0003 |
|
435.0000 |
424.6054 |
7.0089 |
|
|
|
|
|
|
|
|
|
|
7 |
1222 |
|
438.0000 |
427.1057 |
7.0584 |
|
|
|
|
|
|
|
|
|
|
8 |
0022 |
|
445.0000 |
465.6823 |
7.6232 |
|
|
|
|
|
|
|
|
|
|
9 |
0222 |
|
479.0000 |
489.3479 |
8.2886 |
|
|
|
|
|
|
|
|
|
|
10 |
2222 |
|
507.0000 |
498.8078 |
8.4755 |
|
|
|
|
|
|
|
|
|
|
11 |
0033 |
|
530.0000 |
534.5571 |
9.1821 |
|
|
|
|
|
|
|
|
|
|
12 |
0333 |
|
609.0000 |
610.5512 |
10.6841 |
|
|
|
|
|
|
|
|
|
|
13 |
3333 |
|
660.0000 |
659.4790 |
11.6511 |
|
|
|
|
|
|
|
|
|
|
* aH 1, aF 0.7509, aCl 0.8219, aBr 0.8719. |
||||||
Eav 1.34 % и Emax |
2.48 % , число степеней свободы f = 8. |
||||||
90

Рис. 9. Линейная зависимость Tcexp (R) для Si-фреонов на обучающей выборке из
13 соединений (табл. 24): k = 50.5954, с = 69.9822, r = 0.9983, σ = 1.9511.
91
Таблица 26 Галогенпроизводные гидридов Ge: оптимизация весов ребер для Tc , К
на обучающей выборке из 12 Ge-фреонов
№ |
Ключ |
Tc |
|
ИП |
п/п |
|
|
R |
|
Эксп. [14, 72] |
Расчет |
|||
|
|
|
|
|
1 |
0000 |
308.0000 |
311.4770 |
4.0000 |
|
|
|
|
|
2 |
1112 |
390.0000 |
378.5126 |
5.4555 |
|
|
|
|
|
3 |
1122 |
415.0000 |
426.7492 |
6.5029 |
|
|
|
|
|
4 |
0002 |
430.0000 |
428.7336 |
6.5459 |
|
|
|
|
|
5 |
1222 |
475.0000 |
481.8608 |
7.6995 |
|
|
|
|
|
6 |
0003 |
480.0000 |
469.2622 |
7.4259 |
|
|
|
|
|
7 |
0022 |
490.0000 |
498.4101 |
8.0588 |
|
|
|
|
|
8 |
0222 |
540.0000 |
533.7297 |
8.8257 |
|
|
|
|
|
9 |
2222 |
552.0000 |
544.7158 |
9.0643 |
|
|
|
|
|
10 |
0033 |
577.0000 |
583.6362 |
9.9094 |
|
|
|
|
|
11 |
0333 |
660.0000 |
663.1269 |
11.6353 |
|
|
|
|
|
12 |
3333 |
718.0000 |
714.7907 |
12.7571 |
|
|
|
|
|
* aH 1, aF 0.7509, aCl |
0.8219, aBr 0.8719. |
|
|
|||||
Eav 1.42 % и Emax 2.94 % , число степеней свободы f = 7. |
|
|||||||
Сравним вычисленные таким образом веса ребер bC X с |
bSi X и |
bGe X , где |
||||||
X {H,F,Cl,Br} (табл. 27). |
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 27 |
|
|
||
Веса ребер в С-,Si- и Ge-фреонах |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
Х= |
H |
F |
Cl |
Br |
|
|
|
|
|
|
|
|
|
|
|
|
|
C* |
1 |
2.49 |
2.77 |
2.88 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Si |
1 |
2.25 |
3.82 |
4.39 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Ge |
1 |
2.68 |
4.08 |
4.81 |
|
|
|
|
|
|
|
|
|
|
|
|
* (Таблица 10).
Графическое представление данных табл. 27 показано на рис. 11. Очевидно, что точки на графиках расположены не случайно, налицо симбатность Si- и Ge-весов ребер, между ними существует зависимость, хотя говорить о числовых характеристиках этой зависимости еще рано. На таком количестве точек достоверность параметров этой зависимости будет сомнительной. Интересно, что зависимости между найденными весами атомов
92
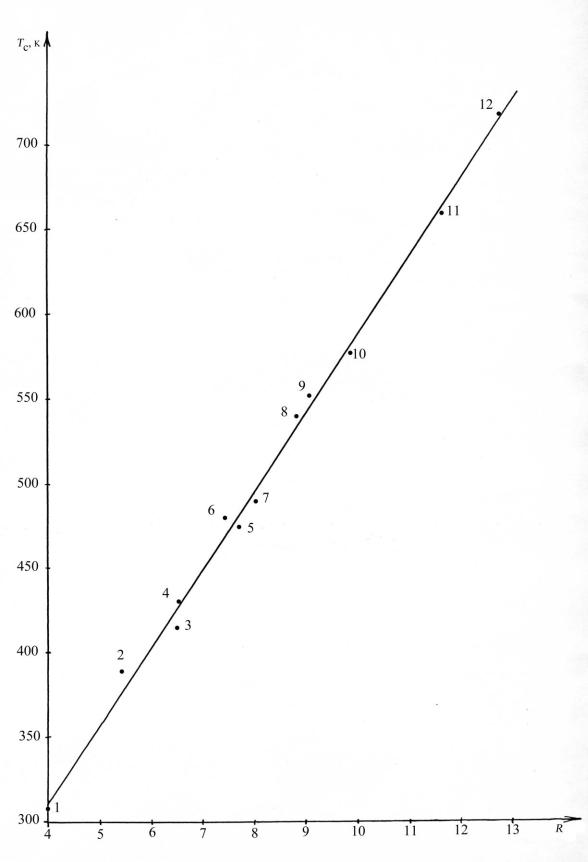
Рис. 10. Линейная зависимость Tcexp (R) для Ge-фреонов на обучающей
выборке из 12 соединений (табл. 26): k = 46.0550, с = 127.2558, r = 0.9976, σ = 2.2584.
93
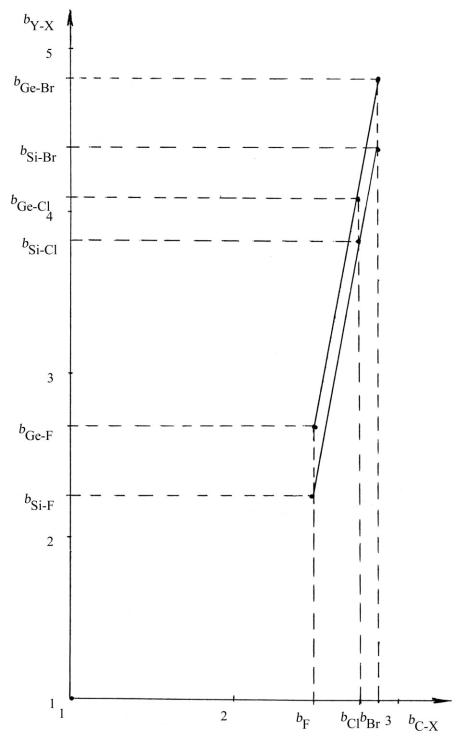
и связей и их самыми различными физическими и квантовохимическими характеристиками нам найти так и не удалось.
Рис. 11. Сравнение весов ребер, полученных оптимизацией в ходе прогнозирования Tc в рядах галогенпроизводных метана и гидридов Si и Ge.
94
Отсутствие упомянутой выше зависимости говорит о том, что имеет место некоторая внутренняя логика, связывающая веса ребер молекулярного графа, найденных оптимизацией для определенного свойства. Но они никак не связаны с физическими характеристиками атомов и связей. Это только подтверждает наше исходное предположение о том, что природа атомов и химических связей в исходных молекулах вещества настолько опосредовано влияет на свойства веществ, что с помощью их естественных характеристик трудно описать некоторое конкретное свойство вещества.
95
96
Глава 6. Механизмы истощения озонового слоя Земли. Озонобезопасные фреоны
6.1. Введение
Жизнь на Земле была бы невозможна без озонового слоя, защищающего все живое от губительного ультрафиолетового излучения Солнца. Истощение озонового слоя стало сегодня одной из основных глобальных экологических проблем человечества. Прежде всего хлорофтороуглеводороды (CFCs / ChloroFluoroCarbons), известные как фреоны различного типа (табл. 28), наряду с некоторыми другими химическими веществами являются основной причиной истощения и разрушения озонового слоя Земли [89, 90].
|
|
Таблица 28 |
|
Типы фреонов [77] |
|
|
|
|
Тип |
Расшифровка |
Атомы в молекуле |
CFC |
ChloroFluoroCarbon |
Cl, F, C |
HCFC |
HydroChloroFluoroCarbon |
H, Cl, F, C |
HFC |
HydroFluoroCarbon |
H, F, C |
HCC |
HydroChloroCarbon |
H, Cl, C |
HC |
HydroCarbon |
H, C |
PFC |
PerFluoroCarbon |
F, C |
PCC |
PerChloroCarbon |
Cl, C |
H |
Halon / Haloalkane |
Br, Cl*, F, H*, C |
* В некоторых, но не во всех.
Фреоны находят исключительно широкое применение в современной цивилизации и характеризуются такими практически и жизненно важными характеристиками как время их жизни в атмосфере [91], их потенциалом глобального потепления [92] и их потенциалом истощения озонового слоя ODP (Ozone Depletion Potential) [93]. Последняя характеристика фреонов особенно важна для нашего обсуждения. Некоторые области применения фреонов показаны в табл. 29 вместе с рекомендуемой заменой ранее и ныне все еще используемых фреонов на экологически безопасные фреоны с ODP = 0.
Хлор- и бромсодержащие фреоны попадают в атмосферу в основном в результате деятельности человека и лишь отчасти как результат естественных природных процессов, например, вулканической деятельности. Под действием УФ излучения солнца эти галогенсодержащие газы превращаются в промежуточные реакционноспособные вещества, такие как нитраты хлора [94] и брома [95], а также HCl, которые сами по себе не взаимодействуют с
97
озоном, но в результате дальнейшей фотодиссоциации порождают исключительно реакционноспособные свободные радикалы ClO и BrO, а также не менее активные свободные атомы Cl и Br, которые вместе и приводят к деструкции озона.
|
|
|
|
|
|
|
|
Таблица 29 |
|
Области применения фреонов с заменой ранее и ныне используемых CFC |
|||||||||
|
на некоторые экологически безопасные фреоны [96] |
. |
|||||||
|
|
|
|
|
|||||
Область |
|
Ранее и ныне используемые CFC |
|
Подлежат замене на один изa с ODP = 0 |
|||||
применения |
|
Тип |
Формула |
Наш код |
ODP [77] |
|
Тип |
Формула |
Наш код |
|
|
CFC-11 |
CFCl3 |
1222 |
1.0 |
|
HFC-23 |
CHF3 |
0111 |
|
|
|
HCFC-141b |
CFCl2CH3 |
122-000 |
||||
|
|
|
|
|
|
|
|||
|
|
CFC-12 |
CF2Cl2 |
1122 |
1.0 |
|
HFC-125 |
F3CCHF2 |
111011 |
|
|
CFC-13 |
CF3Cl |
1112 |
1.0 |
|
HFC-134a |
F3CCH2F |
111001 |
|
|
|
HCFC-141b |
CFCl2CH3 |
122-000 |
||||
|
|
|
|
|
|
|
|||
Хладагенты и |
|
HCFC-22 |
CHF2Cl |
0112 |
12.0 |
|
* HFC 410 HFC 32 |
CH2F2 |
0011 |
кондиционеры |
|
CFC-113 |
Cl2FCCF2Cl |
122-112 |
1.0 |
|
F3CCHF2 |
111011 |
|
|
|
|
|
|
|
|
HFC 125 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CFC-114 |
ClF2CCF2Cl |
112-112 |
1.0 |
|
* HFC 507 HFC 125 |
F3CCHF2 |
111011 |
|
|
CFC-115 |
F3CCF2Cl |
111-112 |
0.44 |
|
F3CCH3 |
111-000 |
|
|
|
|
|
|
|
|
HFC 143a |
|
|
|
|
|
|
|
|
|
|
|
|
Пропелленты |
|
|
|
|
|
|
HFC-134a |
F3CCH2F |
111001 |
|
CFC-114 |
ClF2CCF2Cl |
112-112 |
1.0 |
|
HFC-227ea |
F3CCHFCF3 |
111- 01-111 |
|
в медаэрозолях |
|
|
|||||||
|
|
|
|
|
|
||||
|
|
CFC-11 |
CFCl3 |
1222 |
1.0 |
|
HFC-245fa |
CF3CH2CHF2 |
111- 00-011 |
Пенообразующие |
CFC-12 |
CF2Cl2 |
1122 |
1.0 |
|
HFC-152a |
CHF2-CH3 |
011-000 |
|
CFC-113 |
Cl2FCCF2Cl 122-112 |
1.0 |
|
HFC-365mfc |
CF3CH2CF2CH3 |
111- 00-11- 000 |
|||
|
|
|
|||||||
|
|
HCFC-141b CFCl2CH3 122 - 000 |
0.12 |
|
HCFC-124 |
CHFClCF3 |
012-111 |
||
Растворители, |
|
CFC-11 |
CFCl3 |
1222 |
1.0 |
|
HCFC-123 |
CHCl2CF3 |
022-111 |
|
|
|
|
|
|
|
|
|
|
обезжириватели, |
|
CFC-113 Cl2FCCF2Cl 122-112 |
1.0 |
|
HCFC-141b |
CFCl2CH3 |
122-000 |
||
чистящие |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
a См. также L. Benussi, S. Bianco, D. Piccolo et al. Properties of potential ecofriendly gas replacements for particle detectors in high-energy physics, arXiv:1505.00701v1: cds.cern.ch/record/2013488.
* Азеотропная смесь 1:1.
Хорошо изучены два процесса деструкции озона в стратосфере: фотохимический и в результате столкновения молекул озона с электронами космического происхождения. Можно не сомневаться в том, что это не единственные два известных процесса, приводящие к истощению озонового слоя. Мы приведем аргументы в пользу еще одной возможной корпускулярной модели реакции протонов космического происхождения в истощении озонового слоя Земли, тем более что космическое излучение, достигающее стратосферы Земли состоит приблизительно на 90% из протонов и лишь на 1% из электронов; еще 9% составляют ядра атомов гелия, а на ядра более тяжелых элементов приходится еще около 1%.
98

6.2. Фотохимическая модель
Фотохимическая модель истощения озонового слоя в результате фрагментации хлор- и бромсодержащих фреонов под действием УФ излучения Солнца с образованием исключительно реакционноспособных свободных атомов Cl и Br была предложена с разной степенью детализации механизма превращения озона в кислород в период 1970 – 1974 годов несколькими исследователями [97 – 101], а в 1995 году Паулю Крутцену, Марио Молина и Шервуду Роуланду за их исследования в области атмосферной химии, в частности, образования и распада озона была присуждена Нобелевская премия [102]. С историей исследований атмосферного озона можно ознакомиться в
[103].
Хлор- и бромсодержащие фреоны под действием УФ излучения Солнца образуют исключительно реакционноспособные свободные радикалы монооксиды хлора ClO и брома BrO, а также свободные атомы Cl и Br, которые участвуют в трех принципиально важных реакционных циклах, которые ведут к разрушению молекул озона с образованием молекул кислорода.
В одном из циклов протекают две сопряженные реакции Cl + O3 и ClO + O (рис. 12). Конечным результатом этого цикла является превращение одной молекулы озона и одного атома кислорода в две молекулы кислорода.
Рис. 12. Две сопряженные циклические химические реакции, ведущие к разрушению молекулы озона в результате ее взаимодействия с атомарным хлором с образованием в итоге двух молекул кислорода.
99
