
- •Содержание
- •1 Аналитический обзор 11
- •2 Методическая часть 29
- •3. Экспериментальная часть 37
- •4 Обсуждение результатов эксперимента 44
- •Условные обозначения
- •Введение
- •1 Аналитический обзор
- •1.1 Регулярные мультимолекулярные структуры
- •1.2 Хроматография
- •1.2.1 Металл-аффинная хроматография – сочетание принципов лигандообменной и аффинной хроматографии
- •1.3 Методы характеризации сорбентов
- •1.3.1 Удельная поверхность
- •1.3.2 Емкость сорбента, влажность
- •1.3.3 Электрокинетический потенциал
- •1.4 Maldi масс-спектрометрия
- •1.5 Идентификация белков – метод pmf
- •1.6 Тандемная масс-спектрометрия (мс-мс) и идентификация пептиов по фрагментным масс-спектрам
- •1.7 Идентификация пост-трансляционных модификаций
- •1.8 Аддукты зомана с сывороточным альбумином
- •2 Методическая часть
- •2.1 Используемые материалы:
- •2.2 Методики получения сорбента и исследования
- •2.2.1 Получение рмм (FeIii) сорбента
- •2.2.2 Определение удельной поверхности сорбента
- •2.2.3 Определение сорбционной емкости сорбента
- •2.2.3.1 Проведение металл-аффинного анализа
- •2.2.3.2 Определение влажности рмм Fe(III) сорбента
- •2.2.3.3 Определение влажности коммерческого сорбента
- •2.2.4 Анализ фосфорилированных пептидов казеина молока коровы
- •2.2.4.1 Выделение суммарного белка из обезжиренного сухого молока
- •2.2.4.2 Гидролиз суммарного белка молока коровы в присутствии трипсина
- •2.2.5 Анализ фосфонилированных пептидов сывороточного альбумина человека
- •2.2.5.1 Гидролиз сывороточного альбумина человека в присутствии пепсина
- •2.2.6 Масс-спектрометрический анализ
- •2.2.6.1 Масс-спектрометрический анализ методом maldi-tof и maldi-tof-tof
- •2.2.6.2 Обработка данных масс-спектрометрического анализа
- •3. Экспериментальная часть
- •3.1. Получение рмм Fe(III) сорбента
- •3.2 Определение удельной поверхности
- •3.3 Определение электрокинетического потенциала и размера частиц.
- •3.4 Определение сорбционной емкости сорбента
- •3.4.1Проведение металл-аффинного анализа
- •3.4.2 Определение содержание пептида в проскоке и контрольном образце
- •3.4.3 Определение влажности коммерческого сорбента и рммс Fe(III)
- •3.5 Анализ фосфорилированных пептидов казеина молока коровы
- •3.5.1 Приготовление микроколонки с сорбентом
- •3.5.2 Металл-аффинная хроматография на коммерческом сорбенте
- •3.5.3 Металл-аффинная хроматография на рммс Fe(III)
- •3.6 Анализ фосфонилированных пептидов сывороточного альбумина человека
- •3.6.1 Приготовление металл-аффинной колонки
- •3.6.2 Выбор элюэнта
- •3.6.3 Металл-аффинная хроматография на коммерческом сорбенте
- •3.6.4 Металл-аффинная хроматография на рммс Fe(III)
- •3.7 Масс-спектрометрический анализ
- •3.7.1 Проведение масс-спектрометрического анализа
- •4 Обсуждение результатов эксперимента
- •4.1 Охарактеризация сорбента
- •4.1.1. Получение рмм сорбента, содержащего ионы железа (III) и приготовление хроматографических колонок.
- •4.1.2 Определение удельной поверхности
- •4.1.3 Определение емкости сорбента
- •4.1.4 Микроэлектрофоретические исследования.
- •4.1.4.1 Определение электрокинетического потенциала
- •4.1.4.2 Расчет удельной поверхности рмм сорбента
- •4.2 Исследование возможности специфичного выделения фосфорилированных пептидов из биологического образца методом металл-аффинной хроматографии с использованием рммс(Fe III)
- •4.3 Разработка метода металл-аффинного выделения прямых ковалентных аддуктов зомана с сывороточным альбумином с помощью рмм сорбентов Fe(III) для последующего масс-спектрометрического анализа
- •4.3.1 Поиск и идентификация аддуктов сывороточного альбумина человека с зоманом
- •4.3.2 Выделение фосфонилированных пептидов сывороточного альбумина человека с использованием рммс (Fe III)
- •4.3.2 Масс-спектрометрическая идентификация сайтов связывания зомана с альбумином при взаимодействии с белками in vitro
- •Выводы по работе:
- •Список использованных источников.
- •Приложение а Технико-экономическая оценка научно-исследовательской работы Обоснование договорной цены на разработку
- •Расчет затрат на научно-исследовательскую разработку
- •Расчет затрат на сырье, материалы, реактивы, покупные изделия и полуфабрикаты
- •Расчет затрат на энергоресурсы
- •Расчет затрат на приборы, оборудование для научно-экспериментальных работ и суммы амортизационных отчислений
- •Расчет затрат на оплату труда с обязательными начислениями
- •Прочие затраты Расчет суммы расходов по использованию вычислительной техники.
- •Затраты на выполнение специальных анализов.
- •Расчет суммы накладных расходов
- •Расчет сметы затрат на разработку
- •Приложение б Охрана труда и окружающей среды
- •1 Опасные и вредные производственные факторы
- •2 Пожарная безопасность
- •3 Обеспечение санитарно-гигиенических условий
- •4 Вентиляция
- •5 Аптечка и ее содержание
- •6 Освещение помещения
- •7 Безопасность выполнения работы в лаборатории
- •8 Анализ технологических операций
- •9 Меры первой помощи
- •Охрана окружающей среды
- •Приложение в
- •Приложение г Масс-спектры смеси триптических пептидов казеина, элюированных с колонки с сорбентом, содержащим ионы железа.
1.4 Maldi масс-спектрометрия
Масс-спектрометрия является одним из наиболее универсальных инструментов при анализе сложных белковых проб, который позволяет не только идентифицировать белок в смеси, но так же установить последовательность аминокислот и идентифицировать модификацию белка.
Для исследования белка наиболее подходящими являются мягкие методы ионизации, например ионизация лазерной десорбцией в присутствии матрицы (Matrix-Assisted Laser Desorbtion/Ionization, MALDI).
Метод MALDI основан на воздействии импульсами лазерного излучения на матрицу с анализируемым веществом. Матрица представляет собой химическое соединение, которое способно возгоняться под воздействием лазера и захватывать с собой молекулы нелетучих термолабильных аналитов. Кроме того, матрица способствует, ионизации анализируемого вещества. Наиболее распространенными матрицами являются: 2,5-дигидробензойная кислота (DHB), α-циано-4-гидроксикоричная кислота (CHCA) (рисунок1.4.1).
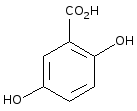
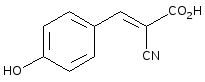
2,5-дигидроксибензойная к-та -циано-4-гидроксикоричная к-та
Рисунок 1.4.1 - Наиболее распространенные матрицы
Поверхность образца (по сравнению с площадью последующего облучения) не является однородной. При облучении в выбранной точке лазерным лучом происходит испарение матрицы вместе с анализируемым веществом и дальнейшая их ионизация [16] (рисунок 1.4.2)
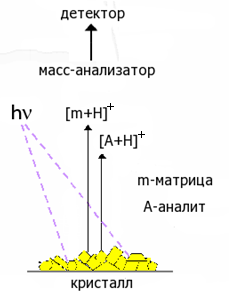
Рисунок 1.4.2 - Схема образования ионов в MALDI.
Процесс образования ионов можно разделить на две стадии. Первая стадия связана с образованием ионов из нейтральных молекул, как правило, она относится к ионам матрицы (МТ). Вторая стадия имеет отношение к последующей ионизации анализируемого вещества (МА).
Возбуждение молекул, которое может протекать несколькими способами, сопровождается фотоионизацией. Далее протекает множество фотохимических реакций. В результате может образоваться набор ионов, которые участвуют в последующей стадии ионизации анализируемого соединения. Часть процессов, происходящих с молекулами матрицы, может относиться и к молекулам анализируемых соединений. Большая (на 5-6 порядков) концентрация молекул матрицы по сравнению с анализируемыми соединениями позволяет считать, что ионизация последних осуществляется в результате переноса электрона или Н+ [17]

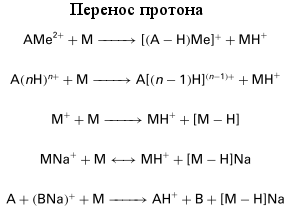
Таким образом, при рассмотрении MALDI-масс-спектра мы наблюдаем пики, относящиеся к фрагментам матрицы (в диапазоне (100-400) Да, что затрудняет масс-спектрометрический анализ аминокислот и небольших пептидов) и анализируемого вещества. Кроме того, достаточно часто регистрируются ионы, относящиеся к комплексу матрица - аналит, что всегда необходимо учитывать при интерпретации масс-спектров.
Обобщая данные, можно сказать, что метод MALDI характеризуется небольшой фрагментацией анализируемого вещества, возможностью работы с многокомпонентными смесями; при ионизации в основном образуются однозарядные ионы, что значительно облегчает интерпретацию спектров. Кроме того, мягкие методы ионизации не являются количественными. Это вызвано тем, что соотношение интенсивности регистрируемых ионов, если это не проверено в специальных экспериментах, не отражает соотношения концентраций ионов, присутствующих в смеси. Подобные расхождения вызваны тем, что сродство к протону, гидрофобность, молекулярная масса соединений, состав веществ, присутствующих при измерении, у разных соединений существенно различаются. Кроме того, интенсивность пиков зависит от условий эксперимента и параметров регистрации [18-21].
