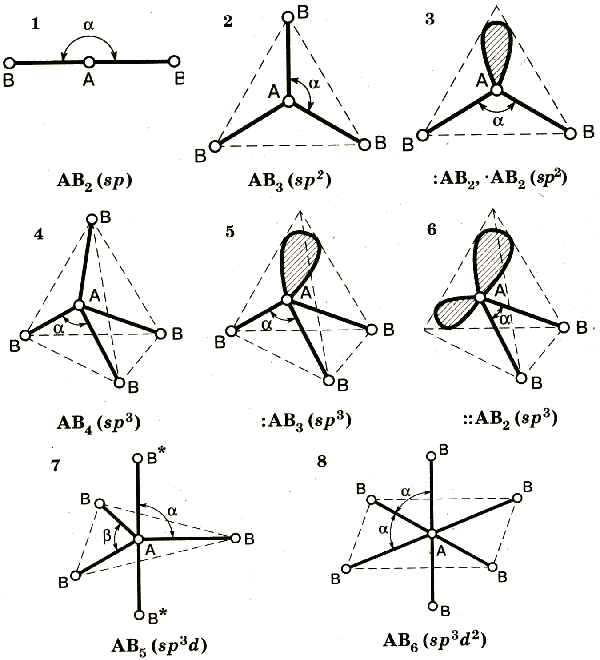Вопрос № 1
Понятия:
А)Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н+ или ОН–, в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества.
Б)Молярная масса эквивалента (МЭ) – это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности:
|
МЭ = М×fЭ. |
В) Моль - это такое количество вещества, в котором содержится определенное число частиц (молекул, атомов, ионов), равное постоянной Авогадро
![]()
Г) Моля́рная ма́сса вещества — масса одного моля вещества. Для отдельных химических элементов молярной массой является масса одного моля отдельных атомов этого элемента. В этом случае молярная масса элемента, выраженная в г/моль, численно совпадает с массой атома элемента, выраженной в а.е.м. (атомная единица массы). Однако надо чётко представлять разницу между молярной массой и молекулярной массой, понимая, что они равны лишь численно и отличаются по размерности.[1]
Молярные массы сложных молекул можно определить, суммируя молярные массы входящих в них элементов.
Например, молярная масса воды (H2O) есть MH2O = 2 MH +MO = 2·1+16 = 18 (г/моль)
Законы:
А)Сохранения массы- Масса веществ, вступающих в химическую реакцию, равна массе веществ, образующихся в результате реакции.
Б) Закон постоянства состава (Ж.Л. Пруст, 1801—1808гг.) — любое определенное химически чистое соединение независимо от способа его получения состоит из одних и тех же химических элементов, причем отношения их масс постоянны, а относительные числа их атомов выражаются целыми числами.
В)Эквивалентов- Закон эквивалентов был открыт в 1792 г. И. Рихтером. Современная формулировка закона: вещества реагируют и образуются согласно их эквивалентам.
Г)Авагадро- В равных объемах газов (V) при одинаковых условиях (температуре Т и давлении Р) содержится одинаковое число молекул.
Вопрос №2
Скорость химической реакции — изменение количества вещества одного из реагирующих веществ за единицу времени в единице реакционного пространства.
Факторы: природа реагирующих веществ, наличие катализатора, температура (правило Вант-Гоффа), давление, площадь поверхности реагирующих веществ, концентрация реагентов.
Единица измерения:
Единицей измерения скорости химической реакции служит 1 моль/л * с
Закон действующих масс - скорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
Константа скорости реакции (удельная скорость реакции) — коэффициент пропорциональности в кинетическом уравнении.
Физический смысл константы скорости реакции k следует из уравнения закона действующих масс: k численно равна скорости реакции при концентрации каждого из реагирующих веществ равной 1 моль/л.
Константа скорости реакции зависит от температуры, от природы реагирующих веществ, но не зависит от их концентрации.
3.Влияние температуры на скорость химических реакций. Правило Вант-Гоффа, температурный коэффициент химической реакции. Энергия активации процесса, активированный комплекс. На состояние хим. Равновесия оказывает влияние темпер-ра. Константа равновесия (К) с ростом темп-ры может и увеличиваться и уменьшаться. При повышении тем-ры смещение происходит в сторону эндотермической реакции, а понижение темпер-ры в сторону экзотермической реакции. При повышении темп-ры смещение происходит влево, при понижении вправо. Правило Вант-Гоффа: при увеличении темпер-ры на каждые 10 градусов, скорость любой реакции возростает в 2-4 раза. Температурный коэффициент: γ(гамма)= (2-4) Энергия активации-это тот избыток энергии по сравнению со средней энергией частиц при данной темп-ре, которым они должны обладать чтобы произошла реакция между ними. Обозначается (Еа) 4. Катализ. Гомогенный и гетерогенный катализ. Механизм влияния катализаторов на скорость хим. реакции. Ферменты. Роль катализа в химии и биохимии. Катализ-изменение скорости химической реакции под действием катализаторов. Гомогенный катализ-реагирующие вещество и катализатор находятся в одном агрегатном состоянии. Гетерогенный катализ- реагирующие вещество и катализатор находятся в разном агрегатном состоянии. Все катализаторы ускоряют как обратную так и прямую реакции, поэтому наличие катализатора на смещение равновесия не влияет, а только способствует более быстрому достижению этого равновесия. Ферменты-биохимические катализаторы. Роль в химии: Многие важнейшие химические производства, такие, как получение серной кислоты, аммиака, азотной кислоты, синтетического каучука, ряда полимеров и др., проводятся в присутствии катализаторов.
5.Системы, в которых протекает хим реакции могут достигать специфич.состояния-хим.равновесия. Хим равновесие имеет динамич.характер.Зависит от условий в которых протекает реакция.Хим.равновесие может устанавливаться только в тех системах,где происходят обратные реакции.Признаки хим.равновесия:1при отсутствии внешних воздействий установившиеся равновестные концентрации не изменяются2значение константы равновесия не зависит от того подходит ли система к равновесию со стороны реагентов или со стороны продуктов.3Система следует за внешними воздействиями,если внешние воздействия снимаются-система возращается в исходное состояние.Кравнов.=Кскор.прям./Кскор.обратн.Она показывает во сколько раз скорость прям.реакции больше скорости обратной.Принцип Ле Шателье:Если на систему находящ.в состоянии равновесия произв.внешнее воздействие,то равновесие смещается в сторону той из двух противоположных реакций,которая ослабевает это воздействие.При увеличении C хотябы одного из реагентов равновесие смещается в сторону образов.продуктов реакции(↑С→).При увелич.давления равнов.смещается в сторону реакции которая идет с уменьшением числа молекул(↑Р→).При ↑t←,при ↓t→.
6.Сущность хим.реакции сводится к разрыву связей в исх.вещ-вах,возникновению новых связей в продуктах.При этом общее число атомов до и после остается одинаковым.Поскольку образование связей происходит с выделением энергии,а разрыв с поглащением.Экзотермич.-с выделением теплоты,эндотермич.-с поглощением теплоты.Количество выделенной и поглащенной теплоты при протекании реакции называют тепловым эффектом.Если все конечные продукты реакции и исходные в-ва находятся в стандарт.условиях,то ∆Н называют стандартной энтальпией.Закон Гессса: тепловой эффект(или изменение энтольпии)зависит только от начального к конечному состоянию реагирующих в-в.И не зависит от промежуточных стадий реакции.
Вопрос7
энтропия-используется для оценки степени беспорядка в системе чем больше беспорядок тем борльше энтропия S. Состояние с большим беспорядком называется более вероятным. Если хим. реакция протекает с увеличением числа молекул то беспорядок в системе увеличивается энтропия возрастает беспорядок уменьшается энтропия уменьшается.
Вопрос 8
свободная энергия системы при постояном давлении и температуре називают свободной энергией гибса G.
Самопроизвольный переход системы из начального состаяния в конечное возможен при условии что G1>G2 то есть дельта G <0 чем больше возрастание энтропии и чем больше уменьшение энтальпии тем больше уменьшается и G и тем полнее реакция протекает в прямом направлении если дельта G >0 то реакция в прямом направлении самопроизвольно не протекает что бы процес шёл необходимо поступление энергии из вне . реакция может протекать самопроизвольно только в обратном направлении если дельта G=0 то система находиться в равновесии.
9)Растворы - однофазные системы, состоящие из двух или более компонентов. По своему агрегатному состоянию растворы могут быть твердыми, жидкими или газообразными.
Концентрация раствора– это величина, отражающая пропорции между растворенным веществом и растворителем. Такие качественные понятия, как «разбавленный» и «концентрированный», говорят только о том, что раствор содержит мало или много растворенного вещества. Для количественного выражения концентрации растворов часто используют проценты (массовые или объемные), а в научной литературе – число молей или химических эквивалентов (см. ЭКВИВАЛЕНТНАЯ МАССА) растворенного вещества на единицу массы или объема растворителя либо раствора. Чтобы не возникало путаницы, следует всегда точно указывать единицы измерения концентрации.
Концентрированный раствор содержит такие кол-ва растворенного вещества, которые сравнимы с кол-вом растворителя.
Насыщенный раствор — раствор, в котором растворённое вещество при данных условиях достигло максимальной концентрации и больше не растворяется. Осадок данного вещества находится в равновесном состоянии с веществом в растворе.
Сильные электролиты — химические соединения, молекулы которых в разбавленных растворах практически полностью диссоциированы на ионы.
Степень диссоциации таких электролитов близка к 1.
К сильным электролитам относятся многие неорганические соли, некоторые неорганические кислоты и основания в водных растворах, а также в растворителях, обладающих высокой диссоциирующей способностью (спирты, амиды и др.).
Слабые электролиты — химические соединения, молекулы которых даже в сильно разбавленных растворах незначительно диссоциированны на ионы, которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым электролитам относится большинство органических кислот и многие органические основания в водных и неводных растворах.
Слабыми электролитами являются:
-почти все органические кислоты и вода;
-некоторые неорганические кислоты: HF, HClO, HClO2, HNO2, HCN, H2S, HBrO, H3PO4,H2CO3, H2SiO3, H2SO3 и др.;
-некоторые малорастворимые гидроксиды металлов: Fe(OH)3, Zn(OH)2 и др.; а также гидроксид аммония NH4OH.
10)
Сильные и слабые электролиты. В зависимости от степени диссоциации различают электролиты сильные и слабые. Электролиты со степенью диссоциации больше 30% обычно называют сильными, со степенью диссоциации от 3 до 30% — средними, менее 3% — слабыми электролитами.
К сильным электролитам относятся почти все соли, некоторые кислоты (НСl, HBr, HI, НNО3, НсlO4, Н2SO4(разб.)) и некоторые основания (LiОН, NaOH, КОН, Са(ОН)2, Sr(OH)2, Ва(ОН)2). К слабым электролитам относится большинство кислот (особенно органических) и оснований.
Степень диссоциации как сильных, так и слабых электролитов зависит от концентрации раствора (степень диссоциации тем выше, чем более разбавлен раствор).
Константа диссоциации. Более точной характеристикой диссоциации электролита является константа диссоциации, которая от концентрации раствора не зависит.
Выражение для константы диссоциации можно получить, если записать уравнение реакции диссоциации электролита АК в общем виде:
A K « A- + K+.
Поскольку диссоциация является обратимым равновесным процессом, то к этой реакции применим закон действующих масс, и можно определить константу равновесия как
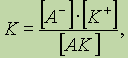
где К — константа диссоциации, которая зависит от температуры и природы электролита и растворителя, но не зависит от концентрации электролита.
Электролитическая диссоциация — процесс распада электролита на ионы при растворении его в полярном растворителе или при плавлении.
11)Ио́нное произведе́ние воды́ — произведение концентраций ионов водорода Н+ и ионов гидроксида OH− в воде или в водных растворах, константа автопротолиза воды.
Водоро́дный показа́тель, pH— мера ионов водорода в растворе, и количественно выражающая его кислотность, вычисляется как отрицательный (взятый с обратным знаком) десятичный логарифм активности водородных ионов, выраженной в молях на литр:
![]()
гидроксильный показатель - обратная pH величина — показатель основности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:
![]()
Буферные растворы — растворы с определённой устойчивой концентрацией водородных ионов; смесь слабой кислоты и её соли (напр., СН3СООН и CH3COONa) или слабого основания и его соли (напр., NH3 и NH4CI).
Примечание:
Значение pH буферного раствора можно
рассчитать по формуле:
![]() ,
где pK это отрицательный десятичный
логарифм от константы диссоциации
кислоты HA.
,
где pK это отрицательный десятичный
логарифм от константы диссоциации
кислоты HA.
12
Гидроксо́ний (оксоний, гидроний) НзО+ — комплексный ион, соединение протона с молекулой воды.
Водородные ионы в водных и спиртовых растворах кислот существуют в виде гидратированных или сольватированных ионов гидроксония. Для измерения концентрации водородных ионов используется водородный электрод.
Вода, как слабый электролит:
1)степень диссоциации меньше единицы и уменьшается с ростом концентрации.
2) очень слабый электролит. Электропроводность природных и сточных вод значительно выше, так как они содержат достаточно много разнообразных солей, диссоциирующих в воде на ионы
Гидролиз солей — разновидность реакций гидролиза, обусловленного протеканием реакций ионного обмена в растворах (преимущественно, водных) растворимых солей-электролитов. Движущей силой процесса является взаимодействие ионов с водой, приводящее к образованию слабого электролита в ионном или (реже) молекулярном виде («связывание ионов»).
Типы гидролиза: 1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону):
CO32− + H2O = HCO3− + OH− Na2CO3 + Н2О = NaHCO3 + NaOH (раствор имеет слабощелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону):
Cu2+ + Н2О = CuOH+ + Н+ CuCl2 + Н2О = CuOHCl + HCl (раствор имеет слабокислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)
3. Гидролиз соли слабой кислоты и слабого основания:
2Al3+ + 3S2− + 6Н2О = 2Al(OH)3(осадок) + ЗН2S(газ) Al2S3 + 6H2O = 2Al(OH)3 + 3H2S (равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа).
Соль сильной кислоты и сильного основания не подвергается гидролизу, и раствор нейтрален.
Степень гидролиза - отношение части соли, подвергающейся гидролизу, к общей концентрации её ионов в растворе. Обозначается α (или hгидр); α = (cгидр/cобщ)·100 % где cгидр — число молей гидролизованной соли, cобщ — общее число молей растворённой соли. Степень гидролиза соли тем выше, чем слабее кислота или основание, её образующие.
Константа гидролиза — константа равновесия гидролитической реакции.
Формулы констант гидролиза:
В общем случае для соли, образованной слабой кислотой и сильным основанием:
![]() ,
где Ka — константа
диссоциации слабой кислоты, образующейся
при гидролизе
,
где Ka — константа
диссоциации слабой кислоты, образующейся
при гидролизе
для соли, образованной сильной кислотой и слабым основанием:
![]() ,
где Kb — константа
диссоциации слабого основания,
образующегося при гидролизе
,
где Kb — константа
диссоциации слабого основания,
образующегося при гидролизе
для соли, образованной слабой кислотой и слабым основанием:
![]()
Cвязь между константой и степенью гидролиза в том, что степень гидролиза зависит от константы.
Ступенчатый гидролиз – гидролиз который протекает за несколько ступеней
Пример
I ступень: Zn(AsO2)2 + H2O = ZnOHAsO2 + HAsO2 Zn2+ + H2O = ZnOH+ + H+ II cтупень: ZnOHAsO2 + H2O = Zn(OH)2 + HAsO2 ZnOH+ + H2O = Zn(OH)2 + H+
13.Электронное облако – область околоядерного пространства, в которой
вероятность пребывания электрона равна 90-95%.
Форма s-орбиталей сферическая, p-орбитали напоминают гантели, d- и f-орбитали имеют более сложную форму.
Электронные облака s p d электронов
s-облако-сфера
p- облако-гантель
d- облако-четырехлепестковая фигура ( две перекрещенные гантели)
14 Состояние электрона в атоме определяется четырьмя Квантовыми числами.
Каждый электрон в атоме характеризуется четырьмя квантовыми числами: n -главное, l – орбитальное (побочное), m – магнитное, ms – спиновое.
Главное квантовое число n характеризует энергию электронов на данном уровне и размер электронного облака: чем больше значение n, тем больше энергия электронов и размер электронного облака. Число n изменяется от 1 до 7. Значение n данного электрона равно номеру уровня, на котором он находится.
l-Орбитальное квантовое число характеризует форму электронного облака и
принимает значения от 0 до n–1. Число значений l равно числу подуровней на
данном уровне:
Магнитное квантовое число m характеризует расположение облаков в пространстве
и принимает значения + l..0..- l. Число значений m равно числу орбиталей в
главном подуровне:
Спиновое квантовое число характеризует ms собственный момент количества движения электрона и принимает значения +1/2 и –1/2. Спин – чисто квантовое
понятие, не имеющее аналогов в макромире. Это собственный момент импульса
электрона, не связанный с движением в пространстве.
15. Энергетический уровень — собственные значения энергии квантовых систем, то есть систем, состоящих из микрочастиц (электронов, протонов и других элементарных частиц) и подчиняющихся законам квантовой механики. Каждый уровень характеризуется определённым состоянием системы, или подмножеством таковых в случае вырождения. Понятие применимо к атомам (электронные уровни), молекулам (различные уровни, соответствующие колебаниям и вращениям), атомным ядрам (внутриядерные энергетические уровни) и т.д.
. Подуровни оболочек обозначаются буквами s, p, d, f, g, h, i или цифрами от 0 до 6.
Атомная орбиталь — одноэлектронная волновая функция в сферически симметричном электрическом поле атомного ядра, задающаяся главным n, орбитальным l и магнитным m квантовыми числами
Правило Кличковского.
Заполнение электронами орбиталей в
атоме происходит в порядке возрастания
суммы главного и орбитального квантовых
чисел
![]() .
При одинаковой сумме раньше заполняется
орбиталь с меньшим значением
.
При одинаковой сумме раньше заполняется
орбиталь с меньшим значением
![]()
Правило Гунда
суммарное значение спинового квантового числа электронов данного подслоя должно быть максимальным.
Принцип Паули можно сформулировать следующим образом: в пределах одной квантовой системы в данном квантовом состоянии может находиться только одна частица, состояние другой должно отличаться хотя бы одним квантовым числом
Принцип наименьшей энергии
В атоме каждый электрон располагается так, чтобы его энергия была минимальной (что отвечает наибольшей связи его с ядром).
16. «свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов».
Теория строения атома объясняется периодичностью изменения свойств элементов , возростание положительных зарядов ядер от 1 до 109 обуславливает периодичностью повторения строения внешних периодов уровня . А поскольку свойства элементов зависят от числа электронов на внешнем энергетическом уровне и они повторяются.
Энергия ионизации, сродство к электрону, электроотрицательность по периоду возростает а в группе уменьшается ; металлические свойства по периоду уменьшаются по группе увеличиваются ; основные св-ва в периоде уменьшаются в группе увеличиваются , кислотные в периоде увеличиваются а в группе уменьшаются восстановительные по периоду уменьшаются а по группе увеличиваются окислотельнные по периоду увеличиваются в группе уменьшаются
17.
энергия ионизации-энергия необходимая для отрыва наиболее слобосвязанного электрона. при отрыве образуется катион.
энергия сродстава к электрону-энергия,которая выделяется в результате присоединения электроная к атому.
электроотрицательность-это способность атомов соединение притягивать к себе валентные электроны, то есть участие электрона в образовании связи.
Радиус атома-расстоянию до самой дальней из стабильных орбит электронов в электронной оболочке этого атома
18.
Ковалентная связь — химическая связь, образованная перекрытием пары валентных электронных облаков.
метод валентных связей:
1.хим.связь образуется только валентными электронами атомов с параллельными спинам.происходит перекрывание электронных облаков, что приводит к
понижению потенциальной энергии системы.
2.в пространстве связь располагается по направлению, в котором возможность перекрывания электронных облаков наибольшая.
обменный механизм.
К обменному механизму относят случаи, когда в образовании электронной пары от каждого атома участвует по одному электрону. Связь возникает благодаря
образованию общей электронной пары за счет объединения неспаренных электронов.
донорно-акцепторный механизм-это механизм образования ковалентной связи за счёт двухэлектронного облака, одного атома(донора) и свободной орбитали другого атома(акцептора).донор имеет свободную пару акцептором свободную орбиталь.
сигма и пи связи. Сигма (σ)-, пи (π)-связи — приближенное описание видов ковалентных связей в молекулах различных соединений, σ-связь характеризуется тем, что плотность
электронного облака максимальна вдоль оси, соединяющей ядра атомов. При образовании π-связи осуществляется так называемое боковое перекрывание
электронных облаков, и плотность электронного облака максимальна «над» и «под» плоскостью σ-связи. Для примера возьмем этилен, ацетилен и бензол.
В молекуле этилена С2Н4 имеется двойная связь СН2=СН2, его электронная формула: Н:С::С:Н. Ядра всех атомов этилена расположены в одной плоскости. Три
электронных облака каждого атома углерода образуют три ковалентные связи с другими атомами в одной плоскости (с углами между ними примерно 120°).
Облако четвертого валентного электрона атома углерода располагается над и под плоскостью молекулы. Такие электронные облака обоих атомов углерода,
частично перекрываясь выше и ниже плоскости молекулы, образуют вторую связь между атомами углерода. Первую, более прочную ковалентную связь между
атомами углерода называют σ-связью; вторую, менее прочную ковалентную связь называют π-связью.
В линейной молекуле ацетилена
Н—С≡С—Н (Н : С ::: С : Н)
имеются σ-связи между атомами углерода и водорода, одна σ-связь между двумя атомами углерода и две π-связи между этими же атомами углерода. Две π-
связи расположены над сферой действия σ-связи в двух взаимно перпендикулярных плоскостях.
Все шесть атомов углерода циклической молекулы бензола С6H6 лежат в одной плоскости. Между атомами углерода в плоскости кольца действуют σ-связи;
такие же связи имеются у каждого атома углерода с атомами водорода. На осуществление этих связей атомы углерода затрачивают по три электрона. Облака
четвертых валентных электронов атомов углерода, имеющих форму восьмерок, расположены перпендикулярно к плоскости молекулы бензола. Каждое такое облако
перекрывается одинаково с электронными облаками соседних атомов углерода. В молекуле бензола образуются не три отдельные π-связи, а единая π-
электронная система из шести электронов, общая для всех атомов углерода. Связи между атомами углерода в молекуле бензола совершенно одинаковые.
19.Гибридизация АО – это взаимодействие (смешение) разных по типу, но близких по энергии атомных орбиталей данного атома с образованием гибридных орбиталей одинаковой формы и энергии.
ТИПЫ ГИБРИДИЗАЦИИ
|
Тип гибридизации |
Геометрическая форма |
Угол между связями |
Примеры |
|
Sp |
линейная |
180o |
BeCl2 |
|
sp2 |
треугольная |
120o |
BCl3 |
|
sp3 |
тетраэдрическая |
109,5o |
CH4 |
|
sp3d |
тригонально-бипирамидальная |
90o; 120o |
PCl5 |
|
sp3d2 |
октаэдрическая |
90o |
SF6 |
|
|
|
|
|
\