
- •Рабочая учебная программа по дисциплине
- •Цель и задачи дисциплины
- •Тематическое содержание дисциплины
- •Тематика курсовых работ и методические указания по их выполнению.
- •Самостоятельная работа.
- •Литература
- •Информационное обеспечение дисциплины
- •Методические указания для студентов
- •1.1.Уравнение состояния газов.
- •1.2. I. Законы термодинамики.
- •1.3. Второй закон термодинамики. Энтропия.
- •Лекция №2.
- •1.4. Исследование основных термодинамических процессов идеальных газов в закрытых системах.
- •Лекция №3.
- •Лекция №4
- •Понятие об условном топливе,
- •Топочные устройства.
- •Общие сведения о котельных установках.
- •Лекция№ 5 теплопроводность твёрдых тел.
- •Способы передачи теплоты.
- •Закон фурье и коэффициент теплопроводности.
- •Перенос теплоты в режиме естественной и вынужденной конвекции. Понятие о теории подобия в теплотехнике. Введение.
- •Физические свойства жидкостей.
- •Краткие сведения из гидродинамики.
- •Подобие и моделирование процессов конвективного теплообмена.
- •Лекция №6 лучистый теплообмен. Понятие сложного теплообмена. Термическое сопротивление ограждающих конструкций здани
- •Основные законы лучистого теплообмена.
- •Термическое сопротивление наружных ограждений зданий.
- •Лекция №7 Современные системы отопления. Гигиенические требования. Классификация систем отопления.
- •Лекция №8
- •Лекция №9. Гигиенические основы вентиляции. Способы организации воздухообмена.
1.3. Второй закон термодинамики. Энтропия.
Величина интеграла
![]() есть количество теплоты подведённой в
термодинамическом процессе между
состояниями 1 и 2 зависит от пути
интегрирования. Из курса высшей математики
известно, что для выражения
есть количество теплоты подведённой в
термодинамическом процессе между
состояниями 1 и 2 зависит от пути
интегрирования. Из курса высшей математики
известно, что для выражения
![]() всегда можно найти
такую функцию β, которая сделает интеграл
всегда можно найти
такую функцию β, которая сделает интеграл
![]() не зависящим от
пути интегрирования. Функцию β называют
интегрирующим множителем. Р. Клаузиус
в Х1Х веке показал, что таким интегрирующим
множителем является функция
не зависящим от
пути интегрирования. Функцию β называют
интегрирующим множителем. Р. Клаузиус
в Х1Х веке показал, что таким интегрирующим
множителем является функция
![]() Умножая левую и правую части выражения
Умножая левую и правую части выражения
![]() на
на
![]() ,
получим:
,
получим:
![]() ,
,
Интегрируя (1.12):
![]() ,
эта величина не зависит
,
эта величина не зависит
От пути интегрирования при осуществлении термодинамического процесса между состояниями 1 и 2 идеального газа.
Функция s=![]() ,
здесь s
,
здесь s![]() -
постоянная интегрирования, Клаузиус
назвал её энтропией. Нернст и М. Планк
вначале ХХ века доказали, что
-
постоянная интегрирования, Клаузиус
назвал её энтропией. Нернст и М. Планк
вначале ХХ века доказали, что
![]() при T=0К.
В термодинамике представляет интерес
разность
при T=0К.
В термодинамике представляет интерес
разность
![]()
Лекция №2.
1.4. Исследование основных термодинамических процессов идеальных газов в закрытых системах.
Исследование термодинамических процессов идеальных газов осуществляется в следующей последовательности: выводится уравнение процесса, связывающее начальные и конечные параметры рабочего тела в данном процессе; работа изменения объёма газа, количество теплоты подведённой к газу; изменение внутренней энергии и энтропии термодинамической системы.
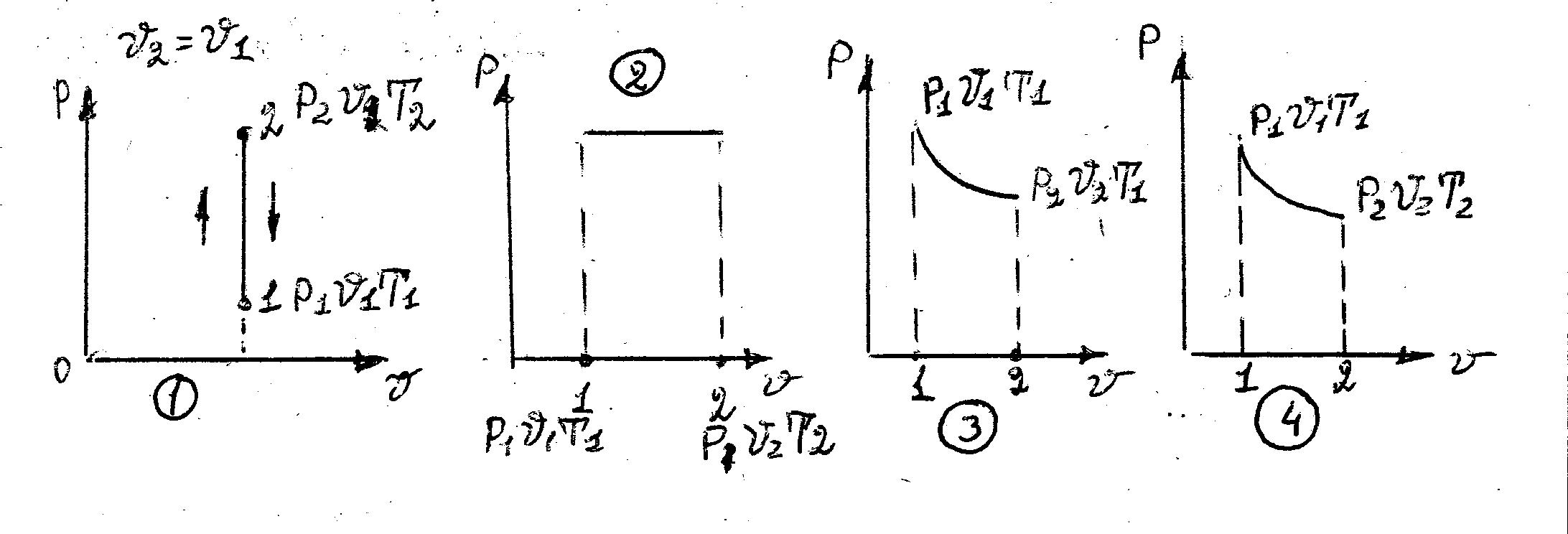
Изохорный процесс.
Условие протекания
процесса v=const;
согласно уравнению состояния идеального
газа р/T=R/v=const.
Работа в процессе dl=рdv=0,
при с![]() =const
=const

Если с![]() ,
т.к. dl=0,
то
,
т.к. dl=0,
то
![]()
Следовательно
![]() .
.
![]() .
.
Изобарный процесс.
Р=const.
![]() ,
закон Гей-Люссака,
,
закон Гей-Люссака,
![]() ,
количество теплоты
,
количество теплоты
в этом процессе
найдём при условии
![]()

изменение внутренней
энергии в процессе
![]()
Если записать
первый закон термодинамики
 Изотермический
процесс.
Изотермический
процесс.
Pv=RT=const,
т.е.
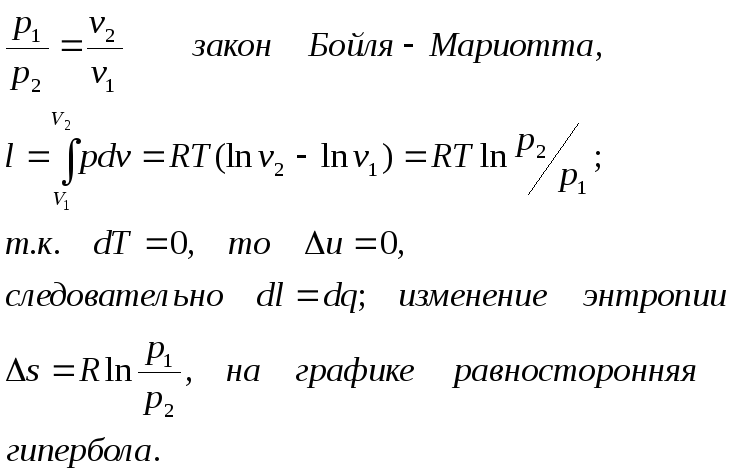
Адиабатный процесс.
Условие адиабатного процесса dq=0. Воспользуемся соотношением:

Политропный процесс.
![]()
![]() ,
,
воспользовавшись уравнением Клапейрона, запишем:
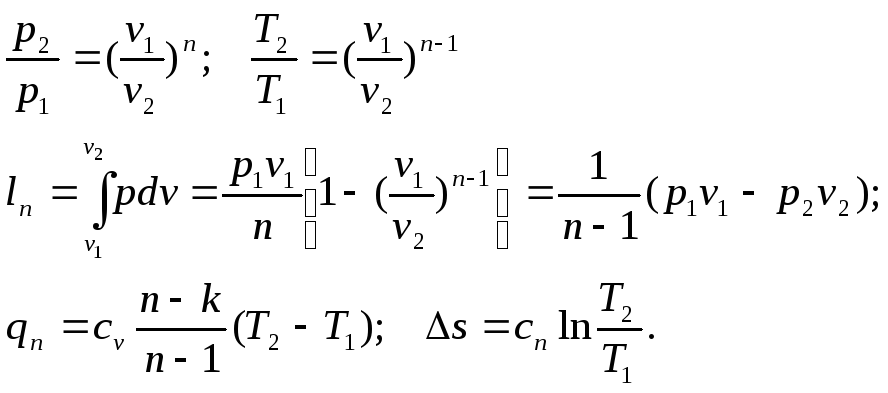
Цикл Карно.
Чем больше тепла в прямом термодинамическом цикле превращено в полезную работу и чем меньше её передано теплоприёмнику, тем цикл более экономичен и тем, следовательно, выше его термический КПД.

Максимальное значение термического КПД было определено С. Карно в 1827 г., французским инженером. Цикл рассматривается в координатах
p-v.
В начальный момент параметры рабочего
тела
![]() начинается изотермический процесс
расширения рабочего тела за счёт подвода
теплоты
начинается изотермический процесс
расширения рабочего тела за счёт подвода
теплоты
![]() до
точки 2, при этом работа, совершённая в
изотермическом процессе, определяется
фигурой 1-2-6-8-1. Далее идёт разобщение
рабочего тела с теплоотдатчиком и
процесс 2-3 адиабатное расширение –
работа 2-3-5-6-2; в положение т.3 поршень
займёт крайнее правое положение. В т.3
происходит общение рабочего тела с
теплоприёмником, имеющим температуру
T
до
точки 2, при этом работа, совершённая в
изотермическом процессе, определяется
фигурой 1-2-6-8-1. Далее идёт разобщение
рабочего тела с теплоотдатчиком и
процесс 2-3 адиабатное расширение –
работа 2-3-5-6-2; в положение т.3 поршень
займёт крайнее правое положение. В т.3
происходит общение рабочего тела с
теплоприёмником, имеющим температуру
T![]() ,
т.е. имеет место изотермическое сжатие
– работа 3-5-7-4-3 – отрицательная работа.
В т.4 процесс заканчивается и далее идёт
процесс адиабатного сжатия по адиабате
4-1. В конце процесса рабочее тело принимает
первоначальные параметры. Работа
адиабатного сжатия 1-4-7-8-1. Общее выражение
термического КПД имеет вид:
,
т.е. имеет место изотермическое сжатие
– работа 3-5-7-4-3 – отрицательная работа.
В т.4 процесс заканчивается и далее идёт
процесс адиабатного сжатия по адиабате
4-1. В конце процесса рабочее тело принимает
первоначальные параметры. Работа
адиабатного сжатия 1-4-7-8-1. Общее выражение
термического КПД имеет вид:

В цикле Карно имеет равенство объёмов, т.е.
![]()
Тогда:
![]() .
.
Для современных материалов η=0,7-0,8,
для холодильных
машин
![]()
Понятие об энтропии газа.
Рассмотрим на рисунке обратимый процесс 1-2. Разобьём его на отдельные участки, на каждом из которых T=const, подводимая теплота dq. Величину dq/T называем приведенной теплотой и дадим обозначение ds:
![]()
Взяв интеграл на участке 1-2, получим выражение:
![]()
Из первого закона термодинамики:


В координатах T-s можно определить количество теплоты, затрачиваемое на осуществление любого термодинамического процесса. Для адиабатного процесса s=const и в T-s координатах цикл Карно есть прямоугольник и соответственно:
![]()
Водяной пар.
Водяной пар широко используется в теплотехнике как рабочее тело и теплоноситель. Его состояние близко к насыщению и не подчиняется законам для идеальных газов. Для реальных газов наиболее простым является уравнение Ван-дер-Ваальса, предложенное в 1873 г.
![]()
![]() ,
,
a – коэффициент, зависящий от сил сцепления;
b – величина, учитывающая собственный объём молекул.
Для водяного пара с поправкой на ассоциацию и диссоциацию получили уравнение М.П. Вукалович и И.И. Новиков в 1939 г.

где с и m – опытные коэффициенты.
Чем больше v, тем ближе к состоянию идеального газа наш реальный газ – водяной пар в воздухе в частности. В этом случае можно пользоваться уравнением Клапейрона.
Поршневые двигатели внутреннего
сгорания.
Тепловые двигатели, в которых топливо сгорает внутри рабочего цилиндра, называются поршневыми двигателями внутреннего сгорания. Преобразование тепловой энергии в механическую в них осуществляется посредством передачи работы расширения продуктов сгорания топлива через поршень и кривошипно-шатунный механизм на коленчатый вал двигателя.
Классификация двигателей осуществляется по следующим основным признакам:
-
4-тактные и 2-тактные;
-
По способу смесеобразования и воспламенения рабочей смеси;
-
По роду топлива;
-
По назначению;
-
По конструктивному исполнению.
ИДЕАЛЬНЫЕ ЦИКЛЫ ДВС.
Действительный
рабочий процесс заменим идеальным –
процесс сгорания заменим подводом
теплоты извне
![]() ,
процесс перезарядки цилиндров –
теплоотводом
,
процесс перезарядки цилиндров –
теплоотводом
![]() .
Цикл, таким образом, становится круговым,
замкнутым.
.
Цикл, таким образом, становится круговым,
замкнутым.
Рабочее тело – 1 кг идеального газа, изменение теплоёмкости которого не учитывается при осуществлении цикла. Эти допущения позволяют считать, что двигатели работают по обратимым термодинамическим циклам и результаты исследования можно применять при изучении тепловых процессов в двигателях, вводя поправочные коэффициенты.
Рассмотрим три способа подвода теплоты к рабочему телу в циклах ДВС.

Циклы поршневых двигателей внутреннего сгорания
в координатах p-v.
Цикл «а» представляет
собой автомобильный цикл с изохорным
подводом теплоты. 1-2 адиабатное сжатие,
2-3 изохорный подвод теплоты q![]() ,
повышение давления до точки 3, как
следствие этого. Затем адиабатное
расширение 3-4 и, наконец, изохорный
процесс отвода теплоты
,
повышение давления до точки 3, как
следствие этого. Затем адиабатное
расширение 3-4 и, наконец, изохорный
процесс отвода теплоты
![]() ,
т.е. приходим в исходное состояние.
Термический к.п.д. такого цикла определяется
по формуле:
,
т.е. приходим в исходное состояние.
Термический к.п.д. такого цикла определяется
по формуле:
![]()
где
![]() степень сжатия рабочего тела. Для цикла
«б» (цикл Дизеля, предложенный в 1897 г.)
аналогичный к.п.д найдём по формуле:
степень сжатия рабочего тела. Для цикла
«б» (цикл Дизеля, предложенный в 1897 г.)
аналогичный к.п.д найдём по формуле:
![]()
где
![]() степень предварительного расширения.
степень предварительного расширения.
Цикл со смешанным подводом теплоты, «в», более экономичен:
![]()
где
![]() степень
повышения давления.
степень
повышения давления.
Действительный процесс и индикаторная диаграмма двигателей внутреннего сгорания.
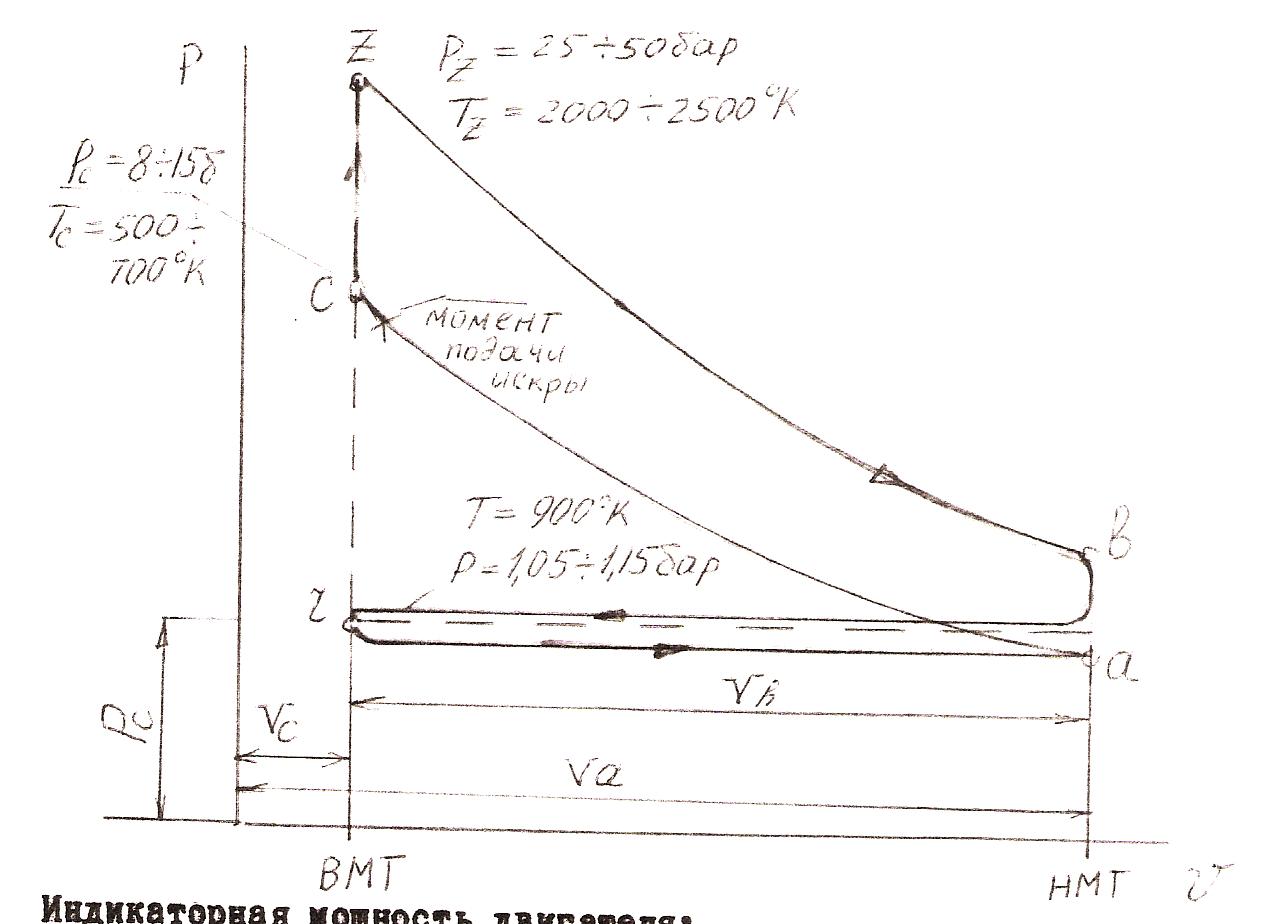
Индикаторная мощность двигателя:
![]()

![]()
![]()
![]()
литровая мощность
двигателя соответственно:
![]()
полнота использования
теплоты:
![]()
для карбюраторных
![]()
Удельный эффективный расход топлива:
 ,
,
![]()
