
- •Математический маятник
- •3)Лагранжев подход
- •1.1. Гармонические колебания
- •1.2. Векторная интерпретация и комплексное представление
- •1.3. Модулированные колебания
- •Сложение колебаний. Векторные диаграммы. Биения.
- •Сложение колебаний Векторная диаграмма
- •3.4.Анализ колебаний маятника на основе равенства сил, моментов и сохранения энергии
- •2.4. Гармонический осциллятор и его характеристики
- •3.3. Солитонное решение уравнения для осциллятора с нелинейностью синуса
- •2.5. Гармонический осциллятор и уравнение Шредингера.
- •2.6. Цепочка осцилляторов и уравнение Клейна-Гордона-Фока(укгф)
- •Уравнение распространения волн в газовой среде.
- •11.2. Гармоническая волна
- •11.3. Волны в пространстве
- •1. Распространение волн в среде
- •§ 2. Уравнения плоской и сферической волн
- •§ 3. Уравнение плоской волны, распространяющейся в произвольном направлении
- •§ 4. Волновое уравнение
- •§ 5. Скорость упругих волн в твердой среде
- •§ 6. Энергия упругой волны
- •§ 7. Стоячие волны
- •Адиабатический процесс.
- •Термодинамические потенциалы.
- •Раздел I. Термодинамика
- •Тема 1. Введение. Основные понятия и определения.
- •1.1 Введение
- •1.2. Термодинамическая система.
- •1.3. Параметры состояния.
- •1.4. Уравнение состояния и термодинамический процесс.
- •Тема 2. Первый закон термодинамики.
- •2.1. Теплота и работа.
- •2.2. Внутренняя энергия.
- •2.3. Первый закон термодинамики.
- •2.4. Теплоемкость газа.
- •2.5. Универсальное уравнение состояния идеального газа.
- •2.6. Смесь идеальных газов.
- •Тема 3. Второй закон термодинамики.
- •3.1. Основные положения второго закона термодинамики.
- •3.2. Энтропия.
- •3.3. Цикл и теоремы Карно.
- •Тема 4. Термодинамические процессы.
- •4.1. Метод исследования т/д процессов.
- •4.2. Изопроцессы идеального газа.
- •4.3. Политропный процесс.
- •Тема 5. Термодинамика потока.
- •5.1. Первый закон термодинамики для потока.
- •5.2. Критическое давление и скорость. Сопло Лаваля.
- •5.3.Дросселирование.
- •Тема 6. Реальные газы. Водяной пар. Влажный воздух.
- •6.1. Свойства реальных газов.
- •6.2. Уравнения состояния реального газа.
- •6.3. Понятия о водяном паре.
- •6.4. Характеристики влажного воздуха.
- •Термодинамика Элементы статистической физики.
- •Закон Фика и уравнение диффузии.
- •Закон Ньютона для вязкого трения.
- •5.10. Вывод закона Фурье
- •1) Введенная величина f есть свободная энергия системы,
- •3) Параметр θ пропорционален абсолютной температуре т:
- •2.16. Большое каноническое распределение и термодинамика систем с переменным числом частиц
- •Двухатомный газ с молекулами из одинаковых атомов. Вращение молекул.
- •9.1. Бозоны и фермионы. Принцип Паули
Термодинамика Элементы статистической физики.
![]()
Вероятность:
![]()
При
подбрасывании монеты
![]() раз вероятность выпадения орла или
решки приближается к
раз вероятность выпадения орла или
решки приближается к
![]()
Игральные кости:

![]() ;
;
![]() ;
;
![]() ;
… ;
;
… ;
![]() ;
;
![]() ;
Вероятность невозможного события равна
нулю.
;
Вероятность невозможного события равна
нулю.
![]() Вероятность
достоверного события равна единице.
Вероятность
достоверного события равна единице.
![]() ;
;
![]() ;
;
![]() - формула сложения
вероятностей.
- формула сложения
вероятностей.
![]() ;
;
![]() .
.
Вероятность нахождения частицы в этих двух объемах:
![]()
![]()
Лекция № 15
![]()
![]() ;
;
![]()
![]() - функция распределения
случайной величины (вероятности).
- функция распределения
случайной величины (вероятности).
Пример. Игральные кости

![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;![]() ;
;
![]()
Пример. Циферблат часов

![]() ;
;
![]()

Таким
образом, функция
![]() примет вид:
примет вид:

![]() изменяется до
изменяется до
![]()
![]() - плотность
вероятности.
- плотность
вероятности.
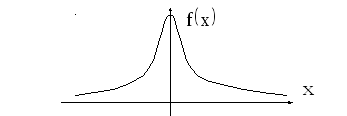
Распределение плотности вероятности(распределение Гаусса)
Рассмотрим
систему случайного движения точки в
плоскости
![]() .
.
Из точки О скачками движется частица. Каждый шаг –равновероятен по всем направлениям, а его величина распределена по произвольному закону. Шаги независимы. Задача-получить распределение координат точки после большого числа шагов. Поскольку движение по обеим координатам независимы, смещения в положительном и отрицательном направлениях равновероятны. Чтобы исключить влияние направления рассматривается зависимость от квадрата координаты.

Плотность вероятности для точки иметь координату х зависит от х2, т.е. равна φ1(x2), аналогично для y φ2(y2). Вероятность нахождения точки в элементе площади dxdy с координатами x и y равна
dp = φ1(x'2)φ2(y2)dxdy
При повороте системы координат, так, чтобы ось x' прошла через элементарную площадку. При этом связь координат имеет вид
x'2 = x2 + y2
При этом вероятность нахождения точки в элементе площади dxdy с новыми координатами равна
dp = φ1(x'2)dxdy
Это одна и та же величина поэтому можно записать
φ(x'2) = φ1(x'2)φ2(y2) = φ(x2 + y2) – функциональное уравнение
Решаем функциональное уравнение используя свойства и структуру уравнения. Для этого логарифмируем это уравнение
![]()
![]() ;
;
Дифференцируем полученное выражение по x2 , и по y2
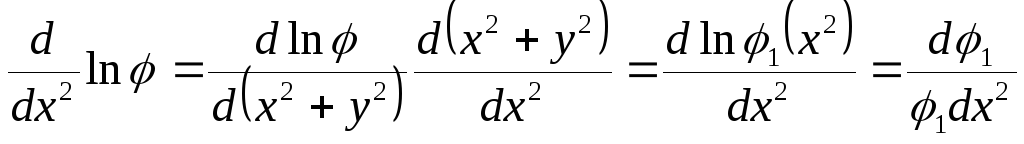 ;
;
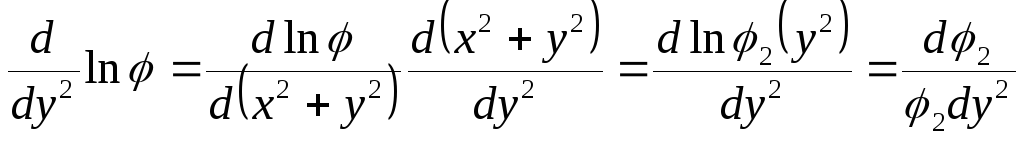 ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]()
Распределение Гаусса.

Доска Гальтона.



………………………….
………………………….
………………………….
…
 ……………………….
……………………….
………………………….
………………………….
………………………….

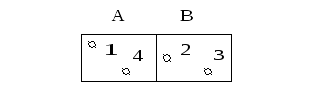
Назовем микросостоянием заданные состояния всех молекул.
Макросостояние
– состояние при заданных макропараметрах.
![]() ,
число молей и т.д.
,
число молей и т.д.
Макросостояние реализуется различными способами или микросостояниями.
Число микросостояний, характеризующих данное макросостояние, называется статистическим весом макросостояния.
Вероятность пребывания 1 молекулы в части А(поскольку равновероятно в А или в В – вероятность пребывания в А равна ½)
Вероятность одновременного пребывания в А двух молекул равна произведению ½ *1/2 (события независимы)
Вероятность одновременного пребывания в А 4-х молекул равна (1/2)4 =1/16.
Поскольку вероятность попадания в объем пропорциональна объему, то
Р(VA) =VA/( VA + VB) – вероятность попадания молекулы в объем А.
Р1(VA) =(VA/( VA + VB))N –вероятность попадания N молекул в объем А.
Р2(VB) =(VB/( VA + VB))N – вероятность попадания N молекул в объем В.
Возможные распределения молекул по половинкам А и В
|
Способы реализации системы макросостояний |
Число способов-реализаций состояния
|
Вероятность события |
|
|
A |
B |
Г |
p |
|
- |
1234 |
1 |
1\16 |
|
1 2 3 4
|
234 134 124 123
|
4
|
1\4 |
|
12 13 14 23 24 34 |
34 24 23 14 13 12
|
6 |
6\16
|
|
123 124 134 234
|
1 2 3 4 |
4 |
1\4 |
|
1234 |
- |
1 |
1\16 |
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]() ;
;
![]() ,
где
,
где
![]() - количество частиц.
- количество частиц.
макросостояниях
Статистический смысл энтропии
Запишем для энтропии
![]() ;
;
Поскольку из уравнения состояния идеального газа для одного моля следует
![]() ;
;
Перепишем уравнение для энтропии
![]() ;
;
Или интегрируя
![]()
При постоянной температуре
![]() ;
;
Изменение энтропии логарифмически зависит от объема или точнее от отношения объемов
![]() ;
;
![]() ;
;
Поскольку число микросостояний пропорционально объему
![]()
![]() - энтропия –логарифм
числа микросостояний -формула Больцмана.
- энтропия –логарифм
числа микросостояний -формула Больцмана.
![]() - уравнение
Больцмана.
- уравнение
Больцмана.
Чем более упорядочена система, тем меньше число микросостояний, характеризующих данное макросостояние.
Если все атомы закреплены в определенных местах, тогда существует единственное микросостояние и энтропия равна нулю.
Состояние с максимальной энтропией является наиболее вероятным состоянием.Энтропия –мера разупорядоченности(беспорядка, хаоса) системы.
В состоянии равновесия энтропия максимальна и это состояние наиболее вероятно.
Если система предоставлена сама себе, то она будет стремиться к равновесию.
Плотность вероятности(объемная интерпретация)
Объем разбивается на части Vi. Вероятность нахождения частицы в объеме ∆Vi
P(∆Vi) = limN->∞ (Ni/N)
Ni - число испытаний, когда частица обнаружена в объеме ∆Vi , N – общее число испытаний
Плотность вероятности
Вероятность нахождения молекулы в бесконечно малом объеме, отнесенная к объему.
f(x,y,z) = lim∆V->0 P(∆Vi)/∆Vi = lim∆V->0 N->∞ (Ni/(∆ViN)) – вероятность нахождения молекулы в бесконечно малом объеме, отнесенная к объему.
По аналогии с плотностью вещества
ρ= lim∆V->0 (∆m/∆V)
Если провести N0 наблюдений, то в объеме ∆V в окрестности точки x,y,z молекула будет обнаружена в
dN = N0f(x,y,z)dV = N0f(x,y,z)dxdydz
случаях. В конечном объеме V1 – молекула окажется обнаруженной
N(V1) = N0 ∫V1f(x,y,z)dxdydz - раз.
Вероятность P((V1) быть обнаруженной при наблюдении в объеме V1 для молекулы
P((V1) = N(V1)/N0 =∫V1f(x,y,z)dxdydz
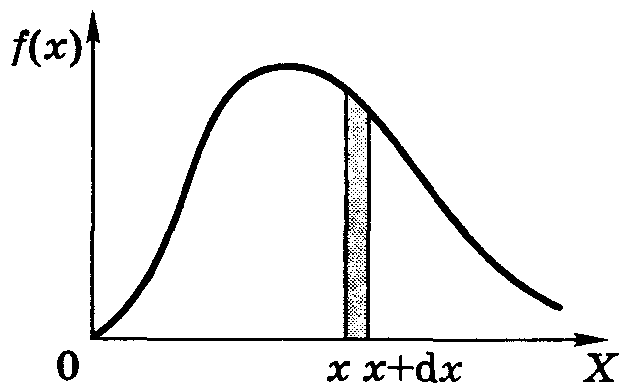
В пределе получим условие нормировки
P((V1->∞) = N(V1->∞)/N0 =∫V1->∞f(x,y,z)dxdydz =1 – условие нормировки плотности вероятности
Для замкнутого объема
∫VfdV=1
Если положения молекулы равноценны, то f0 =const. Из условия нормировки следует
∫Vf0 dV=1 =f0V=1
Тогда
f0=1/ V
в этом случае
N(V1) =N0 ∫V1f0dV = N0 V1/V
P(V1) = N(V1) /N0 = V1/V(что справедливо для постоянной плотности вероятностей)
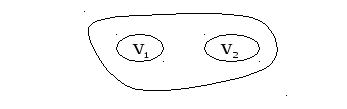
Сложение вероятностей независимых событий
P(V1+V2) = (V1+V2)/V = V1/V+V2/V = P(V1)+P(V2)
Что интерпретируется как или в объеме V1 или в объеме V2. Объемы или множества непересекающиеся.
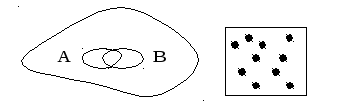
В общем случае при зависимости событий
P(A+B) = P(A) +P(B) - P(AB)
Где
P(AB) = NAB/N
В объемной интерпретации
P(V1+V2) = (V1+V2 –V12)/V = P(V1)+P(V2) –P(V12)
Условная вероятность
Условная вероятность – это вероятность события A при условии, что произошло событие B – обозначается как P(A/B). Например, вероятность вытащить белый шар из урны при условии, что вытащен черный шар.
Поскольку общее число исходов испытаний при которых произошло событие B, равно NB а из него в NAB случаях произошло событие A, то
P(A/B) = NAB/N
Переходя на континуальное рассмотрение условная вероятность P(V1/V2) нахождения частицы в объеме V1 в случае если она находится в объеме V2 , сводится к вычислению вероятности нахождения частицы в объеме V1 , в случае, если она находится в объеме V2, поэтому
P(V1/V2) =V12/V2
Преобразуем
P(A/B) = (NAB/N)/(NB/N) = P(AB)/P(B)), P(AB) – вероятность совместного наступления событий A и B.
Тогда
P(AB) = P(B) P(A/B) = P(A) P(B/A) – формула умножения вероятностей
Для независимых событий
P(A/B) = P(A)
P(AB) = P(A) P(B)
Вероятность микросостояния
Ра = Га/Г0
Га – число микросостояний –термодинамическая вероятность
Г0 – общее число состояний, достижимых для системы
Формулы комбинаторики
Теория размещений
Задача 1
n -мест, n - различных предметов
Число способов размещения n предметов по n местам!
Один предмет –на n мест - n способов
Второй предмет на оставшиеся n -1 мест –поэтому 2 предмета n(n -1) –способов
3 предмета n(n -1)(n-2) способов
n На n - n! способов n(n -1)(n -2)….1 = n!
На 3х стульях 3 человека 3! –способов
Задача 2
m -различных предметов, n - мест
Число способов размещения m предметов по n местам!
Если разместить m предметов, то n-m мест свободны
Если бы эти n –m мест были бы заняты различными предметами, то при каждом фиксированным раcположении m предметов их можно было бы разместить (n -m)! Способами. Если перебрать все возможные размещения m по n местам и при каждом из них произвести (n -m)! Размещений n-m других предметов на оставшихся n - m местах, то всего получается число различных размещений m+(n - m) = n различных предметов по различным местам, т.е. n!
Следовательно, искомое число способов размещения m предметов по n различным местам
Р(n, n - m) = n!/(n - m)!
|∆□_ |□_∆ | _∆□ | ∆_□ |□∆_ | _□∆|
Задача 3
m По n, но m -одинаковые и неразличимые
|∆∆_ |∆_∆ | _∆∆|
Размещения, когда поменялись местами два предмета считаются одинаковыми. В этом случае при каждом размещении предметов можно произвести ! перестановок, которые не изменят размещения. Следовательно, искомое число способов
C(n,m) = n!/[m!(n-m)!]
Задача 4
Сколько способов выбора!
n - различных предметов, m - предметов, отличающихся по составу( n- вагонов m - студентов)
∆□○ n=3 m=2
|∆□|∆○|□○|
Если предмет в группе 1, то n -способов, если 2, то n(n-1) -способов, каждый из различных предметов комбинируется с (n-1) оставшимися.
Комбинации, отличающиеся лишь порядком, одинаковы. Число перестановок для 2-х 2! И тогда n(n-1)/2!
Для m
C(n,m)
=![]()
Расчет вероятности макросостояния
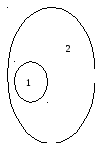 N,V,n
N,V,n
1- N1, V1,m
2-N-N1, V- V1,n-m
V – объем идеального газа
n-число частиц диаметром d в этом объеме V1 находится n -частиц
N = V/d3 Где d3 ≈10-30m3
Всегда соблюдается условие N>>n
Вероятность макроскопического состояния системы, при котором в объеме V1 m -
V1 содержит ячеек больше чем m
N1 = V1/ d3 , поэтому N1 ≥ m
Общее число микросостояний равно, числу способов которыми можно разместить n -частиц по N ячейкам. Предполагается, что частицы отличаются друг от друга(пронумерованы). Свойства частиц одинаковы и если обмен частицами произошел, то состояние не поменялось, но микросостояния различны !!!!
Число микросостояний Г0 = N!/(N-n)!
Число микросостояний, посредством которых реализуется макросостояние, когда в объеме V1 имеется m каких-то частиц
g(V1, m) = N1!/(N1 -m)!
В остальной части объема V - V1 содержится n-m остальных частиц. Число микросостояний для них
g(V - V1, n-m) =(N-N1)!/[N-N1 –(n-m)]!
Т.о. для конкретных частиц в объеме V1 общее число микросостояний
g(V1, m)g(V - V1, n-m), поскольку каждое микросостояние в V1 комбинируется со всеми состояниями в V -V1. но произведение не дает всех микросостояний поскольку это только для некоторого набора m -частиц в объеме V1. но m частиц из общего числа n частиц можно выбрать n!/[m! (n-m)!] Способами. Поэтому общее число микросостояний
Г(V1,
m) =
![]() g(V1,m)
g(V - V1,
n-m)
g(V1,m)
g(V - V1,
n-m)
Следовательно, вероятность макросостояния
Р(V1,
) = Г(V1, )/Г0 =![]()
![]()
Для газа при нормальных условиях V=1см3, n≈1019 , N≈1024, N1 =1024(V1 /V)
При этом N1 >>m
ln n! = ln1 + ln2 + ln3 + ….lnn = ∑1,nlnn∆n, ∆n = 1
ln n! ≈∫1n lnndn = nln n – n, 1 n→∞ ∆n → 0
n! =enlnn-n = enlnne-n =nn/en = (n/e)n
Преобразуем формулу вероятности макросостояния с использованием формулы Стирлинга
N>>m, N – N1 >> n-m, N>>n
Тогда
(N1
- m)! =
![]() =
=![]() =
=![]() e-m
e-m
Где учтено, что limn→∞ (1+x/n)n =ex
Аналогично все факториалы, тогда
P(V1,
m) =
![]()
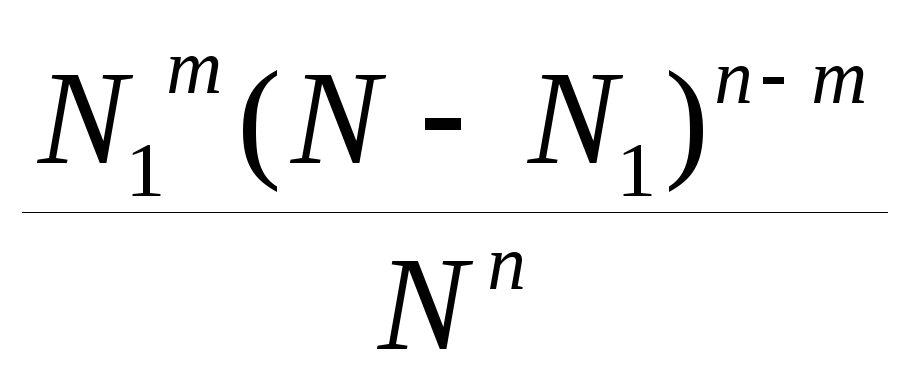 =
=![]()
![]()
Смысл формулы
Р
=
![]() =
=![]() - вероятность нахождения частицы в
объеме V1
- вероятность нахождения частицы в
объеме V1
_q=1-N1/N = 1-p – вероятность нахождения частицы в остальной части объема V-V1
Сумма вероятностей
p+q =1, поскольку частицы или в V1 или в V-V1
тогда для вероятности
P(V1,
m) =
![]() рmqn-m
–биноминальное распределение
рmqn-m
–биноминальное распределение
Физический смысл энтропии
Из первого закона термодинамики запишем
![]()
Поскольку
p/T = R/V
и, кроме того,
dT/T = dlnT dV = dlnV
дифференциал энтропии запишем
dS = d(cvlnT + RlnV), причем для изотермы T=const
имеем
dS = RlnV
или
∆S=lnV2/V1
Число частиц в 1 моле – это число Авогадро NA
Число состояний системы
Г01
=
![]()
Г02
=
![]()
Где N1 = V1/l3 , N2 = V2/l3
_l =10-10 m - размеры частиц
Используя формулу стирлинга
![]() =
=
![]() ≈
≈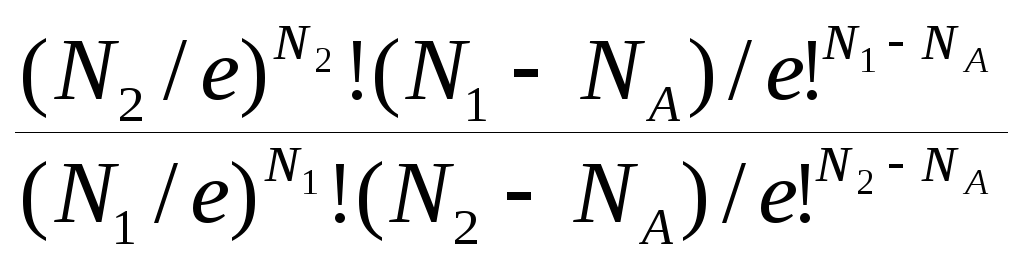
Для разреженного газа
N1 >>NA , N2 >>NA
Тогда приближенно но с большой точностью
![]() =
=
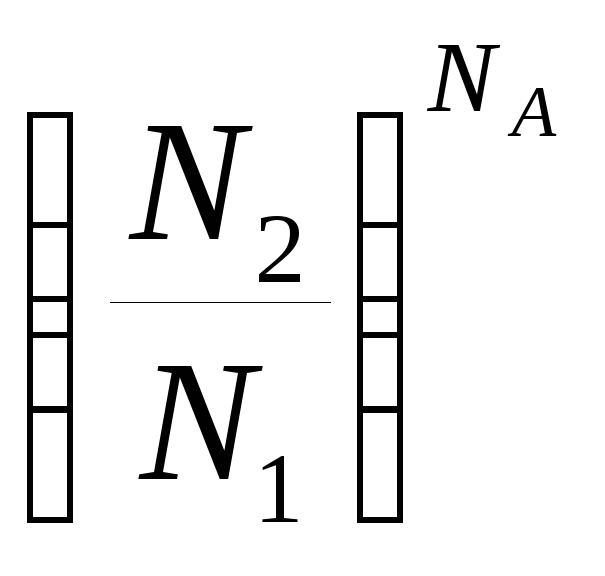 =
=![]()
![]()
∆S
=S2 –
S1 =![]() = kln Г02
-kln Г01
= kln Г02
-kln Г01
R/NA = k –
Таким образом энтропию можно интерпретировать как логарифм числа микросостояний
S = kln Г –формула Больцмана
Чем более упорядочена система, тем меньше число микросостояний, которыми реализуется макросистема. Если все атомы закреплены в определенных местах, тогда существует одно микросостояние, а соответственно, энтропия равна 0. чем больше микросостояний Г->0, тем более разупорядочена система. Энтропия – мера разупорядоченности(беспорядка, хаоса) системы.
В состоянии равновесия S -max, наиболее вероятное состояние.
Система, предоставленная самой себе движется к равновесию.
Все процессы в природе стремяться к равновесию.
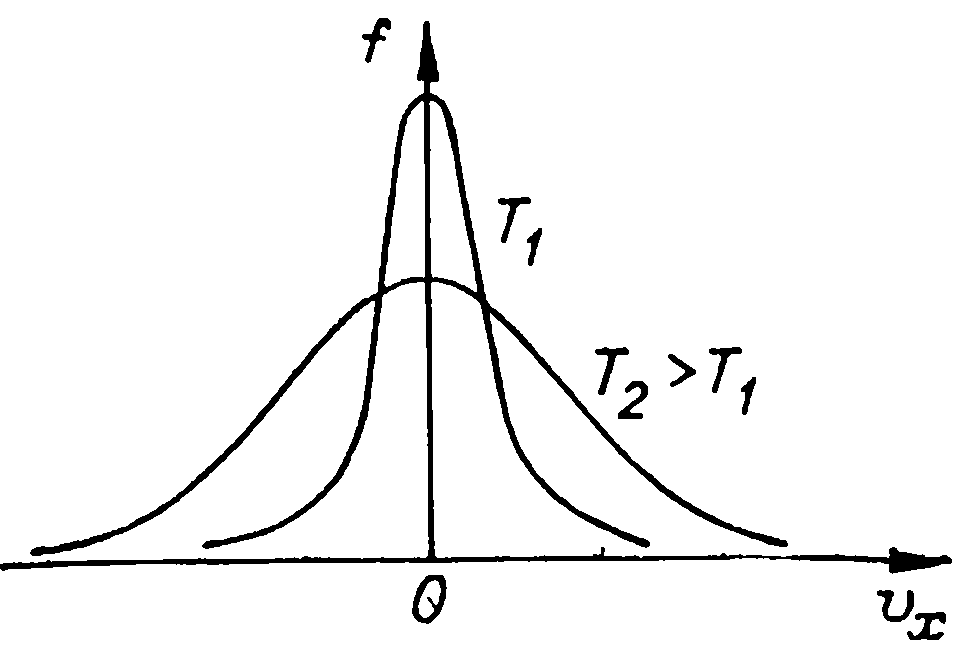
Тема: распределение Максвелла – Больцмана
Физическое содержание вопроса: молекулы хаотически движутся, для них характерен вероятностный подход
Цель: получить зависимость доли частиц, имеющих скорости в диапазоне от м до м+ вм(вероятность)
Задачи, вытекающие из цели: 1.выразить вероятность
2. проинтегрировать
3.проанализировать
4.практически применить
Метод решения: решение функциональных уравнений(логарифмируя и дифференцируя, затем интегрируя полученную зависимость путем сведения к произведению интегралов и переходу к полярным координатам
2-й метод- переход к сферическому слою
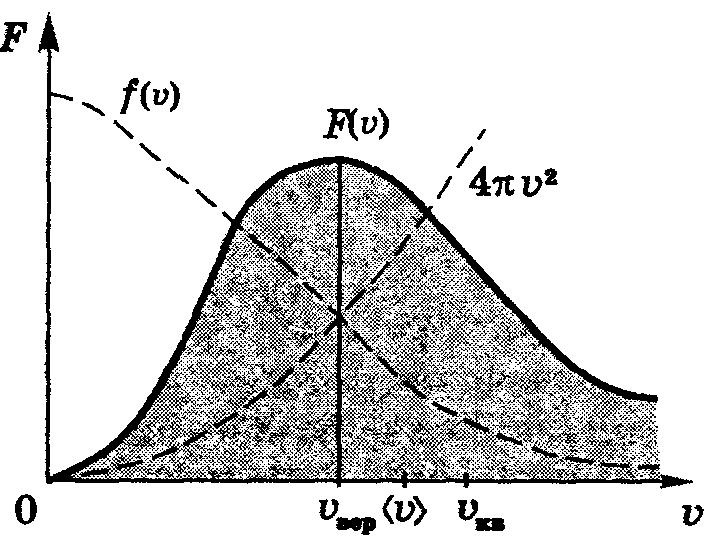
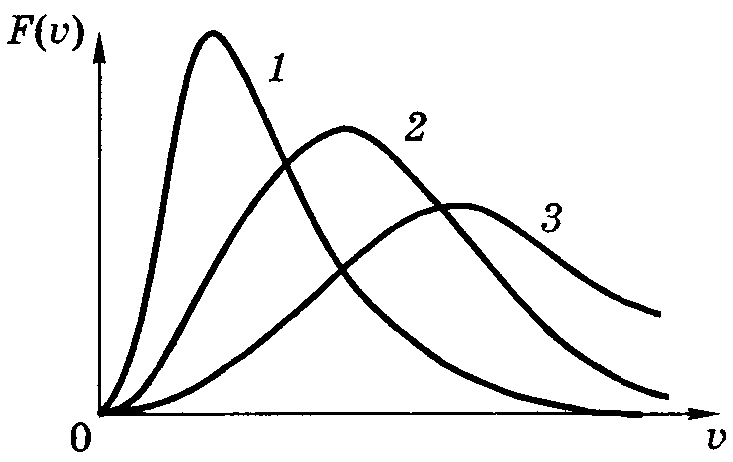
Выводы: график, есть максимум. Есть крылья. Можно получить наиб вероятную скор., ср скор., ср квадратичную скор.
Практические примеры: расчет доли молекул в диапазоне наиб вер скор
Распределение Максвелла.
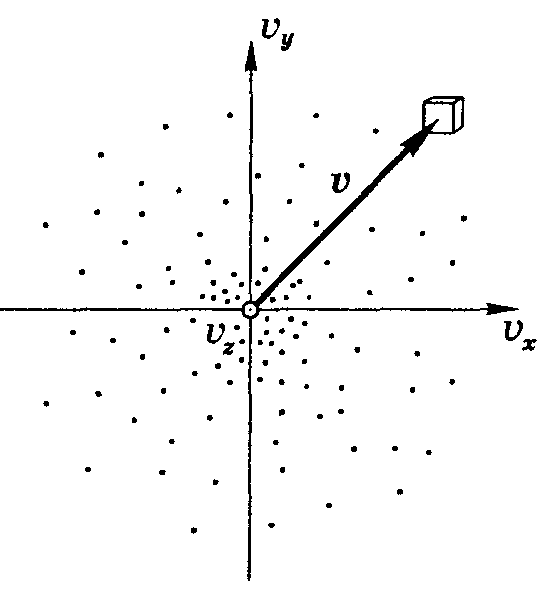
Из Бурштейна
Иродов
![]() до
до
![]()
Получить функцию распределения вероятности молекул по скоростям.
Допущения при выводе формулы:
-
скорости молекул равновероятны, имеют различные значения
скорости молекул равнонаправлены по всем координатам при различных значениях.
-
составляющие скорости независимы.
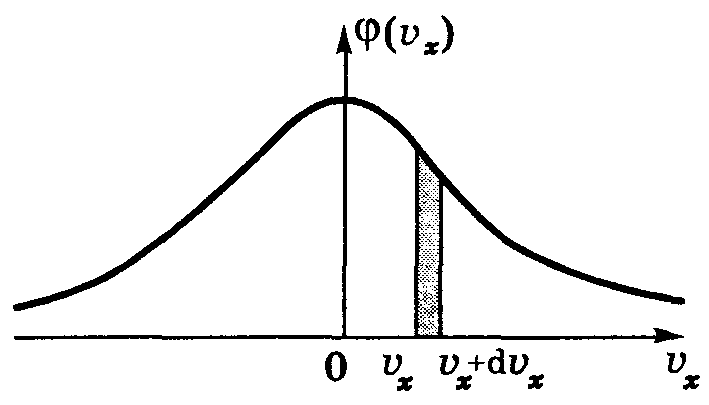
![]() - вероятность того,
что молекула имеет скорость в пределах
от
- вероятность того,
что молекула имеет скорость в пределах
от
![]() до
до
![]()
выражается через плотность распределения в виде
![]()
Аналогично для другой координаты
![]()
Аналогично для 3-ей координаты
![]()
Вероятность одновременного попадания трех компонент скорости в соответствующий интервал
dω = ω1ω2ω3
Вероятность зависит от квадрата скорости, чтобы знак скорости не влиял
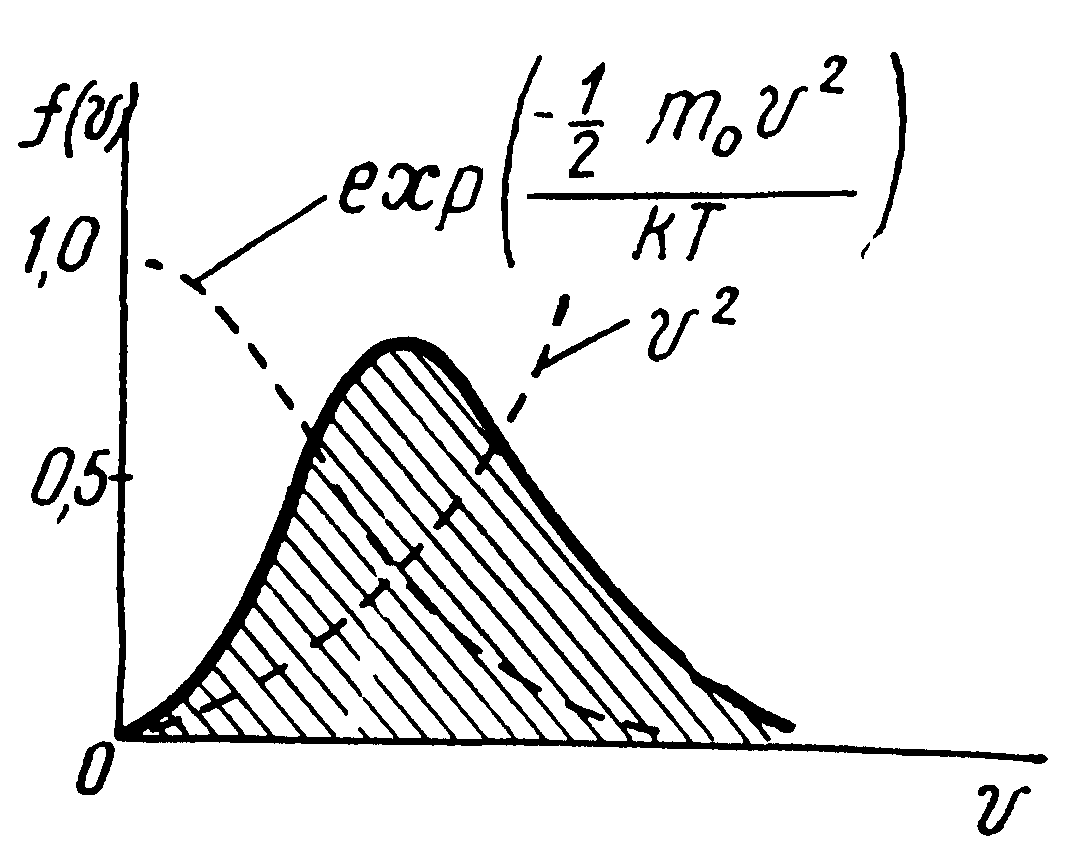
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Под квадратом вектора скорости понимается зависимость от компонент по формуле
![]() ;
;
С другой стороны
![]() ;
;
Или
![]() ;
;
Откуда следует функциональное уравнение
![]()
![]()
![]()
![]() ;
;
Логарифмируя
![]()
![]()
![]()
![]()
Решаем функциональное уравнение, дифференцируя по компонентам скорости

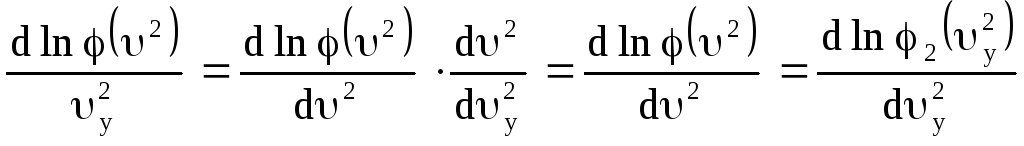
И т.д.
Учитывая, что производная от квадрата скорости по квадрату компонента скорости равна 1, и, следовательно, равны между собой покомпонентные производные, можно приравнять покомпонентные производные одной постоянной величине
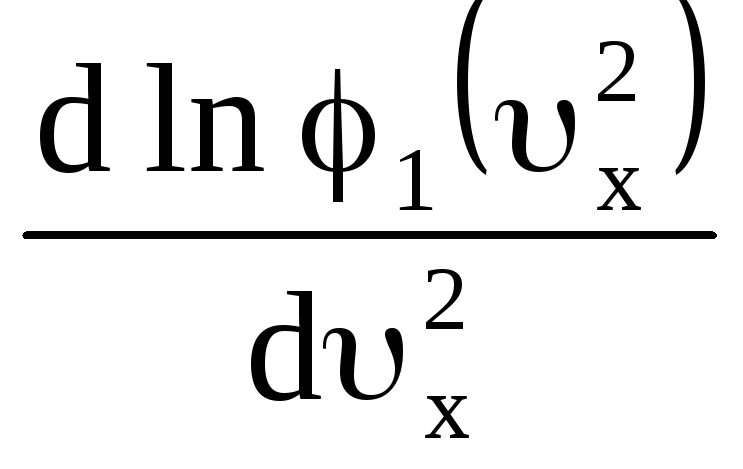
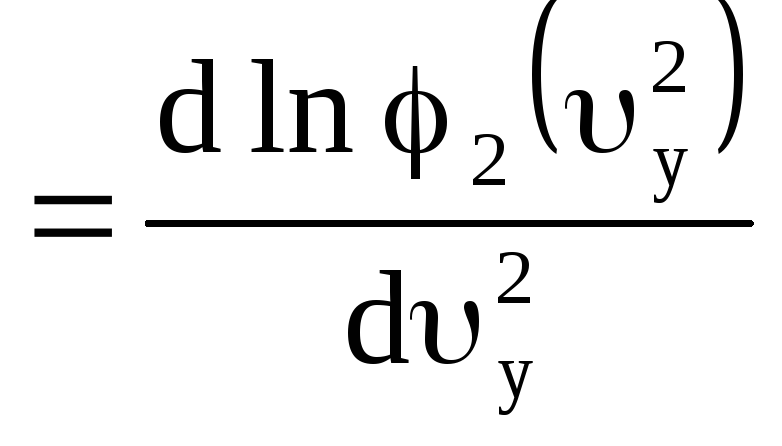 ;
;
Приравниваем постоянной эти уравнения
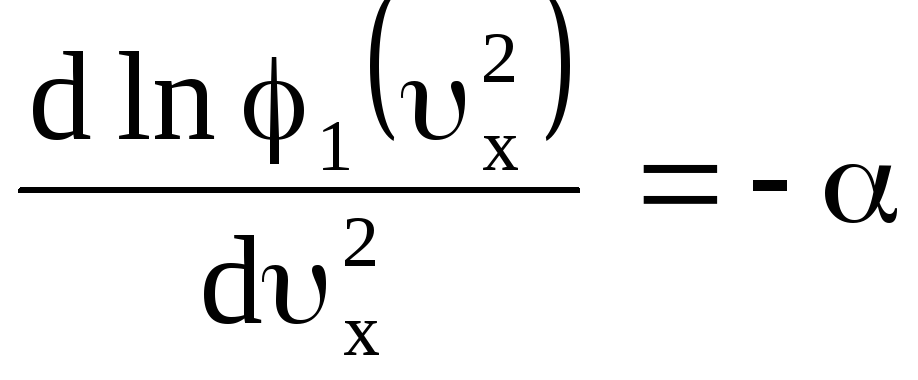 ;
;
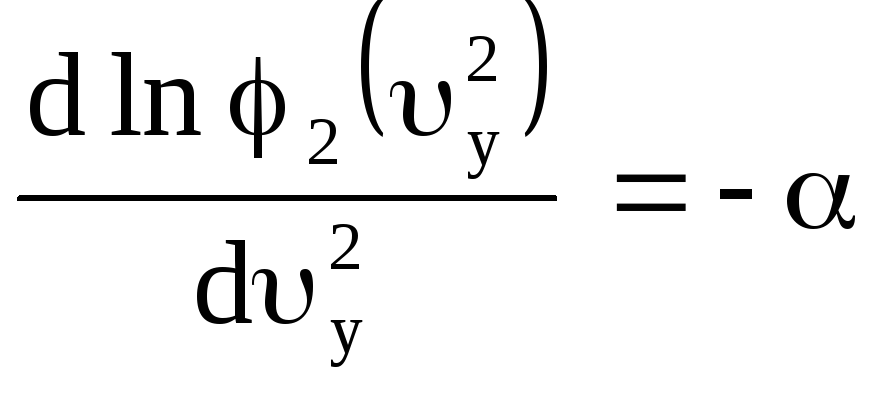
И т.д.
Тогда для плотности функции распределения справедливы равенства
![]() ;
;
![]() ;
;
![]()
![]()
Учтем условие нормировки.
Из него определяем константы.
условие нормировки
![]() ;
;
Причем, интегрирование выполняется по всем возможным значениям скорости.
Физический смысл условия номаровки – левая часть представляет собой вероятность того, что данная молекула будет иметь какое-нибудь(любое) значение составляющей скорости, а это событие является достоверным. Вероятность же достоверного события равна единице.
Для распределения условие нормировки дает
![]() - интеграл Пуассона.
- интеграл Пуассона.
Интеграл в левой части – интеграл Пуассона.
Вычисляется он следующим образом. Рассмотрим интегралы
![]() ;
;
![]() ;
;
Так как значения определенного интеграла не зависит от обозначения переменной интегрирования, то интеграл 1 равен интегралу 2. поэтому:
![]()

Переход
от декартовых координат к полярным дает
возможность упростить вычисления.
Площадь элемента
![]() в полярной системе координат:
в полярной системе координат:![]() ;
;
![]()
Отсюда, учитывая, что элемент площади выражается в полярных координатах
![]()
Учитывая равенство интегралов, перепишем
![]() =
=
![]() =
=
![]() =
=
![]() =
=
![]() =
=![]()
Из условия нормировки следует
![]()
Здесь интегрировали по углу и использовали равенство
I=![]() =
=![]()
Поскольку такие же значения имеют константы С1 и С2 , то постоянная перед интегралом равна
A=![]()
![]()
На основании предыдущих зависимостей получим
![]()
Лекция № 16
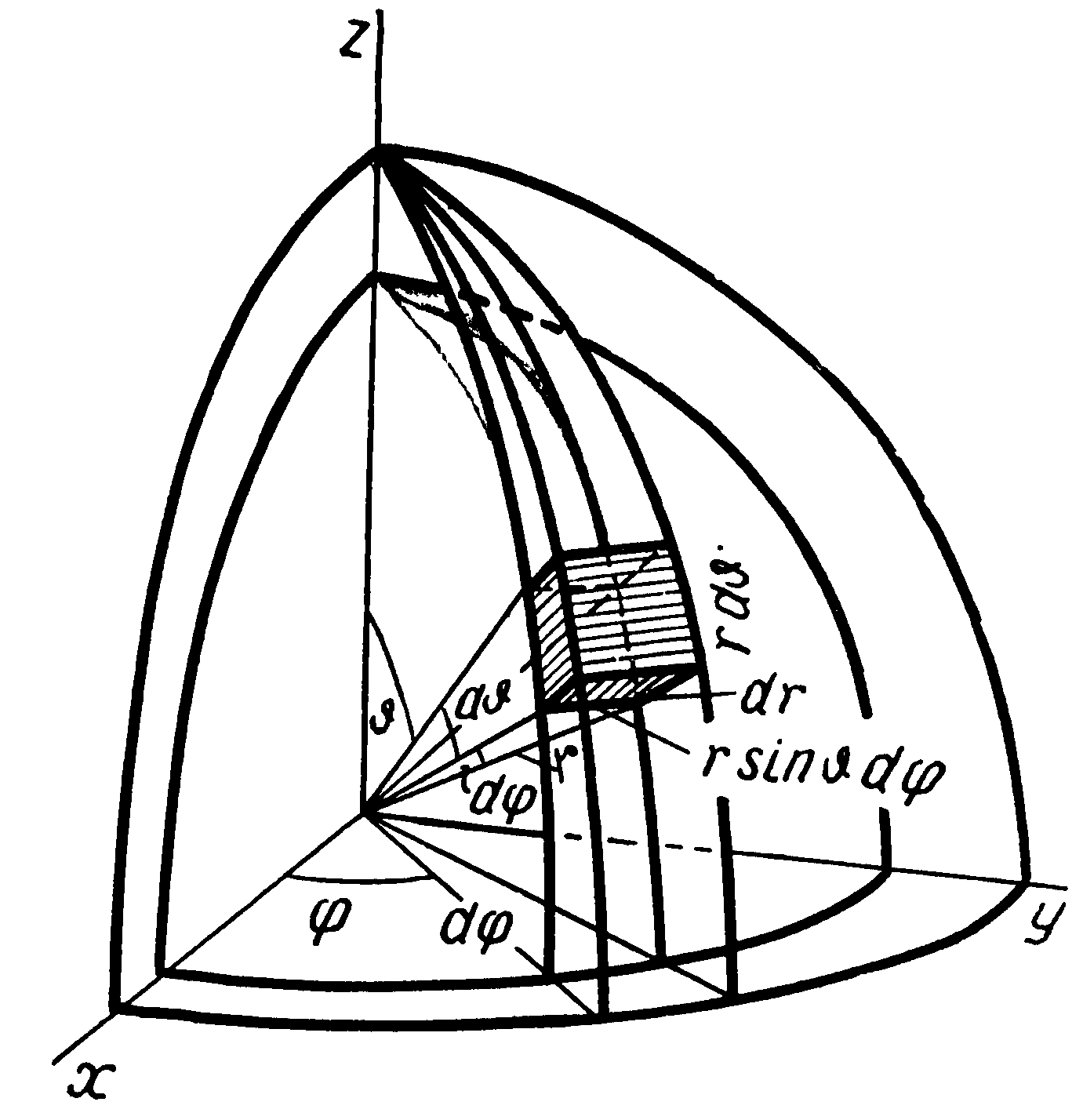
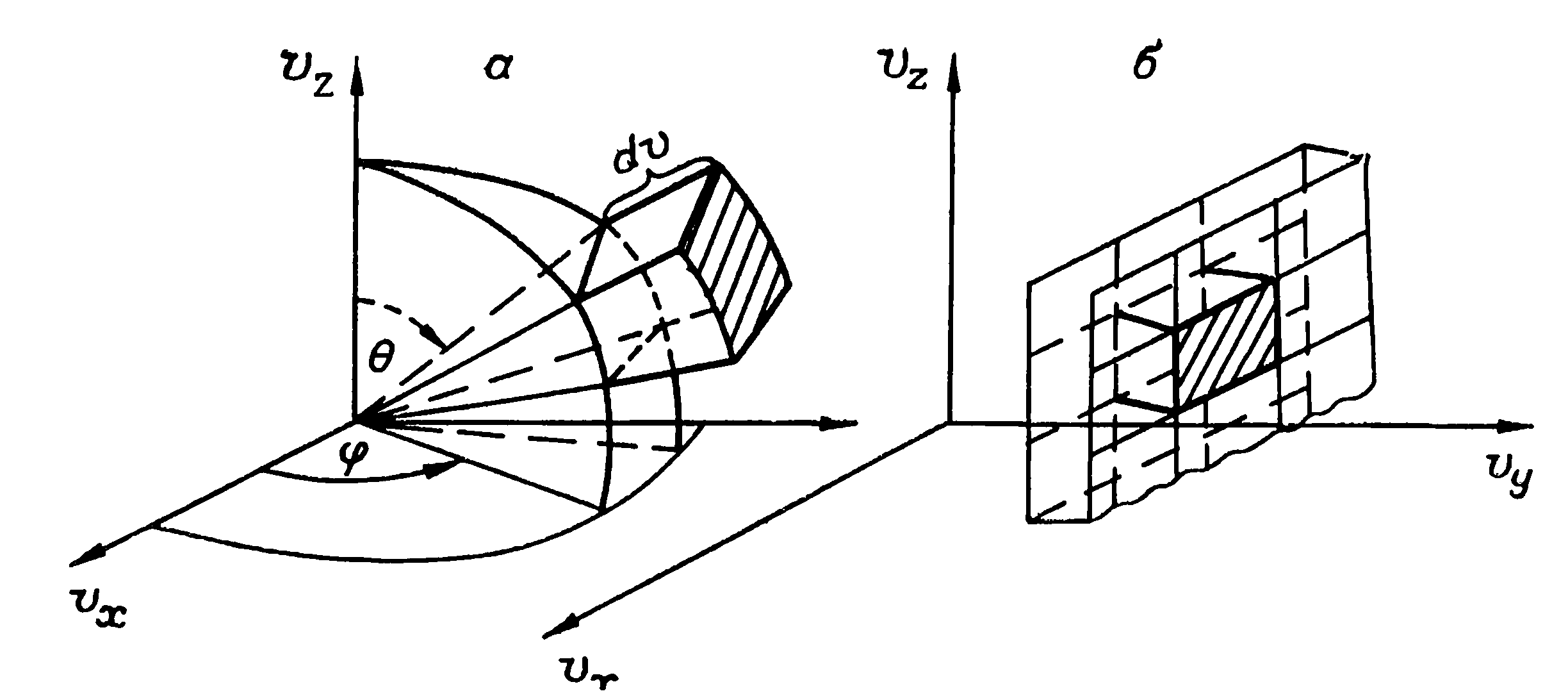
Представляя элементарный объем в сферических координатах(рис ), где одна грань элемента v sinψ dφ , а другая v dψ и высота элемента dv для модуля скорости получим
v sinψ dφ
 v
dψ
v
dψ
В сферических координатах
![]()
Вероятность обнаружения у любой выбранной молекулы какого-либо признака характеризует в то же время относительное число молекул, обладающим этим признаком, следовательно, можно определить относительное число молекул, конец вектора скорости которых лежит в заданном элементе объема, или, иными словами, относительное число молекул, имеющих заданную по величине и направлению скорость.
Если требуется определить вероятность обнаружения у некоторой молекулы скорости, заданной только по величине при любом ее направлении, т.е. по модулю скорости, то последнее выражение необходимо проинтегрировать по всем возможным направлениям углов, т.е.
![]()
Тогда получим
![]()
Или
![]() ;
;
Можно сказать, что величина
![]()
Представляет собой вероятность обнаружения конца вектора скорости в шаровом слое, заключенном между сферами с радиусами, отличающимися на приращение радиуса.
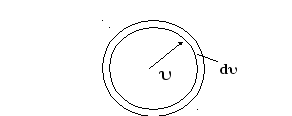
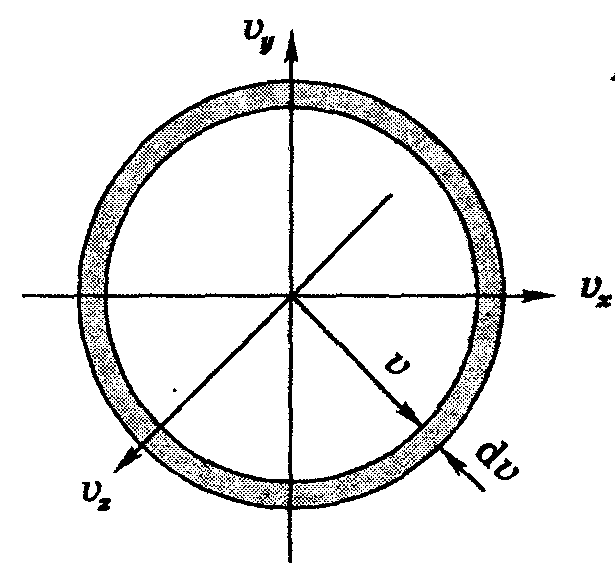
Для сферического слоя можно получить аналогичные результаты. Рассмотрим сферический слой
![]() - сферический слой.
- сферический слой.
Объем сферического слоя равен произведению площади слоя на толщину слоя, равную разности скоростей
![]()
Или
![]()
![]() ;
;
Тогда функция распределения частиц по скоростям будет выглядеть
![]()
Для определения постоянной, фигурирующей во всех соотношениях, как константа, используем ранее полученное соотношение для давления газа на стенку. Для этого запишем
![]()
Вспомним зависимость давления
![]()
Давление выражается через число ударов молекул о стенку в виде
p = 2mvxdν
при этом число ударов
dν =vx dnv
dnv –число молекул в единице объема с заданной по величине и направлению скоростью
число ударов молекул можно получить из выражения
dν
= n![]()
поскольку для давления на стенку требуется задание лишь одной из составляющих по оси х, а значения других составляющих могут быть любыми, то число ударов молекул о стенку получается путем интегрирования по всем значениям составляющих по осям у и z
dν
= n![]()
произведение двух интегралов Пуассона учитываем и получаем
dν
= n![]()
для давления в этом случае получим
p
= 2mn![]()
для вычисления интеграла учтем
![]() - половина интеграла
Пуассона.
- половина интеграла
Пуассона.
![]()
![]() =(1/2)
=(1/2)![]()
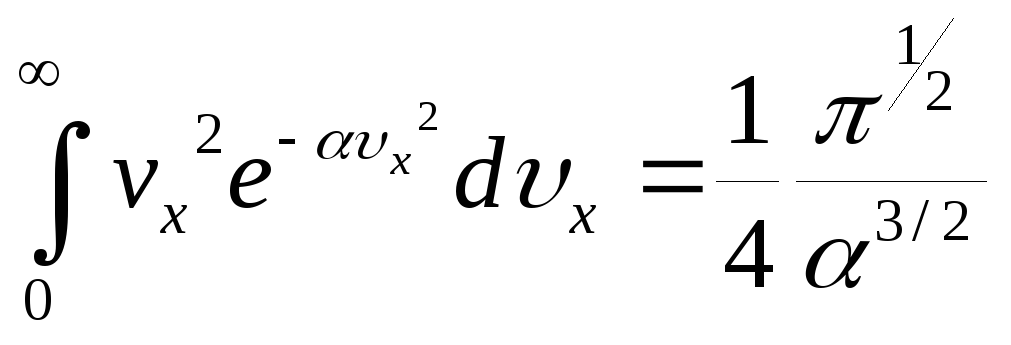
p = mn/(2α)
p= nkT
![]()
![]()
![]() = 4
= 4![]() - распределение Максвелла,
- распределение Максвелла,
где
![]()
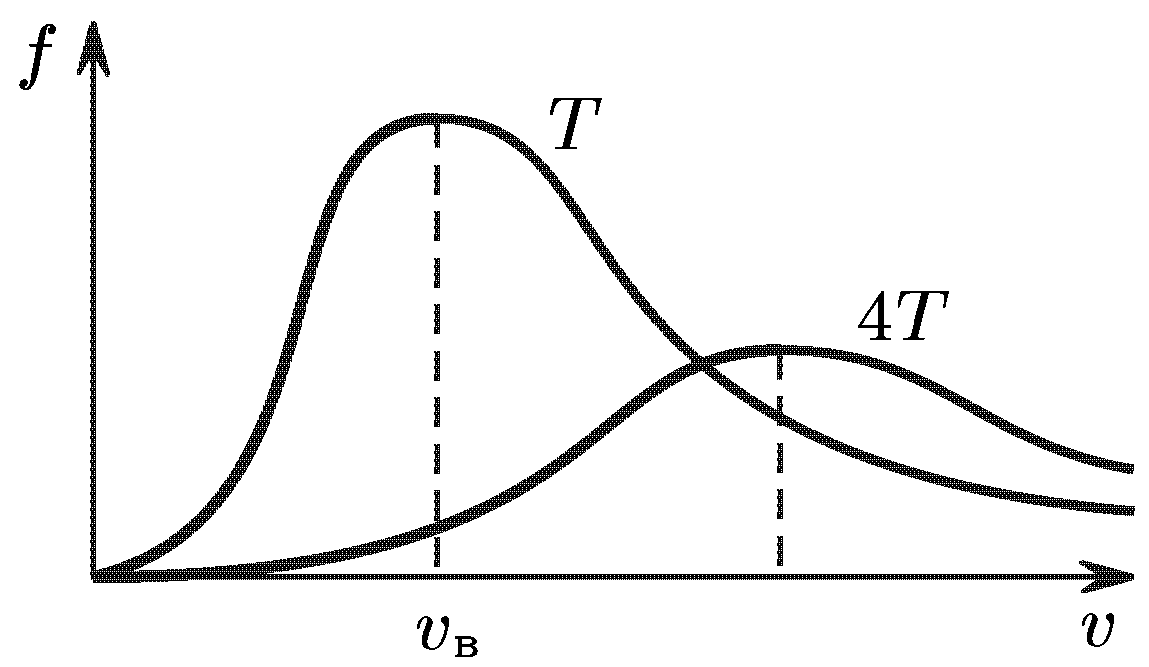

![]() - наивероятнейшая
скорость.
- наивероятнейшая
скорость.
![]() - найдем экстремумы.
- найдем экстремумы.
![]()
![]()
![]()
![]()
![]()
Найдем среднюю скорость:
![]()
![]()
![]()
Интеграл вычисляется путем интегрирования по частям
Однако, следует учесть, что
![]()
Можно дифференцировать этот интеграл по параметру α и умножить результат на -1
Среднеквадратичная скорость представляет собой корень квадратный из среднего значения квадрата скорости
![]()
Чтобы это получить, необходимо дважды продифференцировать по параметру половину интеграла Пуассона
Явление переноса
(неравновесные системы).
Средняя длина свободного пробега молекулы

![]()
![]()
![]()
![]()
![]()
![]() ;
;
Поскольку средние скорости молекул равны нулю(прямые и противоположные направления движения равноправны)
![]()
Произведение скоростей равно нулю.
В этом случае квадрат относительной скорости равен сумме квадратов одинаковых скоростей молекул, а корень квадратный из квадрата относительной скорости равен
![]() ;
;
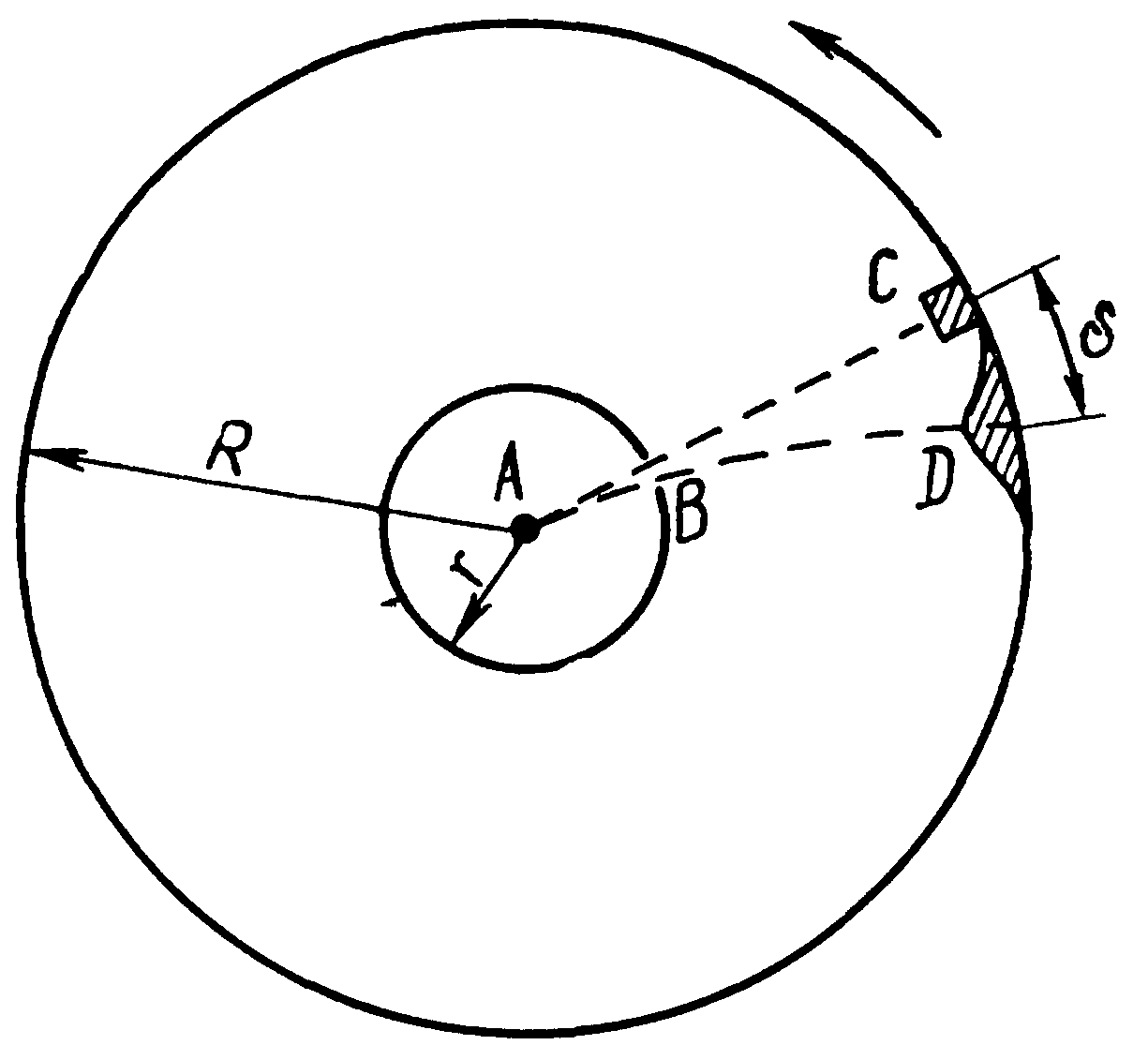
Молекулы совершают хаотические движения, непрерывно сталкиваясь с другими молекулами, находящимися в сечении, площадь которого можно записать в виде:
![]() - сечение, в которое
будут попадать молекулы, столкнувшиеся
с рассматриваемой.
- сечение, в которое
будут попадать молекулы, столкнувшиеся
с рассматриваемой.
Путь, пройденный молекулой между столкновениями можно выразить через время между столкновениями
![]() ;
;
Молекула
столкнется со всеми молекулами, которые
находятся в цилиндре объемом
![]()
![]() ;
;
Количество
молекул в объеме
![]()
![]() ;-
это число столкновений за время ∆t
;-
это число столкновений за время ∆t
Время между столкновениями – это время за которое произошли столкновения на число столкновений за это время
![]() ;
;
Площадь поперечного сечения столкновения
![]() ;
;
Число столкновений в единицу времени
![]() ;
;
Длина свободного пробега молекул
![]() - длина пробега.
- длина пробега.
