
Особенности закиси азота
Закись азота N2 О - бесцветный газ, сладковатого вкуса, сгущающийся при давлении 40 атмосфер и температуре +15° в бесцветную жидкость, которая при нормальном атмосферном давлении кипит при -87,9° (Реньо) и при -115° (Натерер), перевращается в снегообразную массу и прозрачные кристаллы. Из 1 кг жидкой закиси азота образуется 500 л газа при нормальном атмосферном давлении и температуре 0оС.
Удельный вес газа при 10° 1,52638 г./м3, при 100° - 1,52336 (Думрейхер). N 2 O непосредственно из N и O не получается и единственный, способ ее получения – микробиологическое или химическое восстановление высших оксидов азота
В воде растворяется закись азота весьма значительно (при 0° в 100 объемах воды 130 объемов N2O, Кариус). Кислой реакцией раствор не обладает. Закись азота растворяется в спирте, эфире, летучих и жирных маслах. Закись азота, как при непосредственном действии кислорода, так и действием окислителей не переходит в высшие степени окисления азота и вообще отличается значительной инертностью. Поэтому в тропосфере N2O практически не окисляется и ее концентрации в воздухе не зависят от высоты.
Закись азота N2O первые была получена в лабораторных условиях в 1799 г. Гемфри Дэви. Она представляет собой бесцветный газ, тяжелее воздуха (относительная плотность 1,527), с характерным сладковатым запахом. N2O растворима в воде (0,6 объёма N2O в 1 объёме воды при 25 °C). N2O не воспламеняется, но поддерживает горение. Смеси с эфиром, циклопропаном, хлорэтилом в определённых концентрациях взрывоопасны.
N2O является самым сильным парниковым газом. Создаваемый ею термофорсаж (вклад в потепление глобального климата, который мог бы иметь место, если бы это вещество присутствовало в той же концентрации, что и СО2) в 298-310 раз выше, чем у углекислого газа. Это вещество дает сейчас около 1,4 °С в общий парниковый эффект. В спектре поглощения N2O присутствуют линии с длинами волн 4,5 и 8,7 мкм.
N2O относится к несолеобразующим оксидам. В нормальных условиях N2O химически инертен, при нагревании проявляет свойства окислителя:
N2O + H2 → N2 + H2O;
N2O + C → N2 + CO.
При взаимодействии с сильными окислителями N2O может проявлять свойства восстановителя:
5N2О + 8KMnO4 + 7H2SO4 → 5Mn(NO3)2 + 3MnSO4 + 4K2SO4 + 7H2O.
При нагревании N2O разлагается:
2N2O → 2N2 + O2.
Малые концентрации N2O вызывают у человека чувство опьянения (отсюда название — «веселящий газ») и лёгкую сонливость. При вдыхании чистого газа быстро развиваются состояние наркотического опьянения, а затем асфиксия.
В смеси с кислородом N2O при правильном дозировании вызывает наркоз без предварительного возбуждения и побочных явлений. В большинстве случаев анестезиологи применяют комбинированный наркоз, при котором N2O сочетают с другими, более мощными, средствами для наркоза.
N2O при вдыхании не вызывает раздражения дыхательных путей. В легких N2O проникает в кровь и растворяется в ее плазме. С гемоглобином не связывается. После прекращения вдыхания выделяется из организма в атмосферу (в течение 10—15 мин) через дыхательные пути в неизменном виде.
Наркоз с применением закиси азота используется в хирургической практике, оперативной гинекологии, хирургической стоматологии, а также для обезболивания родов. «Лечебный анальгетический наркоз» (Б. В. Петровский, С. Н. Ефуни) с использованием смеси закиси азота и кислорода иногда применяют в послеоперационном периоде для профилактики травматического шока, а также для купирования болевых приступов при острой коронарной недостаточности, инфаркте миокарда, остром панкреатите и других патологических состояниях, сопровождающихся болями, не купирующимися обычными средствами.
Применяют закись азота в смеси с кислородом при помощи специальных аппаратов для газового наркоза. Обычно начинают со смеси, содержащей 70—80 % закиси азота и 30—20 % кислорода, затем количество кислорода увеличивают до 40—50 %. Если не удается получить необходимую глубину наркоза, при концентрации закиси азота 70—75 %, добавляют более мощные наркотические средства: фторотан, диэтиловый эфир, барбитураты.
После прекращения подачи закиси азота в легкие следует во избежание гипоксии продолжать давать кислород в течение 4—5 мин.
Применять закись азота, как и любое средство для наркоза, необходимо с осторожностью, особенно при выраженных явлениях гипоксии и нарушении диффузии газов в лёгких.
Для обезболивания родов пользуются методом прерывистой аутоанальгезии с применением, при помощи специальных наркозных аппаратов, смеси закиси азота (40—75 %) и кислорода. Роженица начинает вдыхать смесь при появлении предвестников схватки и заканчивает вдыхание на высоте схватки или по её окончании.
Лечебный наркоз закисью азота (при стенокардии и инфаркте миокарда) противопоказан при тяжёлых заболеваниях нервной системы, хроническом алкоголизме, состоянии алкогольного опьянения (возможны возбуждение, галлюцинации). В зимние месяцы содержание в воздухе N2O снижается, в летние оно возрастает. В летние месяцы распределение N2O в полушарии практически однородно, в отличие от зимних месяцев.
Распределения в атмосфере Южного и Северного полушарий закиси азота в июне и январе показаны на рисунке 2.а, б
Из данного рисунка следует, что на протяжение всего года концентрации N2O максимальны над экваториальными регионами планеты. В зимние месяцы над приполярными районами формируются области с пониженным содержанием N2O – «закисные дыры». Над Южным полушарием они более выражены, чем над Северным.
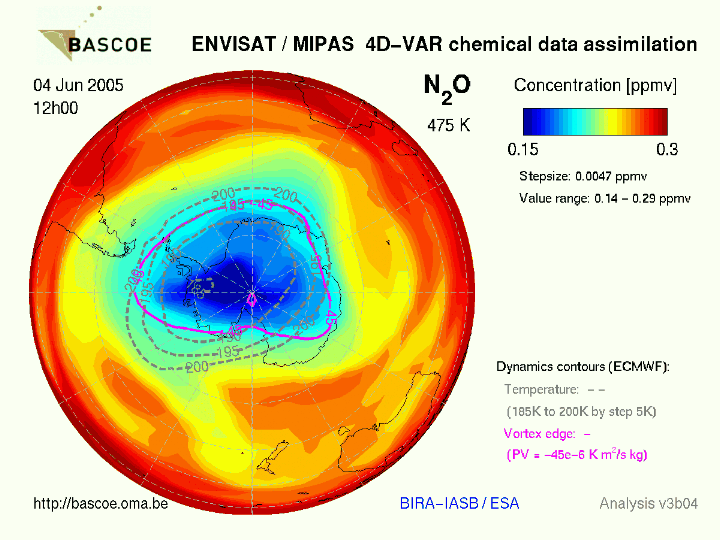
А)зима в Южном полушарии.
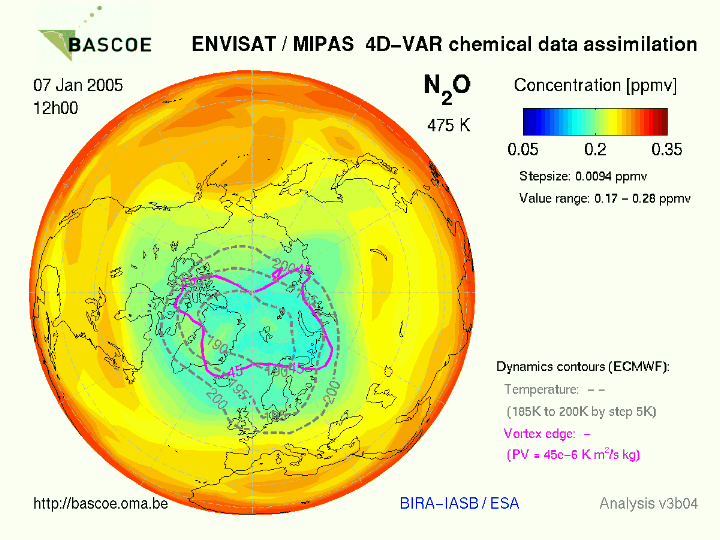
Б) зима в Северном полушарии
Рисунок 2. Распределения в атмосфере Южного и Северного полушарий закиси азота в июне и январе
