
Лекция 3. Кислотообразующие окислы в атмосфере
Учебные вопросы:
-
Экологические особенности кислотообразующих окислов.
-
Физические и химические свойства NO2
-
Биогеохимический круговорот азота.
4. Особенности закиси азота
5. Особенности окиси азота.
6. Оксиды азота в атмосфере как компонент летнего смога.
7. Оксиды азота в атмосфере как компонент Кислотных осадков.
Экологические особенности кислотообразующих окислов.
КОО- NO2, SO2, CO2 относятся к числу компонентов земной атмосферы, важнейших с точки зрения экологии.
КОО - посредники, делающие вещества, образующие неживую природу, доступными компонентам живой природы.
Реагируя с водой, образующей облака и атмосферные осадки, КОО образуют кислоты, растворяющие горные породы и многие вещества, входящие в состав почв. Тем самым они обогащают поверхностные и подземные воды микроэлементами, как необходимыми для развития растений и животных, так и вредными для них.
Существенное влияние они играют в обеспечении обмена веществ в организмах людей и других живых существ. Главную роль в этом играет CO2, способный образовывать угольную кислоту, а также ее соли растворимые в воде, крови и лимфе - гидрокарбонаты.
Все КОО в небольших количествах необходимы для формирования белков, образующих организмы растений и животных, но при увеличении своего содержания, играют роль ингибиторов, тормозящих биохимические процессы.
Кислоты, содержащиеся в атмосферных осадках в избыточных количествах, оказывают на биоту также прямое поражающее воздействие. Ими поражаются эпителии, глаза и другие органы людей, животных, а также листья растений. Поэтому такие КОО, как NO2, SO2 относятся ко 2 классу опасности.
КОО участвуют в образовании и разрушении стратосферного, тропосферного и приземного озона.
КОО уменьшают РН в водоемах, что оказывает существенное влияние на развитие водных экосистем.
КОО обладают свойствами парниковых газов, а CO2 является веществом, которое, по мнению Международной группы экспертов по проблемам изменений климата, является главным виновником современного потепления климата.
Наряду с перечисленными общими особенностями, каждое из веществ, рассматриваемых как КОО, обладает существенными специфическими свойствами.
В данной лекции мы более подробно остановимся на свойствах лишь одного из рассматриваемых веществ - NO2. Свойства SO2 и CO2 будут рассмотрены в последующих лекциях.
Физические и химические свойства no2
Двуокись азота при температурах, встречающихся в земной атмосфере, присутствует в основном в виде азотноватого ангидрида N2O4 . Азотноватый ангидрид при температурах ниже (-16оС) представляет собой бесцветные кристаллы. При более высоких температурах это жидкость, окрашивающаяся в цвета (в зависимости от температуры) от бледно-желтого до бурого.
Именно эта жидкость снималась в фильме «Охотники за привидениями в подземельях Нью Йорка» как среда, порождающая привидения.
Пары азотноватого ангидрида окрашены в бурый цвет, становящийся с повышением температуры все интенсивнее, вследствие того, что все большая часть содержащихся в них молекул азота входит в состав NO2. Сен-Клер, Девилль и Трост показали, что нагревании до + 140° все молекулы азотноватого ангидрида превращаются в NO2 , а пары окрашиваются в черный цвет. Бертело установлено, что реакция разложения N2O4 = 2NO2 сопровождается поглощением тепла (-13,0 кал./г).
Будучи окислом промежуточным, азотноватый ангидрид может быть получен как из высшей степени окисления - азотной кислоты, так и из низшей - окиси азота.
Из азотной кислоты азотноватый ангидрид в лабораторных условиях образуется при восстановлении ее действием олова: 4HNO3 + Sn = H2SnO3 + Н2 О + 2N2O4, крахмала, мышьяковистого ангидрида As2 О 3 и др. веществ, способных легко окисляться, отнимая кислород от азотной кислоты, но при этом N2O4 не получается свободным от других окислов азота (NO, N2O). Лучше исходить из азотнокислого свинца, который при накаливании разлагается: 2Pb(NO 3)2 = 2PbO + 4NO2 + O2.
Из окиси азота NO азотноватый ангидрид получается наиболее чистым и прямо дает при охлаждении бесцветные кристаллы. Для этого 2 объема окиси азота и 1 объем кислорода, хорошо высушенные, проводятся в охлаждаемую трубку, где, смешиваясь, и соединяются 2NO + O2 = 2NO2.
С водой азотноватый ангидрид гидрата не дает, но тотчас же разлагается. Вообще во многих случаях азотноватый ангидрид, как промежуточный окисел, разлагается, образуя производные азотистого и азотного ангидридов.
Как установил Фричше, при действии воды на холоде происходит реакция: 2N2O4 + Н2 О = 2HNO3 +N2O3.
Действие теплой воды в большом количестве дает исключительно НNО3, но это происходит потому, что N 2O3 тотчас разлагается:
2N 2O3 = 2NO + N2O4, и далее 2 NO +О2 = N2О 4.
Техногенными источниками NO2 в атмосфере являются двигатели внутреннего сгорания, топки, котельные, взрывы, а также сельское хозяйство, где применяются азотные удобрения.
Природными источниками NO2 в атмосфере являются грозы, где это вещество образуется в каналах молний, а также в биогеохимическом цикле преобразований соединений азота, протекающем с участием микроорганизмов в почвах, а также различных водных объектах. Распределение в земной атмосфере по высоте различных оксидов азота и их газообразных соединений приведено на рисунке 1.
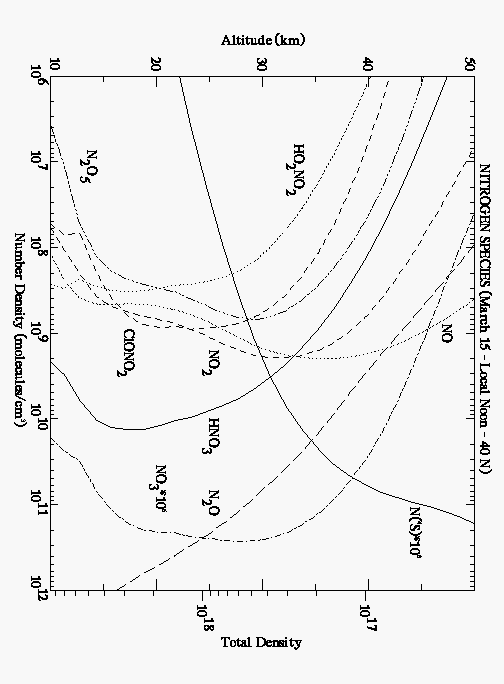
Рисунок 1. Зависимости от высоты количества молекул того или иного вещества в 1 см3 воздуха.
Из рисунка 1 видно, что NO2, NO, НNO3 N2O5 в атмосфере образуют слои, расположенные преимущественно в стратосфере. У земной поверхности концентрации этих веществ весьма не велики и ощутимы лищь вблизиисточников их техногенных выбросов. В тоже время концентрации N2O у земной поверхности максимальны и с увеличением высоты монотонно убывают. Причем в стратосфере их убывание происходит быстрее, чем уменьшается концентрация молекул воздуха.
Происходит это потому, что в стратосфере происходит фотолиз О2 и Н2О, приводящий к образованию О и ОН.
В результате здесь могут протекать реакции:
N2O+О= 2NO
NO+О= NO2.
NO2+ОН= НNO3
