
- •1.Функції печінки
- •2. Панкреатичне і кишкове травлення. Роль жовчі в механізмі травлення
- •3.Синтез гема
- •4. Вторинні месенджери та їх роль в механізмах гормонального впливу на клітини-мішені
- •5. Нормальні і патологічні складові сечі
- •6.Катаболізм пуринових нуклеотидів
- •1.Види жовтяниць. Причини виникнення
- •2. Блокування біосинтезу білка дифтерійним токсином (адф-рибозилювання факторів трансляції)
- •3. Джерело енергії для м’язового скорочення. Атф, креатинфорфат. Особливості обміну в серцевому м’язі.
- •4. Всмоктування вуглеводів. Порушення травлення і всмоктування. Недостатність лактази
- •5. Орнітиновий цикл сечоутворення. Послідовність реакцій
- •6. Порушення обміну медіаторів і модуляторів головного мозку при психічних розладах. Нейрохімічні механізми дії психотропних препаратів
- •Розпад гема
- •Паренхіматозна жовтяниця. Причини. Біохімічні показники
- •Молекулярні механізми дії тиреоїдних гормонів.
- •Молекулярні механізми м’язового скорочення та розслаблення м’язів
- •Нейромедіатори. Рецептори для нейромедіаторів та фізіологічно активних сполук
- •Білковосинтезуюча система. Особливості генетичного коду
- •Орнітиновий цикл сечоутворення.
- •Обтураційна жовтяниця
- •Білки плазми крові. Альбуміни. Глобуліни. Фібриноген.
- •Біологічний ефект альдостерону.
- •Особливості метаболізму нервової тканини
- •Значення обміну мінеральних солей.
- •Механізм активації й функціонування каскадної системи згортання крові.
- •Види жовтяниць
- •Молекулярні механізми м’язового скорочення та розслаблення м’язів
- •Енергетичний обмін в головному мозку людини. Значення аеробного окислення глюкози.
- •Мікросомальне окислення і реакції кон’югації в печінці. Компоненти окислення. Роль цитохрома р-450
- •Розпад гема. Жовчні пігменти.
- •Молекулярні механізми м’язового скорочення та розслаблення м’язів
- •Всмоктування вуглеводів. Порушення травлення і всмоктування.
- •Класифікація гормонів: за місцем синтезу, хімічною природою, механізмом дії.
- •Біосинтез піримідинових нуклеотидів
- •Жіночі статеві гормони. Механізм дії
- •Загальна схема біосинтезу днк. Ферменти реплікації днк у прокаріотів та еукаріотів.
- •Розпад гема.
- •Біохімія нейромедіаторів та фізіологічно активних сполук.
- •Роль печінки в обміні білків, жирів та вуглеводів
- •Потреба в ліпідах, роль лейкотрієпів, простагландинів, тромбоксанів. Ліпіди і захворювання.
- •Етапи та механізми трансляції. Ініціація. Елонгація. Термі нація.
- •Гормони гіпофіза
- •2.Технологія трансплантації генів.
- •Дія стероїдних та тиреоїдних гормонів.
- •Дія гормонів білково-пептидної природи та катехоламінів
- •Транспортні рнк. Активація ак, Аміноацил-тРнк-синтетази. Кодони рнк
- •Гормони на обмін кальцію та фосфатів
- •Єдиний нейрогуморальний механізм регуляції
- •Цтк і механізми, що контролюють його у мозку
- •Катаболізм піримідинових нуклеотидів
- •Порушення гомеостазу кальцію
- •Хімічний склад поперечно-смугастих мязів.
- •3. Експресія генів на рівні транскрипції.
- •Гормони підшлункової. Цукровий діабет.
- •Травлення в шлунку.
- •Антибіотики
- •Сполучна тканина
-
Єдиний нейрогуморальний механізм регуляції
???
Білет 13
-
Цтк і механізми, що контролюють його у мозку
???
-
Катаболізм піримідинових нуклеотидів
Р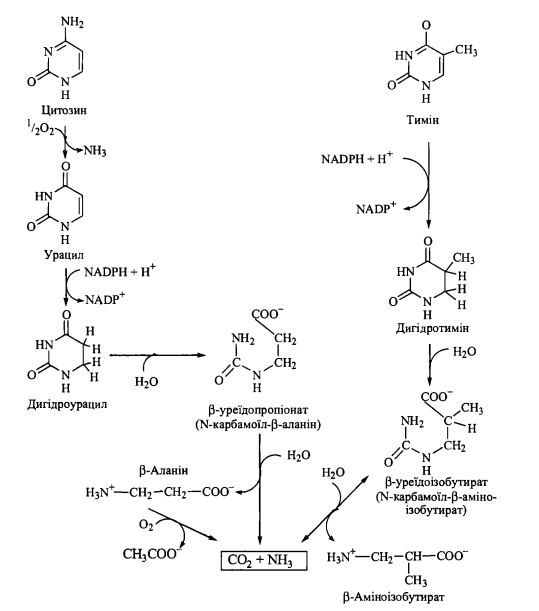 озщеплення
піримідинових нуклеотидів Початкові
етапи катаболізму піримідинових
нуклеотидів, як і в разі пуринових
нуклеотидів, полягають у відщепленні
рибозофосфату з подальшим окисленням
утворених піримідинів. Катаболізм
азотистих основ (урацилу, цитозину,
тиміну) полягає в розриві піримідинових
циклів з утворенням у якості продуктів
похідних амінокислот - ^-аланіну та
$-аміноізобутирату. В свою чергу, ^-аланін
розщеплюється до двоокису вуглецю та
аміаку, тоді як $-аміноізобутират може
метаболізуватися подібно до інших
озщеплення
піримідинових нуклеотидів Початкові
етапи катаболізму піримідинових
нуклеотидів, як і в разі пуринових
нуклеотидів, полягають у відщепленні
рибозофосфату з подальшим окисленням
утворених піримідинів. Катаболізм
азотистих основ (урацилу, цитозину,
тиміну) полягає в розриві піримідинових
циклів з утворенням у якості продуктів
похідних амінокислот - ^-аланіну та
$-аміноізобутирату. В свою чергу, ^-аланін
розщеплюється до двоокису вуглецю та
аміаку, тоді як $-аміноізобутират може
метаболізуватися подібно до інших
розгалужених амінокислот з утворенням сукциніл-КоА.
Білет 14
-
Порушення гомеостазу кальцію
Найбільш поширеними клінічно окресленими порушеннями гомеостазу кальцію є патологічні синдроми, пов'язані з дефіцитом вітаміну D3 (які проявляються як рахіт у дітей і різні форми остеопорозу в дорослому та похилому віці) та захворювання, спричинені первинною патологією паращитовидних залоз—гіпер- та гіпопаратиреоз.
Рахіт - захворювання дитячого віку, яке спричиняється зменшеним надходженням та (або) синтезом в організмі вітамінів групи D — тваринного D3 (холекальциферолу) та рослинного D2 (ергокальциферолу). Вірогідність захворювання значно зростає в умовах недостатнього опромінення шкіри дитини сонячним світлом, що є необхідним для утворення вітаміну D3 з 7-дегідрохолестерину. Основними проявами рахіту є гіпо- кальціємія та гіпофосфатемія, які призводять до глибоких порушень кальцифікації кісткової тканини та специфічних змін скелета.
Гіперпаратиреоз - група захворювань, розвиток яких пов'язаний із надлишковою секрецією паратгормону, аномальним збільшенням внаслідок цього концентрації кальцію в сироватці крові і гіпофосфатемією. Первинний гіперпаратиреоз - патологія, що спричиняється наявністю в паращитовидних залозах гормонально активних пухлин - аденоми, карциноми - або гіперплазією залози. Провідними симптомами захворювань цієї групи є ураження кісткової системи (проявляється демінералізацією кісток остеопорозом) та нирок із розвитком сечокам'яної хвороби (внаслідок відкладання солей та утворення каменів, що складаються з оксалату та фосфату кальцію) і нефрокальцинозу.
-
Хімічний склад поперечно-смугастих мязів.
Біохімічний склад м'язів Скелетні м'язи ссавців містять у своєму складі: 72-80 % води; 16-20 % білків; 0,9-2,2 % небілкових азо-і А ! тистих сполук (креатин, креатинфосфат, АТФ,
АДФ, амінокислоти тощо); безазотисті органічні сполуки (глікоген - 0,3- 3,0 %; фосфоліпіди - 0,4— 1,0%; холестерин - 0,06- 0,2 %); мінеральні елементи (К+, Са2+, Na+ тощо).
Білки м'язів Білки скелетних м'язів складаються з водонероз- чинних білків міофібрил (які становлять 75-80 % загального вмісту білків м'язів) і водорозчинних білків саркоплазми - так званого "міогену" До складу фракції міогену входять переважно ферменти, що каталізують ката-
болічні реакції, які забезпечують біоенергетику м'язового скорочення - глікогенфос-
форилаза, ферменти гліколізу, креатинфосфокіназа, аденілаткіназа, кисеньдепо-
нуючий білок міоглобін. У саркосомах містяться ферменти циклу трикарбонових
кислот, біологічного окислення й окисного фосфоритування.
Білки міофібрил До складу міофібрил входять такі білки: 1) до складу товстих ниток - білок міозин; 2) до складу тонких ниток - білки актин, тропоміозин, тропоніновий комплекс {тропонін Т, тропонін І, тропонін Q; 3) білок a-актинін - компонент Z-лінії саркомерів; з цим білком сполучені кінці F-актинових молекул тонких філаментів. Міозин - фібрилярний білок, що утворює товсті філаменти міофібрил. Молекула міозину асиметрична, складається з двох важких поліпептидних ланцюгів, що мають конформацію ос-спіралі й закручені один відносно одного; довжина молекули - 160 нм. N-кінці важких ланцюгів утворюють глобулярні "головки", які нековалентни- ми зв'язками сполучені з додатковими чотирма легкими поліпептидними ланцюгами. В умовах триптичного гідролізу міозин розщеплюється на два фрагменти - меро- міозини: легкий мероміозин — LMM {light meromyosin - англ.) та важкий мероміозин - НММ {heavy meromyosin — англ.). Подальший гідроліз НММ папаїном спричиняє утворення двох ідентичних глобулярних субфрагментів S1 (головок міо зину) і паличкоподібного субфрагмента S2
(рис. 33.3). До складу головок S1 входять каталітичні центри з АТФ-азною активністю і
центри для зв'язування з актином (при відсутності АТФ). Фібрилярні "хвости" молекул міозину
контактують між собою в поздовжньому напрямку, утворюючи товсті філаменти саркомерів, до складу кожного з яких входять близько 400 молекул міозину. Глобулярні головки виступають із зовнішньої поверхні філамента (рис. 33.4). Актин - білок, що існує у двох формах: G- та F-актин. G-актин - глобулярний білок, що має вигляд кулястих молекул діаметром близько 5 нм. Молекули G-актину (субоди- ниці) нековалентно сполучаються між собою, утворюючи намистоподібні утворення -ланцюги фібрилярного F-актину. У м'язових клітинах F-актин представлений фібрилярними структурами, що складаються з двох ланцюгів, переплетених один навколо одного (рис. 33.5). F-актин складає основу будови тонких ниток саркомерів. У складі тонких ниток ланцюги F-актину сполучені з тропоміози- ном і тропонінами. Тропоміозин - білкові молекули витягнутої форми, що складаються з двох поліпептидних ланцюгів (а та 0), які утворю ють подвійну спіраль. Паличкоподібні молекули тропоміозину (довжиною 40 нм і товщиною 2 нм) розміщуються в борозенках між двома ланцюгами F-актину таким
чином, що кожна молекула тропоміозину контактує із сімома молекулами (субоди-
ницями) G-актину. Тропонін - білок тонких філаментів, що складається з трьох субодиниць: ТпТ, ТпІ, ТпС. Тропонінові комплекси мають глобулярну форму і розміщуються впродовж ак-
тинового філамента з інтервалами в 38,5 нм, контактуючи з кінцями молекул
тропоміозину (рис. 33.6). Найбільш вивченим компонентом тропонінового комплексу є ТпС - кальційзв 'язуючий білок, близький за структурою і властивостями до кальмодуліну - універсального трансдуктора кальцієвих сигналів у біохімічних системах. Білок ТпІ взаємодіє з актином, ТпТ - забезпечує взаємодію тропонінового комплексу з тропоміозином.
