
- •Министерство образования и науки Российской Федерации
- •Научный редактор
- •Введение
- •1. Основные термические параметры состояния
- •Удельный объем
- •Давление
- •Соотношения единиц измерения давления
- •Температура
- •1.1. Задачи
- •1.2. Контрольные вопросы
- •2. Законы и уравнения состояния идеальных газов. Смеси идеальных газов
- •2.1. Задачи
- •2.2. Контрольные вопросы
- •3. Теплоемкости газов и газовых смесей
- •3.1. Задачи
- •3.2. Контрольные вопросы
- •4. Первый закон термодинамики для закрытой системы
- •4.1. Задачи
- •4.2. Контрольные вопросы
- •5. Политропные процессы изменения состояния идеальных газов
- •5.1. Задачи
- •5.2. Особенности расчета процессов идеальных газов при учете влияния температуры на их изобарную и изохорную теплоемкости
- •5.3. Задачи
- •5.4. Контрольные вопросы
- •6. Термодинамические свойства воды и водяного пара. Процессы водяного пара
- •6.1. Задачи
- •6.2. Контрольные вопросы
- •7. Влажный воздух
- •Основные характеристики влажного воздуха
- •Характеристики атмосферного влажного воздуха
- •Область влажного ненасыщенного воздуха h,d- диаграммы
- •Область перенасыщенного влажного воздуха h,d- диаграммы
- •Пример пользования h,d- диаграммой
- •7.1. Задачи
- •7.2. Контрольные вопросы
- •8. Второй закон термодинамики
- •8.1. Задачи
- •8.2. Контрольные вопросы
- •9. Первый закон термодинамики для потока. Работа изменения давления в потоке. Эксергия в потоке
- •Работа изменения давления в потоке для адиабатных процессов
- •Эксергия в потоке
- •9.1. Задачи
- •9.2. Контрольные вопросы
- •10. Истечение газа и пара через сопловые каналы
- •Особенности расчета процесса истечения через сопло реальных веществ
- •Необратимое истечение газов и паров через сопло
- •Процессы торможения. Параметры заторможенного потока
- •Методика расчета соплового канала при истечении через него газа или пара с начальной скоростью больше нуля
- •10.1. Задачи
- •10.2. Контрольные вопросы
- •11. Дросселирование газов, паров и жидкостей
- •11.1. Задачи
- •11.2. Контрольные вопросы
- •12. Процессы смешения газов и паров
- •Смешение в объёме
- •Смешение в потоке
- •Смешение при заполнении объёма
- •12.1. Задачи
- •12.2. Контрольные вопросы
- •13. Циклы двигателей внутреннего сгорания
- •Цикл двс с подводом теплоты к рабочему телу при постоянном объеме
- •Цикл двс с подводом теплоты к рабочему телу при постоянном давлении
- •Цикл двс со смешанным подводом теплоты к рабочему телу
- •13.1. Задачи
- •13.2. Контрольные вопросы
- •14. Циклы воздушных реактивных двигателей
- •Цикл прямоточного врд
- •Цикл турбокомпрессорного врд
- •14.1. Задачи
- •14.2. Контрольные вопросы
- •15. Циклы газотурбинных установок
- •Методика расчета тепловой экономичности обратимого цикла гту
- •Тепловая экономичность реального цикла гту
- •Регенеративный цикл гту
- •Регенеративный цикл гту с двухступенчатым сжатием и расширением рабочего тела
- •15.1. Задачи
- •15.2. Контрольные вопросы
- •16. Циклы паротурбинных установок
- •16.1. Базовый цикл пту – цикл Ренкина
- •Расчет простого обратимого цикла пту
- •Расчет необратимого цикла простой пту
- •Система кпд цикла пту
- •16.2. Цикл пту с вторичным перегревом пара
- •16.3. Регенеративный цикл пту
- •Выбор оптимальных давлений отборов пара турбины на регенеративные подогреватели пту
- •Особенности расчета регенеративных пту с подогревателями поверхностного типа
- •16.4. Теплофикационные циклы пту
- •Теплофикационные пту с отборами пара на тепловые потребители
- •16.5. Термодинамические особенности расчета циклов аэс на насыщенном водяном паре
- •16.6. Задачи
- •16.7. Контрольные вопросы
- •17. Циклы парогазовых установок
- •17.1. Цикл пгу с котлом-утилизатором
- •17.2. Циклы пгу со сжиганием топлива в паровом котле
- •Цикл пгу с низконапорным парогенератором
- •Цикл пгу с высоконапорным парогенератором
- •Полузависимая пгу
- •17.3. Задачи
- •17.4. Контрольные вопросы
- •18. Циклы холодильных установок и тепловых насосов
- •18.1. Цикл воздушной холодильной установки (вху)
- •Методика расчета вху
- •18.2. Цикл парокомпрессорной холодильной установки
- •Методика расчета цикла пкху
- •18.3. Парокомпрессорный цикл теплового насоса
- •Методика расчета цикла парокомпрессорного теплового насоса
- •18.4. Задачи
- •18.5. Контрольные вопросы
- •Заключение
- •Библиографический список
- •Приложения
- •Оглавление
- •Чухин Иван Михайлович
- •Редактор н.Б. Михалева
- •153003, Г. Иваново, ул. Рабфаковская, 34.
3.1. Задачи
Теплоемкости идеальных газов
Пример решения задачи:
3.1. Определить удельные массовые, мольные, объемные (на нормальный м3) изохорные и изобарные теплоемкости кислорода О2 (=32 кг/кмоль), считая его идеальным газом с “жесткими” молекулами.
Решение
Удельные мольные изохорная и изобарная теплоемкости идеального кислорода
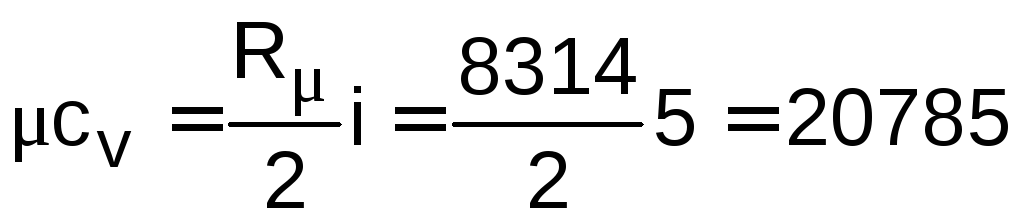
![]() ;
;
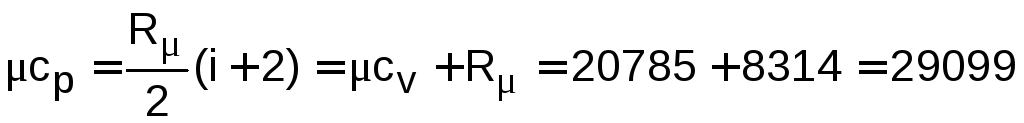
![]() .
.
Удельные массовые изохорную и изобарную теплоемкости кислорода можно определить через соответствующие мольные теплоемкости:
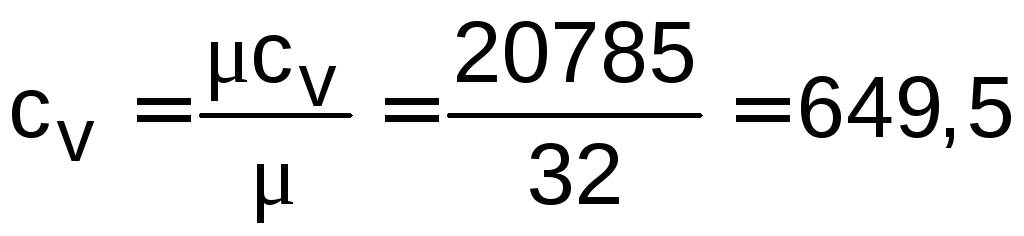
![]() ;
;
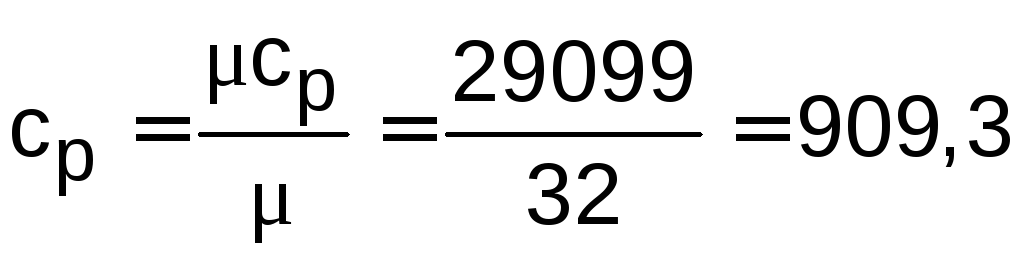 ,
,
![]() .
.
Удельные объемные (на нормальный н.м3) изохорную и изобарную теплоемкости кислорода можно также определить через соответствующие мольные теплоемкости:
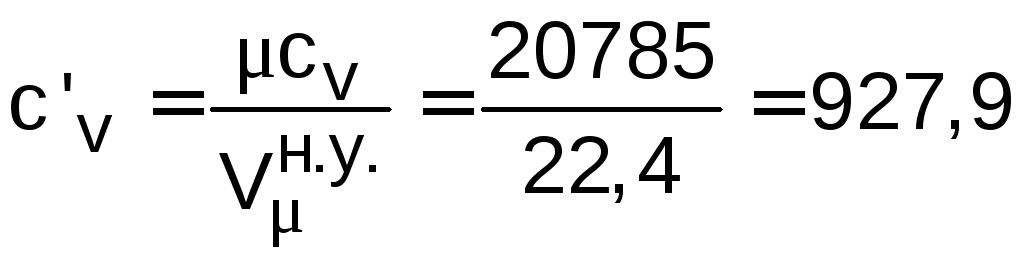
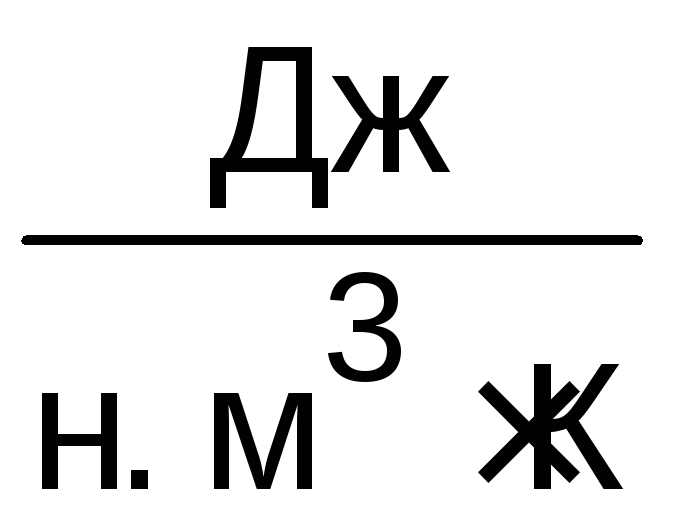 ;
;
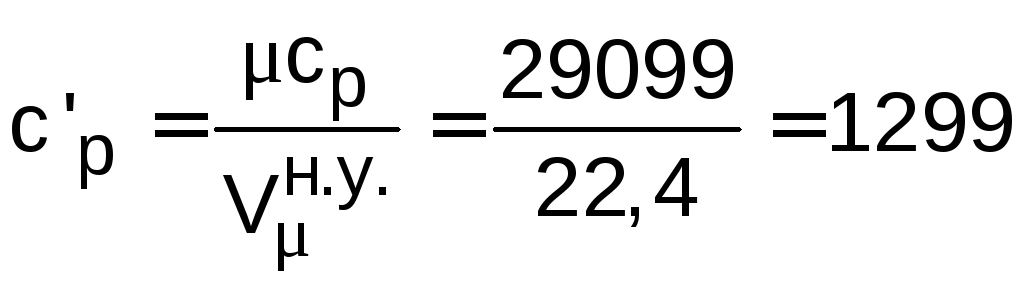
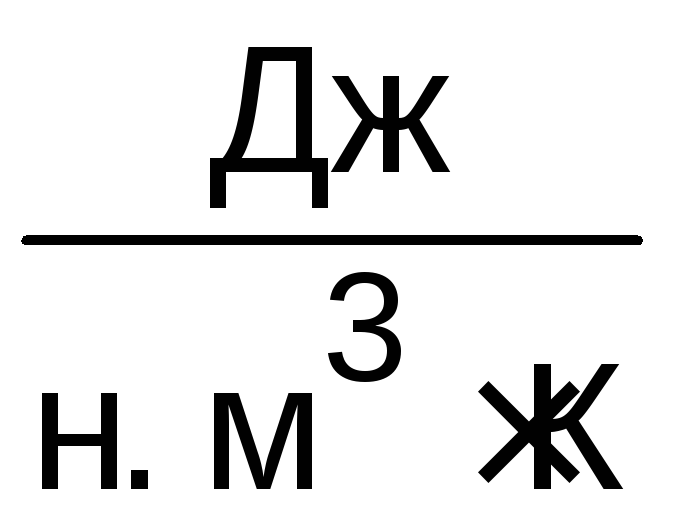 .
.
3.2. Воздух, занимающий объем V1=15 м3 при температуре t1=1500 оС и давлении р1=760 мм рт.ст., изохорно охлаждается до t2=250 оС. Определить отведенную от воздуха теплоту Q, считая его теплоемкость постоянной, как у идеального двухатомного газа с молярной массой µ=28,96 кг/кмоль.
Ответ: Q=-2,68 МДж.
Теплоемкости реальных газов
3.3. Истинная мольная изобарная теплоемкость газа с µ=38 кг/кмоль определяется зависимостью
![]() ,
кДж/(кмоль∙К).
,
кДж/(кмоль∙К).
В изохорном процессе 6 кг этого газа нагреваются от 80 до 700 оС. Определить теплоту этого процесса.
Ответ: Q=2236 кДж.
3.4.
Средняя массовая изобарная теплоемкость
газа с
µ=30
кг/кмоль на
интервале температур от 0 оС
до 50 оС
имеет значение
![]() кДж/(кг∙К), а на интервале от 0оС
до 100 оС
имеет значение
кДж/(кг∙К), а на интервале от 0оС
до 100 оС
имеет значение
![]() кДж/(кг∙К). Определить среднюю массовую
и мольную изобарную теплоемкости газа
на интервале температур от 50оС
до 100 оС.
кДж/(кг∙К). Определить среднюю массовую
и мольную изобарную теплоемкости газа
на интервале температур от 50оС
до 100 оС.
Ответ: сpm=0,92 кДж/(кг∙К), µсpm=27,6 кДж/(кмоль∙К).
3.5. Воздух (µ=28,96 кг/кмоль) с температурой 150 оС образуется в результате изобарного смешения двух потоков воздуха: холодного с t1 = 15 оС и горячего с t2 =900 оС. Определить, сколько холодного и горячего воздуха образует 1 кг смеси. Все давления считать одинаковыми. Средняя мольная изобарная теплоемкость воздуха, взятая от 0 оС, определяется по формуле
![]() ,
кДж/(кмоль∙К).
,
кДж/(кмоль∙К).
Ответ: m1=0,855 кг, m2=0,145 кг.
3.6. Воздух (µ=28,96 кг/кмоль), имеющий температуру tt=1500 оС, давление р=760 мм рт.ст. и занимающий объем V1=5 м3 , изобарно охлаждается до t2=250 оС. Определить количество отводимой от воздуха теплоты, если:
1) считать теплоемкость постоянной, как для идеального двухатомного газа;
2)
считать истинную теплоемкость воздуха,
подчиняющуюся зависимости
![]() кДж/(кмоль∙К).
кДж/(кмоль∙К).
Определить относительную разницу результатов по первому и второму методам расчета.
Ответ: Q1=-1250 кДж, Q2=-1340 кДж, Q=9,1 %.
3.7. 4 м3 углекислого газа (СО2) находятся при р1=7 бар и t1=400 оС. Определить количество теплоты, которое нужно при постоянном давлении подвести к газу, чтобы нагреть его до 1000 оС. Значения теплоемкостей газа брать из таблиц средних теплоемкостей (табл. П2.2).
Ответ: Q=16 МДж.
3.8. Истинная мольная изобарная теплоемкость газа, кДж/(кмоль∙К), с молярной массой µ= 28 кг/кмоль определяется по формуле
![]() .
.
Определить изменение внутренней энергии 1 кг газа при изменении его температуры от 200 оС до 1000 оС.
Ответ: u=781 кДж/кг.
3.9. Истинная мольная изобарная теплоемкость газа, кДж/(кмоль∙К), с молярной массой µ= 30 кг/кмоль определяется выражением
![]() .
.
Определить среднюю массовую изобарную теплоемкость этого газа срm на интервале температур от 300 оС до 1200 оС.
Ответ: срm=1,242 кДж/(кг∙К).
3.10. Средняя мольная изобарная теплоемкость газа, кДж/(кмоль∙К), принятая от 0 оС, определяется по формуле
![]() .
.
Определить теплоту изохорного процесса при нагреве 1 кг газа от 200 оС до 800 оС, если его молярная масса µ=32 кг/кмоль.
Ответ: qv = 564 кДж/кг.
Теплоемкости смеси газов
3.11. Определить массовые изохорную и изобарную теплоемкости смеси идеальных газов, если задан объемный состав смеси: 10 % водорода (Н2), 10 % окиси углерода (СО), 40 % углекислого газа (СО2), 40 % азота (N2).
Ответ: сv=0,706 кДж/(кг∙К); ср=0,967 кДж/(кг∙К).
3.12. Пользуясь таблицами средних теплоемкостей, определить среднюю объемную теплоемкость (на нормальный м3) при постоянном давлении для смеси газов, при изменении температуры от 200 до 1200 оС. Объемный состав смеси: 14,5 % углекислого газа; 6,5 % кислорода, 79 % азота.
Ответ: ср’=1,58 кДж/(н.м3∙К).
3.13. Смесь водорода и метана, содержащая по объему 40 % водорода, нагревается при постоянном давлении от 20 до 350 оС. Определить расход теплоты на 1 кг смеси, если считать:
1) теплоемкость постоянной, как для идеальных газов с жесткими молекулами;
2) теплоемкость переменной (использовать табл. П2.2 средних теплоемкостей).
Оценить относительную погрешность результатов расчета первого метода по отношению ко второму.
Ответ:
q1=1003
кДж/кг, q2=1208
кДж/кг,
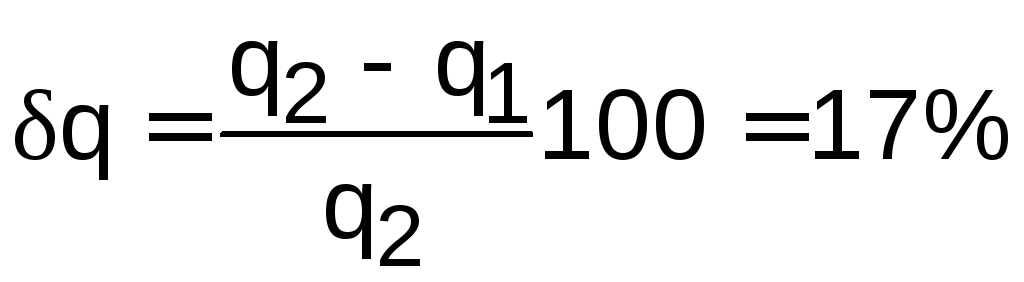 .
.
3.14. Объемный состав газовой смеси задан: 80 % N2, 16 % O2, 4 % CO2. Определить удельные изобарные теплоемкости смеси этих газов: мольную, массовую, объемную (в расчете на нормальный кубический метр). Расчеты выполнить двумя способами:
а) считая газы идеальными с постоянными теплоемкостями, не зависящими от температуры,
б) определить средние теплоемкости смеси в интервале температур 400 оС – 1000 оС, используя таблицы средних теплоемкостей (табл. П2.2), и оценить относительную погрешность по сравнению с предыдущими расчетами.
Ответ:
а) µср см =29,265 кДж/(кмоль∙К), ср см =0,9995 кДж/(кг∙К),
с’р см =1,306 кДж/(н.м3∙К);
б) µср см =33,691 кДж/(кмоль∙К), ср см =1,151 кДж/(кг∙К),
с’р см = 1,504 кДж/(н.м3∙К);
ср см =13,13 %.
