
Журнал неврологии и психиатрии / 2008 / NEV_2008_12_16
.pdf
КРАТКИЕ СООБЩЕНИЯ
Применение мексидола в послеоперационной реабилитации больных с дегенеративно-дистрофическими заболеваниями позвоночника
В.П. ШАТРОВА, К.Т. МЕСХИ
Mexidol in the post-surgery rehabilitation of patients with degenerative-dystrophic diseases of the spine
V.P. SHATROVA, K.T. MESKHI
Отделение хирургии позвоночника Научного центра хирургии им. акад. Б.В. Петровского РАМН, Москва
В России среди неврологических заболеваний взрослого населения более половины составляют поражения периферической нервной системы [2]. В общей структуре инвалидности вследствие заболеваний костно-суставной системы, дегенеративно-дистрофические заболевания позвоночника составляют 20,4% [16]. Среди причин временной нетрудоспособности дегенеративно-дистрофические изменения пояснично-крестцового отдела позвоночника занимают одно из первых мест [6, 7]. В настоящее время болевой синдром в области спины, обусловленный дегенеративными заболеваниями позвоночника, рассматривается как дорсопатия [14, 15].
Основными причинами дорсопатий являются остеохондроз, дисфункция фасеточных суставов, частичный надрыв фиброзного кольца, пролабирование межпозвонковых дисков, в ряде случаев — формирование грыжи диска, спондилолистез, стеноз позвоночного канала, остеопороз. Важными патогенетическими факторами являются компрессионные механизмы и рефлекторные влияния, сопровождающиеся воспалительным процессом, микроциркуляторными расстройствами, их сочетанием [1]. Дегенеративные поражения поясничного отдела позвоночника рассматриваются как дегенеративное заболевание диска [17, 18]. Корешковые синдромы выявляются у 37,4% больных с дегенеративно-дистрофическими изменениями межпозвонковых дисков [5].
Причинами дегенеративных изменений в межпозвонковых дисках могут быть повторные травмы, избыточная статическая или динамическая нагрузка, врожденные особенности строения скелета, наследственная предрасположенность, естественные процессы старения. Уменьшение диффузии питательных веществ к пульпозному ядру приводит к нарушению синтеза коллагена и протеогликанов, обезвоживанию диска, при этом уменьшается его устойчивость к механическим воздействиям [12, 17]. В дистрофически измененных коллагеновых волокнах фиброзного кольца появляются трещины и разрывы, что приводит к образованию грыжи межпозвонкового диска [13, 20]. Определенное значение имеют оксидантный стресс, нейрогенное воспаление, аутоиммунные нарушения.
© В.П. Шатрова, К.Т. Месхи, 2008
Zh Nevrol Psikhiatr Im SS Korsakova 2008;108:12:68—70
Грыжа межпозвонкового диска наряду с воздействием на спинномозговые корешки вызывает компрессию корешковых сосудов, тем самым способствуя развитию корешковых сосудистых синдромов. Особенность болевых синдромов при остеохондрозе позвоночника — сочетание рефлекторных мышечно-тонических и миофасциальных синдромов с изменениями в эмоционально-личностной сфере [1, 10]. Даже при купировании острых болей эмоциональные расстройства могут персистировать на протяжении длительного времени, обусловливая дезадаптацию пациента.
Эффективным методом лечения дорсопатий является хирургическое лечение. Вопрос о целесообразности оперативного лечения решается при отсутствии эффекта от комплексного лечения на протяжении нескольких месяцев [4, 9, 11, 19]. Хронизация процесса может привести к пролиферативным изменениям в связочном аппарате, усиливая тем самым стеноз позвоночного канала в зоне грыжевого выпячивания [7, 11].
Широкое развитие современных микрохирургических методов способствует снижению частоты неэффективных вмешательств. Несмотря на это у 20—25% больных после операции не происходит устранения двигательных нарушений вследствие необратимости дооперационных изменений в корешке [8]. Кроме того, наряду с органическими причинами, в формировании болевого синдрома неизбежно участвуют функциональные «генераторные» механизмы боли. Также отмечено, что преморбидные невротические и психопатологические особенности личности в результате длительного болевого синдрома до операции также способствуют декомпенсации заболевания.
Необходимость проведения реабилитационных мероприятий у данной категории больных не вызывает сомнений. Большой интерес представляет возможность медикаментозной реабилитации с учетом ее этапности
икомплексного подхода. В раннем восстановительном периоде, непосредственно после операции, проводится профилактика вторичной рубцовой компрессии, а также мероприятия, направленные на улучшение метаболизма
имикроциркуляции (вазоактивные препараты, нейропротекторы), купирование послеоперационного болевого синдрома (нестероидные противовоспалительные средства, миорелаксанты), активацию трофических процессов (витамины, анаболические препараты), коррекцию психо-вегетативных расстройств (транквилизаторы, антидепрессанты).
68 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2008 |
Учитывая разнонаправленность проводимого лечения в рамках реабилитации, среди лекарственных средств привлекает к себе внимание современный препарат с поликомпонентным действием — мексидол. Препарат является антигипоксантом и антиоксидантом, ингибитором перекисного окисления липидов, мембранопротектором, а также обладает транквилизирующими, анксиолитическими и вегетостабилизирующими свойствами [3]. Указанные свойства мексидола в сочетании с хорошей переносимостью позволяют рассчитывать на высокую клиническую эффективность этого препарата при лечении компрессионно-ишемических невропатий.
Исходя из сказанного, целью настоящего исследования явилось изучение возможности применения мексидола в комплексной реабилитации больных после хирургического лечения по поводу дегенеративных заболеваний позвоночника.
Материал и методы
Висследование был включен 131 пациент (73 женщины и 58 мужчин) в возрасте от 23 до 65 лет с корешковым синдромом, обусловленным грыжами межпозвонковых дисков пояснично-крестцового отдела позвоночника.
По данным МРТ, у всех пациентов имели место протрузии межпозвонковых дисков на уровне поясничнокрестцового отдела позвоночника. У 97 больных имелось поражение поясничного отдела позвоночника на одном уровне, у 34 (26,0%) — на двух уровнях. Наиболее частой локализацией грыжи диска оказывались межпозвонковый промежуток L5-S1 — 62 (47,3%) наблюдения и межпозвонковый промежуток L4-L5 — 35 (26,7%).
Пациенты были рандомизированы в две группы: основную (n=69) и контрольную (n=62). В контрольной группе больные получали курс общепринятой медикаментозной терапии (диклофенак 150 мг/сут, сирдалуд — 8 мг/сут, мильгамма — 2,0 мл/сут, пентоксифиллин 800 мг/ сут в течение 10—14 дней) и немедикаментозное лечение (массаж, иглорефлексотерапия, чрескожная электронейро- и/или миостимуляция). В основной группе дополнительно применялся мексидол 600 мг/сут [500 мг внутривенно капельно при его разведении в 100,0 мл 0,9% раствора хлорида натрия утром или в обед и 100 мг (2 мл) внутримышечно вечером] в течение 10—14 дней. Пациентам были проведены операции: микродискэктомия L4L5, L5-S1 с обеих сторон, межтеловой спондилодез L4-L5, L5-S1 раздвигающимися кейджами.
До начала лечения проводилось комплексное нейроортопедическое обследование, определение интенсивности болевого корешкового синдрома по визуальной аналоговой шкале (ВАШ), магнитно-резонансная томография (МРТ) пояснично-крестцового отдела позвоночника
ирентгенологическое исследование с целью определения уровня поражения, локализации грыжевого выпячивания диска и наличия компрессии дурального мешка, оценка эмоционального статуса пациентов. Состояние пациентов оценивалось на 2-й, 7-й и 14-й день лечения после операции.
Вамбулаторном периоде оценка эффективности реабилитации основывалась на учете динамики жалоб, объективных симптомов заболевания (характер и степень нейроортопедических нарушений, выраженности мышечно-тонических болевых симптомов, тяжести дви-
гательных и чувствительных расстройств), функциональной активности нейромоторного аппарата.
Результаты исследования подвергали статистической обработке методами вариационной статистики с вычислением значений средней арифметической и их сравнения с использованием t-критерия.
Результаты и обсуждение
До операции интенсивность боли по ВАШ в обеих группах была сопоставимой и составляла 8,6±0,3 и 8,8±0,4 балла в контрольной и основной группе соответственно. У 64 (92,7%) пациентов основной и у 59 (95,1%) контрольной группы выявлялось напряжение паравертебральных мышц и болезненность при пальпации остистых отростков позвоночника на уровне поражения.
Наряду с болевым синдромом наблюдались расстройства чувствительности, которые чаще выражались в виде гиперестезии у 81,8% пациентов основной группы и у 82,5% контрольной, иногда гиперестезия сочеталась с гиперпатией — у 25,1 и у 23,5% пациентов в основной и контрольной группе соответственно. Корешковый синдром характеризовался симптомами «натяжения» у 89,2% больных в основной группе и у 85,2% в контрольной на стороне пораженного корешка. У 37,0 и 33,5% пациентов соответственно наблюдалась слабость икроножных мышц.
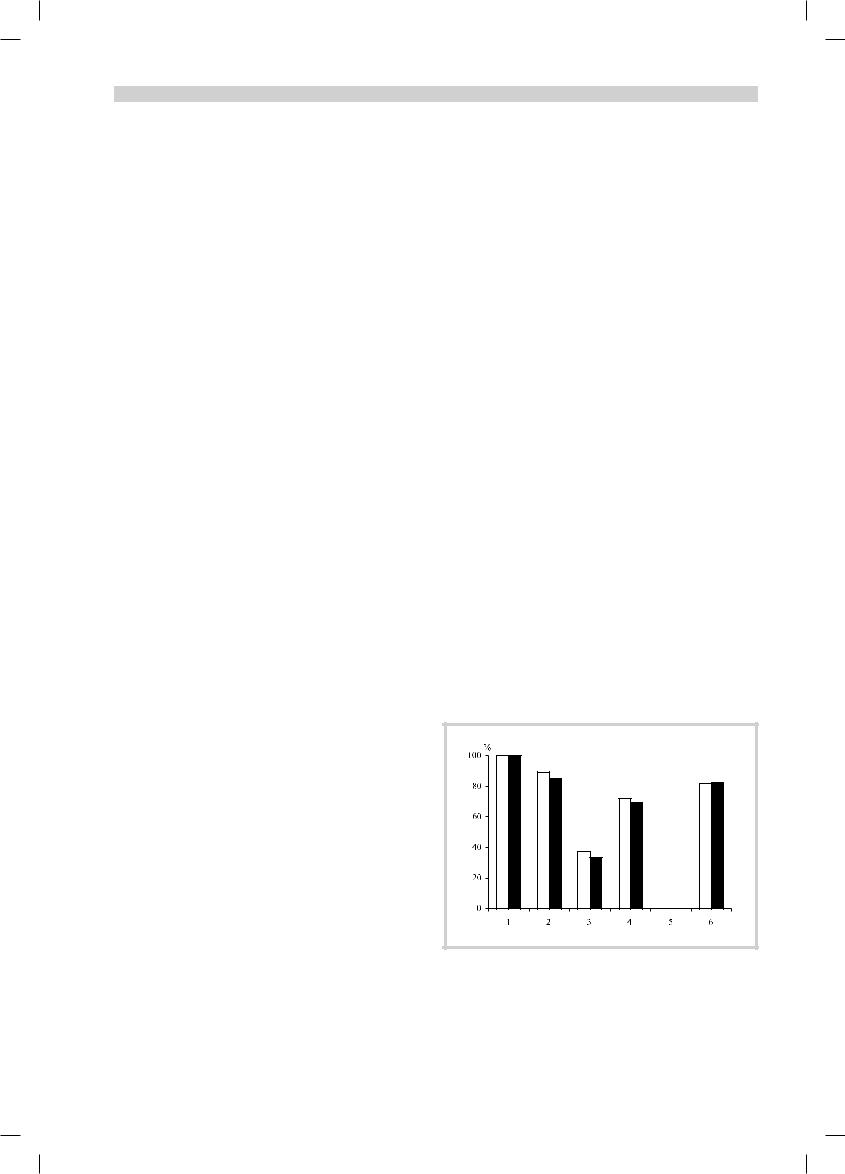
У 71,9% общего количества пациентов при компрессии корешка L4 отмечалось снижение коленного рефлекса, при радикулоишемии S1 корешка — снижение ахиллова рефлекса у 69,7% пациентов. При сдавлении корешка L5 рефлексы, как правило, были сохранены (рис 1).
После проведенного курса медикаментозного лечения у 96,4% основной и у 87,6% пациентов контрольной групп в послеоперационном периоде было отмечено клиническое улучшение, что выражалось в уменьшении болевого синдрома по ВАШ в основной группе до 1,2±0,5 балла, тогда как в контрольной — до 2,3±0,6. Помимо снижения интенсивности болевого синдрома, у пациентов основной группы на фоне применения мексидола отмечался регресс
Рис. 1. Клинические симптомы при корешковом синдроме до |
операции. |
Здесь и на рис. 2: светлые столбцы — основная группа, темные — кон- |
трольная. 1 — болевой синдром; 2 — симптомы натяжения; 3 — двигатель- |
ные расстройства; 4 — рефлекторные нарушения; 5 — расстройства функ- |
ции тазовых органов; 6 — чувствительные нарушения. |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2008 |
69 |

КРАТКИЕ СООБЩЕНИЯ |
|
|
ческой симптоматики у больных основной и контрольной |
|
групп (оживление сниженных рефлексов в 93,2 и 72,6% |
|
соответственно). |
|
Выздоровление наблюдали у всех пациентов основ- |
|
ной группы и у 85,2% контрольной. У 14,8% пациентов |
|
контрольной группы в сроки от 3 до 6 мес после оператив- |
|
ного лечения наступило значительное улучшение, из них |
|
у 6% — сохранялись незначительные боли, у 8,8% отмеча- |
|
лись остаточные неврологические нарушения. При этом |
|
самочувствие больных расценивалось как удовлетвори- |
|
тельное, они были способны выполнять бытовые и про- |
|
фессиональные обязанности, не связанные со значитель- |
|
ной статодинамической нагрузкой на поясничный отдел |
|
позвоночника. |
Рис. 2. Клинические симптомы при корешковом синдроме после |
Заключение |
проведенного курса лечения. |
|
|
Таким образом, включение препарата мексидол в |
неврологической симптоматики (рис. 2). Чувствительные |
комплексную терапию при реабилитации пациентов по- |
сле оперативного лечения по поводу дискогенного ко- |
|
расстройства регрессировали к 14-му дню лечения у 83% |
решкового синдрома, достоверно улучшает регенератив- |
пациентов основной группы и у 74% контрольной. Учи- |
ные процессы в нервной ткани и позволяет с большим |
тывая ранние сроки после оперативного вмешательства, |
эффектом снизить интенсивность болевого синдрома и |
изменения в рефлекторной сфере претерпели незначи- |
улучшить репаративные процессы в поврежденных тка- |
тельные изменения у пациентов обеих групп. Симптомы |
нях. Рекомендуемый режим дозирования мексидола — |
натяжения на фоне лечения регрессировали у всех паци- |
600 мг/сут (500 мг внутривенно капельно при его разве- |
ентов к 14-му дню лечения. |
дении в 100,0 мл 0,9% раствора натрия хлорида в первой |
На амбулаторном этапе реабилитации отмечено пол- |
половине дня) и 100 мг (2 мл) внутримышечно вечером в |
ное купирование болевого синдрома и регресс неврологи- |
течение 10—14 дней. |
ЛИТЕРАТУРА
1. Алексеев В.В. Боль в поясничном отделе позвоночника: диагностика |
11. Подчуфарова Е.В. Боль в пояснично-крестцовой области: диагности- |
и лечение. Трудный пациент 2004;2:4. |
ка, лечение. РМЖ 2004;12:10. |
2.Вейн А.М. Болевые синдромы в неврологической практике. М: 12. Попелянский Я.Ю. Болезни периферической нервной системы. М:
МЕДпресс-информ 2001;368. |
Медицина 1989;463. |
3.Воронина Т.А. Механизм действия и обоснование применения препа13. Попелянский Я.Ю. Ортопедическая неврология (вертебрология). М:
|
рата мексидол в неврологии. Научно-практическая конференция по |
|
МЕДпресс-информ 2003;221. |
|
|
неврологии. М 2000;2—4. |
14. |
Путилина М.В., Гайкин А.В., Казакова Т.В. Дорсопатия поясничного |
|
4. |
Дривотинов Б.В. Неврологические нарушения при поясничном |
|||
|
отдела. Методическое пособие для врачей. М 2007;2. |
|||
|
остеохондрозе. Минск: Беларусь 1979;143. |
15. |
Шостак Н.А. Дорсопатии — совершенствование терапевтических |
|
5. |
Жулев Н.М., Бадзгарадзе Ю.Д., Жулев С.Н. Остеохондроз позвоноч- |
|||
|
возможностей. Трудный пациент 2006;4:10. |
|||
|
ника. Руководство для врачей. Ст-Петербург: Лань 2001. |
16. |
Шустин В.А., Парфенов В.Е., Топтыгин С.В.и др. Диагностика и хи- |
|
6. |
Мовшович И.А., Шотенор Ш.Ш. К вопросу о нестабильности позво- |
|
рургическое лечение неврологических осложнений поясничного |
|
|
ночника. Ортопед травматол протез 1979;5:24—29. |
|
остеохондроза. Ст-Петербург: Фолиант 2006;8. |
7.Мусалатов Х.А., Аганесов А.Г., Шуляк Ю.А. и др. Лечение грыж меж17. Aihara T., Ogasawara A., Itadera E. et al. Intervertebral disc degeneration
позвонковых дисков в поясничном отделе позвоночника. Вестн травматол и ортопед 1997;3:31—34.
8.Ненашева Т.В. Влияние электропунктуры и СМТ на состояние нервно-мышечного аппарата больных, оперированных по поводу грыжи межпозвонкового диска: Автореф. дис. ... канд. мед. наук. СтПетербург 1993;207.
9.Новиков Ю.О. Дорсалгии. М: Медицина 2001;160.
10.Новиков А.В., Яхно Н.Н. Невропатическая боль, патофизиологические механизмы и принципы терапии. РМЖ 2001;7—8:318—327.
associated with lumbosacral transitional vertebrae. A Clinical and anatomical study. J Bone J Surg Br 2005;87:5:687—691.
18.Deyo R.A., Gray D.T., Kreuter W. et al. United States trends in lumbar fusion surgery for degenerative conditions. Spine 2005;30:12:1441—1445.
19.Gibson J., Waddell G. Surgery for degenerative lumbar spondylosis. Cochrane Database Syst Rev 2005;2:CD001352.
20.Hammerberg K.W. New concepts on the pathogenesis and classification of spondylolisthesis. Spine 2005;30:6:Suppl:S4—S11.
70 |
ЖУРНАЛ НЕВРОЛОГИИ И ПСИХИАТРИИ, 12, 2008 |
