
- •Гетерофункциональные соединения
- •Гидрокси-, или оксикислоты
- •Номенклатура
- •Изомерия
- •Химические св-ва
- •Номенклатура солей
- •Фенолокислоты
- •Оксокислоты
- •Номенклатура
- •Лекция 8 Аминофенолы (аф)
- •Аминоспирты
- •Адреналин
- •Лекция 9 Липиды
- •Классификация
- •Нейтральные жиры
- •Химическое строение
- •Физико-химические свойства
- •Остаток олеиновой к-ты Твердый жир
- •Цетилпальмитат Мирицилпальмитат
- •Фосфатидная кислота. Фосфатиды
- •Сфингофосфатиды (сф)
- •Гликолипиды
- •Лекция 10 Углеводы (ув)
- •Моносахариды (мс)
- •Лекция 11 Олигосахариды
- •Химические свойства
- •Полисахариды
- •Фрагмент цепи амилозы
- •Декстрины мелкие Мальтоза
- •Лекция 12 Аминокислоты (ак)
- •Номенклатура
- •Изомерия
- •Классификация
- •Химические свойства
- •Коричневый
- •Применение ак
- •Лекция 13 Белки
- •Диполь-дипольное
- •Функции белков:
- •Лекция 14 Гетероциклические соединения (гцс)
- •Классификация
- •Пятичленные гц с одним гетероатомом Пиррол
- •Химические св-ва
- •Шестичленные гц Пиридин
- •Химические свойства
- •Шестичленные гц с двумя гетероатомами
- •Барбитуровая к-та
- •Конденсированные гцс
- •Пуриновые нуклеиновые основания
- •Гидроксипроизводные пурина
- •Лекция 15 Нуклеиновые к-ты (нк)
- •Химический состав нк
- •Нуклеозиды
- •Мононуклеотиды
- •Аденозинтрифосфат, аденозинтрифосфорная к-та, атф Структура молекулы днк
Номенклатура солей
Молочной к-ты – лактаты, яблочной – малаты,
Винной – тартраты, лимонной – цитраты.
СН3–
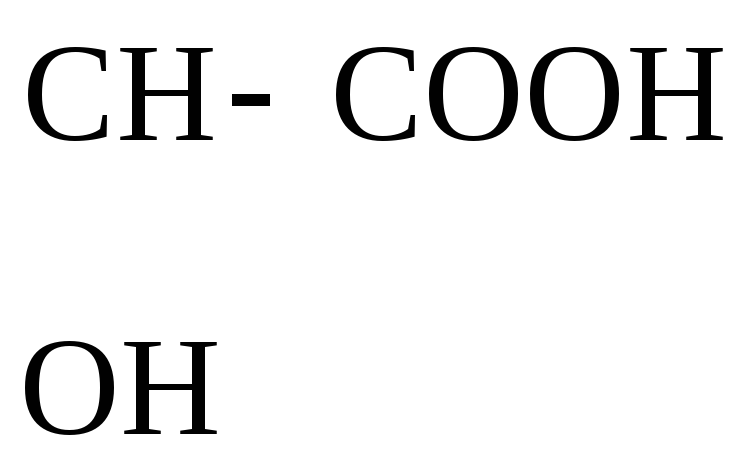 + 2РС15
+ 2РС15
 СН3–
СН3–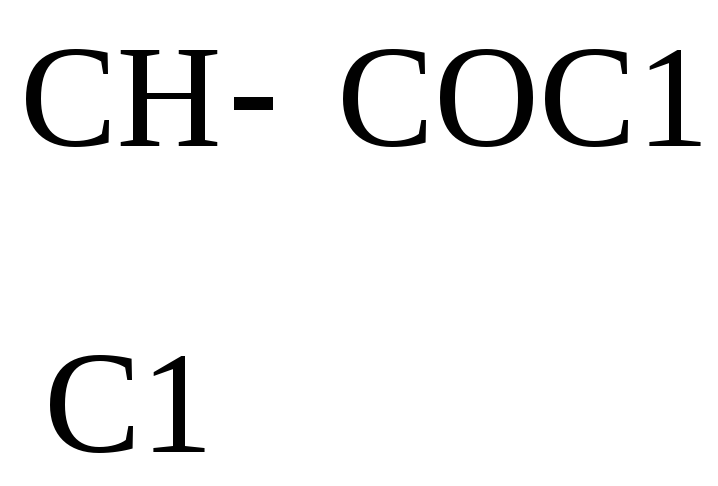 + 2РОС13
+ 2НС1
+ 2РОС13
+ 2НС1
Молочная к-та
II. Р-ции по гр. –ОН
Это р-ции образования алкоголятов, простых и сложных эфиров, галогенопроизводных [НС1 (газ), РС15, SOC12], р-ции окисления.
СН3–
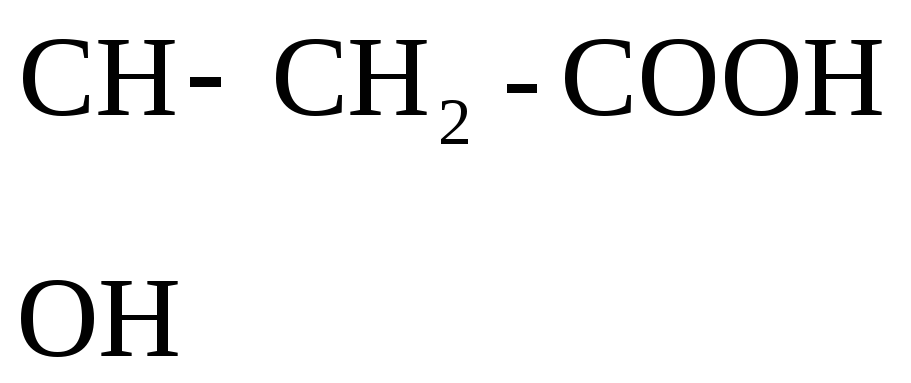 + О
+ О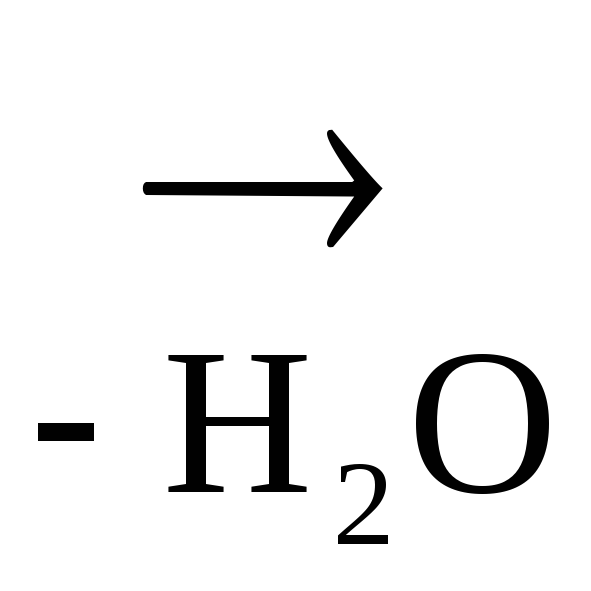 СН3–
СН3–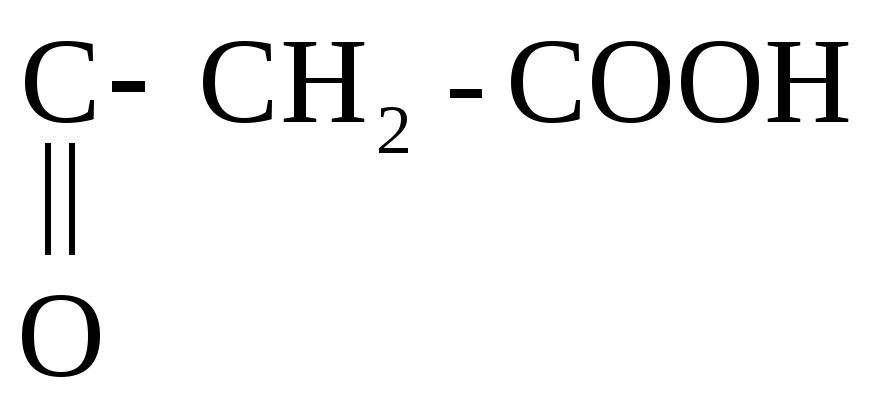 .
.
-гидроксимасляная к-та Ацетоуксусная к-та (АУК)
Ацетон, ацетоуксусная к-та и -гидроксимасляная к-та составляют группу «ацетоновых тел», образующихся в большом количестве в организме при сахарном диабете.
НООС–![]() + О
+ О![]() НООС –
НООС –![]()
Яблочная к-та Щавелевоуксусная к-та (ЩУК)
АУК и ЩУК являются естественными продуктами обмена веществ. В организме образуются при участии кофермента НАД+. Окисление происходит очень легко.
Образование сложного эфира при действии хлоргидрида к-ты:
СН3–![]() + С1 –
+ С1 –![]()
![]() СН3
СН3![]()
При действии Na и РС15 р-ция пойдет по двум группам.
4) Винная к-та и ее производные дают качественную р-цию на диольный драгмент – характерное ярко-синее окрашивание – с р-ром Сu(ОН)2 в щелочной среде.
КООС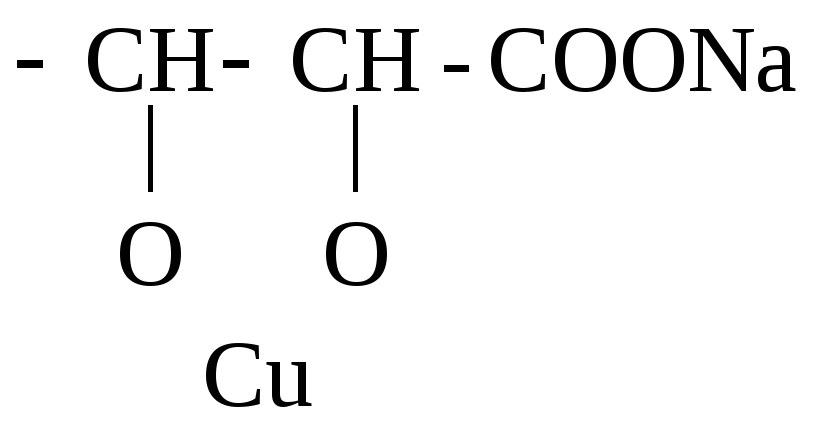
Образовавшееся комплексное соединение под названием реактива Фелинга используется для обнаружения алифатических альдегидов.
III. Специфические р-ции
Они представляют наибольший интерес, т.к. обусловлены взаимным влиянием гетерофункциональных групп.
1) Р-ции дегидратации -, -, -оксикислот
Вследствии наличия групп, способных взаимодействовать друг с другом, молекулы гетерофункциональных соединений способны вступать в р-ции внутри- и межмолекулярного взаимодействия с образованием циклических и нециклических соединений.
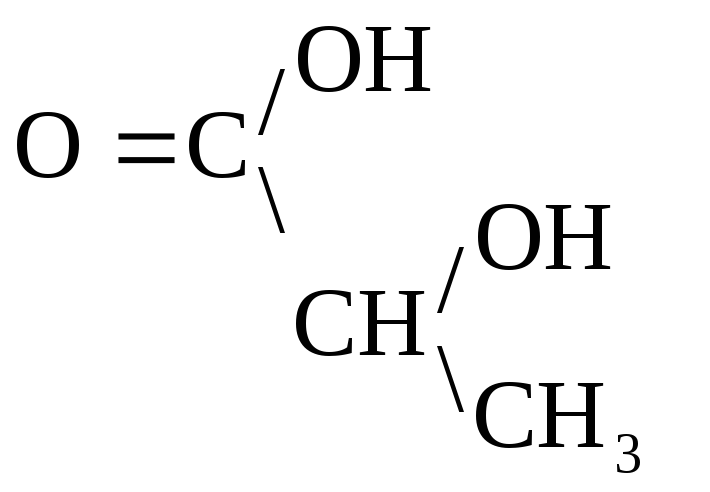
а) Две молекулы -оксик-ты при нагревании выделяют две молекулы воды и образуются ЛАКТИДЫ:
С
+ 
![]()
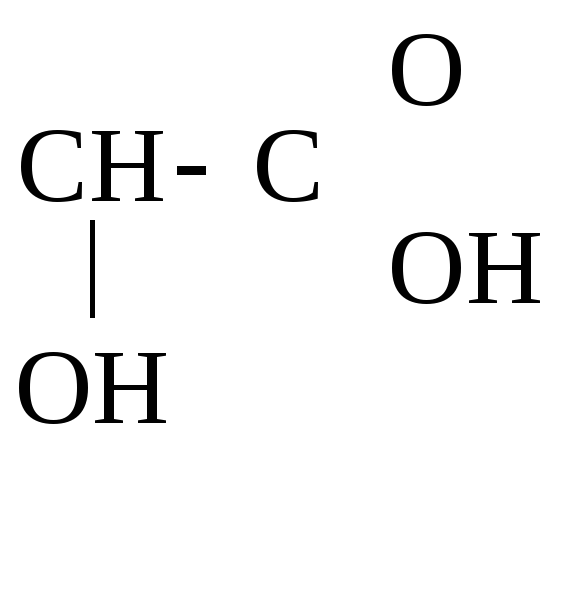
 СН3–
СН3–![]()
Лактид
Молочная к-та
б) -оксик-та, в молекуле которой фрагмент – СН2 – находится между двумя ЭА группами, увеличивающих подвижность атомов Н, подвергается дегидратации с образованием непредельной к-ты:
С
Бутен-2-овая
к-та
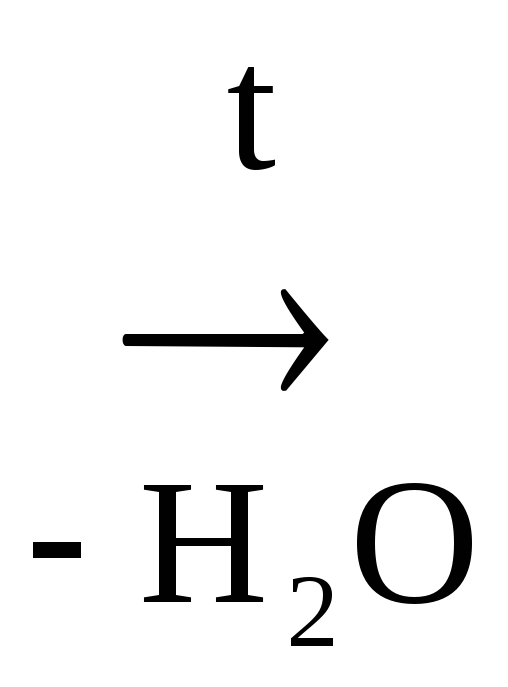 СН3 – СН
= СН – СООН
СН3 – СН
= СН – СООН
-оксимасляная к-та
Яблочная к-та ведет себя как -к-та и при дегидратации превращается в фумаровую:
НООС–![]()
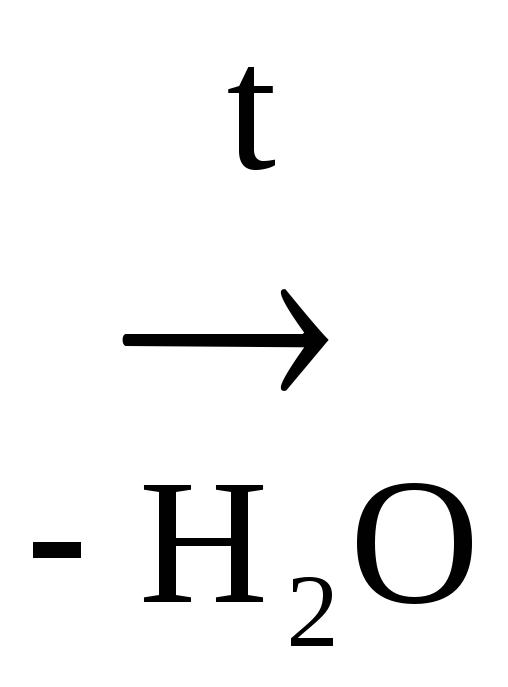
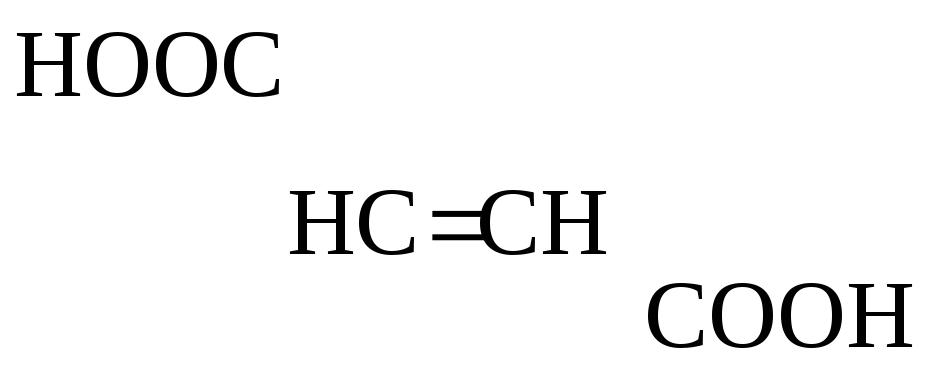
Яблочная к-та Фумаровая к-та
в) -,- и т.д. оксик-ты, в которых две функциональные группы находятся рядом идет внутримолекулярная этерификация с образованием ЛАКТОНА:
ОН НО О![]()
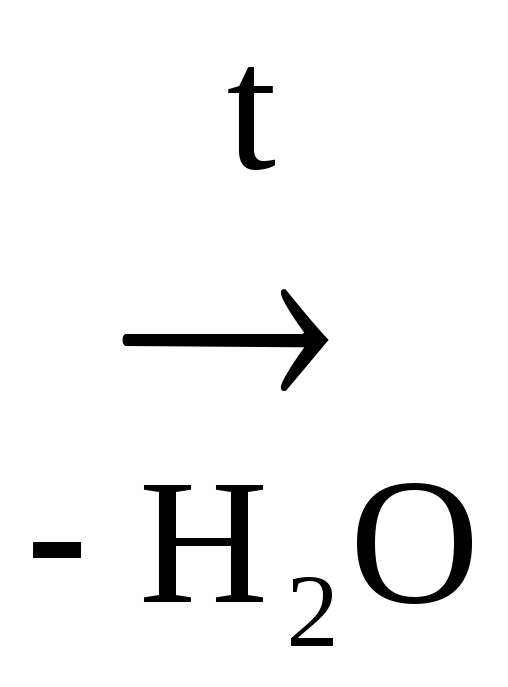
![]()
-Масляная к-та -Бутиролактон
Лактиды и лактоны являются циклическими сложными эфирами и легко гидролизуются в присутствии щелочей с образованием солей:
ОН О![]()
![]()
-Бутиролактон 4-Гидроксибутаноат натрия
2) Наличие двух ЭА групп у одного атома С приводит -оксик-ты к декарбоксилированию:
СН3
– СНОН – СООН
![]() СН3
– СН2ОН
СН3
– СН2ОН
Молочная к-та Этанол
В организме эта р-ция протекает под действием фермента.
В присутствии сильных минеральных к-т углеродный скелет -оксик-т расщепляется по связи С–1 – С–2 с образованием карбоксильного соединения (альдегида или кетона) и муравьиной к-ты:
R
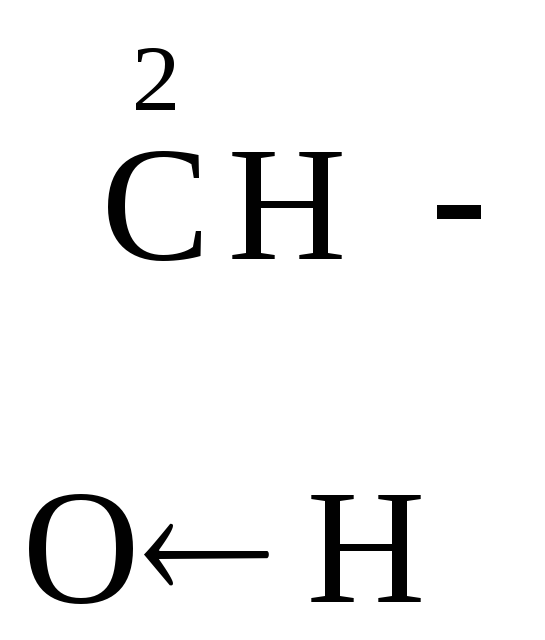
![]()
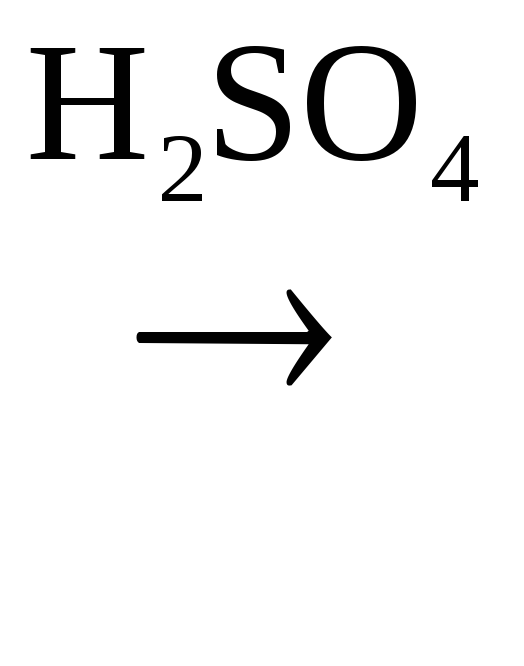 R
-
R
-![]() +H
-
+H
-
![]()
-Оксик-та Альдегид Муравьиная к-та
Особый интерес представляет поведение лимонной к-ты при нагревании в присутствии минеральных к-т. Как -оксик-та она отщепляет НСООН, СО2, образуя в итоге ацетон:
-2СО2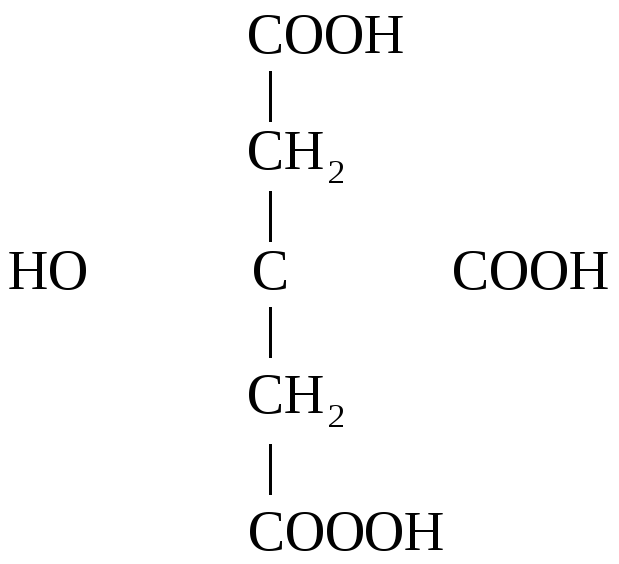
![]()
![]()
![]()


![]()
Лимонная к-та Ацетондикарбоновая Ацетон
к-та
Как -оксик-та она дегидратируется, образуя цис- аконитовую к-ту, участвующую в обмене веществ:
НООС–СН2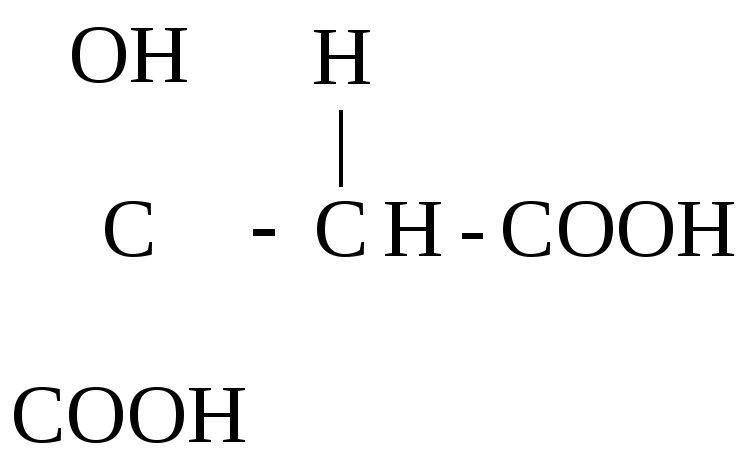
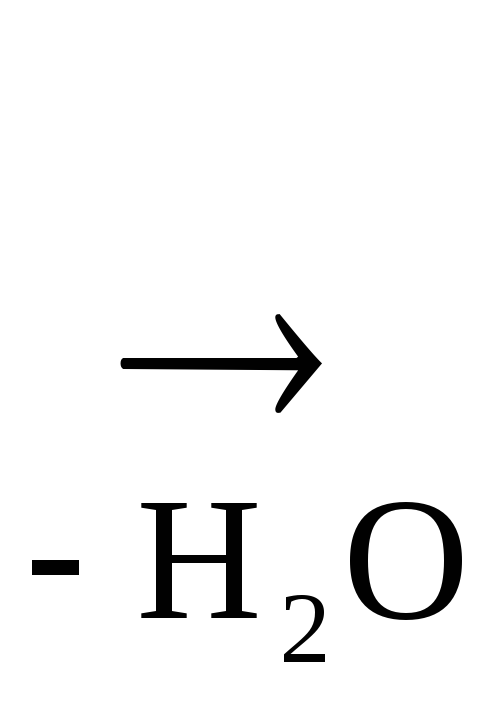 НООС–СН2
НООС–СН2![]()
Аконитовая к-та
При этих процессах выделяется энергия. Процесс последовательных превращений лимонной и других к-т в организме наз-ся циклом Кребса.
Отдельные представители
Гликолевая
к-та содержится в незрелом винограде,
свекле и др.![]()
Тиогликолевая
к-та восстанавливает в белках S–S
мостики цистина в цистин в организме.
![]()
Молочная
к-та содержит один ассиметрический
атом С, в связи с этим существует в виде
пары, энантиомеров. Кроме того, известна
рацемическая молочная к-та.
![]()
Все три формы встречаются в природе. Рацемическая оптически неактивная молочная к-та (кристаллы) образуется из углеводов в результате молочнокислого брожения под действием бактерий. Получить безводную молочную к-ту очень трудно, т.к. обезвоживание ее р-ров сопровождается образованием лактида. Она образуется при скисании молока, квашении капусты, в различных соленьях, выполняя при этом роль консерванта, т.к. способна препятствовать развитию гнилостных бактерий.
Левовращающая D–молочная к-та образуется также в результате молочнокислого брожения, но под действием других бактерий нежели рацелическая молочная к-та. Правовращающая L–молочная к-та образуется в живых организмах в результате расщепления углеводов. Особенно много ее накапливается в мышцах при больших физических нагрузках.
Соли и эфиры молочной к-ты наз-ся ЛАКТАТАМИ.
В медицине используется как прижигающее (80%-ный р-р) при выведении мозолей, бородавок, пигментных пятен.
Лактат железа (II) (СН3СНОНСОО)2Fе 3Н2О хорошо всасывается в кишечнике и хорошо переносится больными при анемии.
Лактат кальция применяют внутрь в тех же случаях, что хлорид и глюканат кальция.
НОСН2– СН2– СН2СООН -Гидроксимасляная к-та (ГОМК) в свободном виде неустойчива, легко отщепляет воду с образованием лактона. В виде натриевой соли используется в медицине как неингаляционное наркозное средство.
НООССН(ОН)СН2СООН яблочная к-та содержит один ассиметрический атом С, поэтому возможно существование ее в виде пары энантиомеров. В природе встречается L-(–)-яблочная к-та (кристаллы), она содержится в ягодах и фруктах. L–яблочная к-та – один из продуктов распада углеводов в живых организмах.
НООССН(ОН)СН(ОН)СООН винная к-та содержит два центра хиральности и теоретически должна существовать в виде четырех стереоизомеров. Однако две формы этой к-ты соответствуют одному соединению (имеется плоскость симметрии) – оптически неактивной мезовинной к-те. Мезовинная к-та по отношению к двум другим формам D– и L–винной к-ты является диастереомером. Таким образом, 2,3-дигидроксибутандионовая к-та (,-дигидроксиянтарная к-та) существует в виде трех стереоизомеров. Кроме того известен рацемат – смесь равных количеств D– и L–винной к-т, называемая виноградной к-той. Большие заслуги в изучении стереохимии винных к-т принадлежат французскому естествоиспытателю Л. Пастеру (1822–1895).
В природе встречается только D-(+)-винная к-та, содержащаяся во многих растениях, особенно много ее в винограде, который служит сырьем для ее получения. Выделяется в виде малорастворимой кислой калиевой соли («винный камень») в процессе винного брожения виноградного сока. Соли и сложные эфиры винной к-ты наз-ся тартратами.
Винная к-та в смеси с содой NaНСО3 под названием «шипучие порошки» применяются как слабительное средство.
НООССН2С(ОН)(СООН)СН2СООН лимонная к-та (2-гидроксипропан-1,2,3-трикарбоновая к-та) – бесцветное кристалическое вещество, хорошо растворимое в воде. Содержится в различных растениях. Впервые была выделена известным химиком К. Шееле (1742–1786) из лимонного сока, где ее содержание достигает 10%. В промышленности получают путем лиминнокислого брожения отходов сахарного производства.
Соли и сложные эфиры лимонной к-ты наз-ся цитратами. Цитрат натрия применяется для консервирования донорской крови. Противосвертывающее действие основано на том, что цитрат натрия связывает ионы кальция в нерастворимый цитрат. Цитрат железа (II) – при анемии.
