
- •устойчивости коллоидов.
- •Виды устойчивости растворов (по
- •Коагуляция ‒ …
- •Факторы, вызывающие коагуляцию
- •Факторы, вызывающие коагуляцию
- •При изучении влияния электролитов на коагуляцию следует учитывать:
- •чем выше заряд коагулирующего иона, тем меньше сп и выше γ электролита.
- •Правило Дерягина ‒ Ландау …
- •Факторы, вызывающие коагуляцию
- •Факторы, вызывающие
- •Особые случаи
- •2. Чередование зон коагуляции
- •4. Сенсибилизация …
- •Защитное число …
- •Процесс перехода свежевыпавшего при
- •Кинетика коагуляции
- •Коагуляция по Смолуховскому М. (1906г.)
- •νкоаг.
- •Коагуляция
- •Уравнение Смолуховского …
- •Спасибо за внимание!

Особые случаи |
|
|
коагуляции |
|
|
|
11 |
|
1.Смесями электролитов; |
|
|
2.Многозарядными |
ионами‒ |
|
коагуляторами |
(чередование |
зон |
коагуляции); |
|
|
3.При смешивании коллоидов с гранулами |
||
разного по знаку заряда (взаимная |
||
коагуляция / гетерокоагуляция); |
|
|
4.Добавлением очень малых количеств |
||
ВМС (сенсибилизация). |
|
|
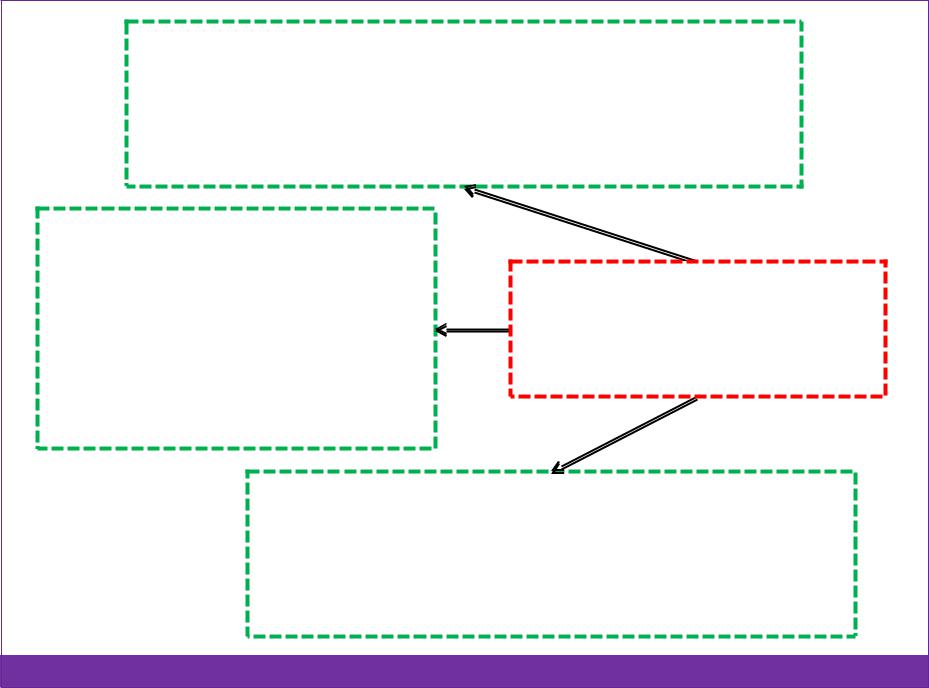
|
Синергизм |
|
(усиление γ электролитов) |
||
FeCl3 + 6KSCN [Fe(SCN)6]K3 + |
||
Аддитивность3KCl |
||
(суммирование γ |
1. Смесями |
|
ионов одинакового |
||
q и близких по |
электролитов |
|
свойствам: Na+, |
|
|
K+) |
Антагонизм |
|
|
||
(уменьшение γ электролитов) |
||
|
PbCl2 + Na2SO4 PbSO4↓ + |
|
|
|
NaCl |
|
|
12 |

2. Чередование зон коагуляции |
||||
|
|
13 |
|
|
‒ ζ |
II |
IV |
VI |
|
‒ 30 мВ |
||||
|
|
|
||
‒ |
‒ |
‒ |
‒ |
|
0 |
+ |
+ |
сэл |
|
|
+ |
|||
+ 30 мВ I |
III |
V |
VII |
|
+ ζ |
|
|
|
|
Причина явления ‒ перезарядка |
||||
коллоидной частицы за счёт адсорбции |
||||
многозарядных ионов. |
|
|||
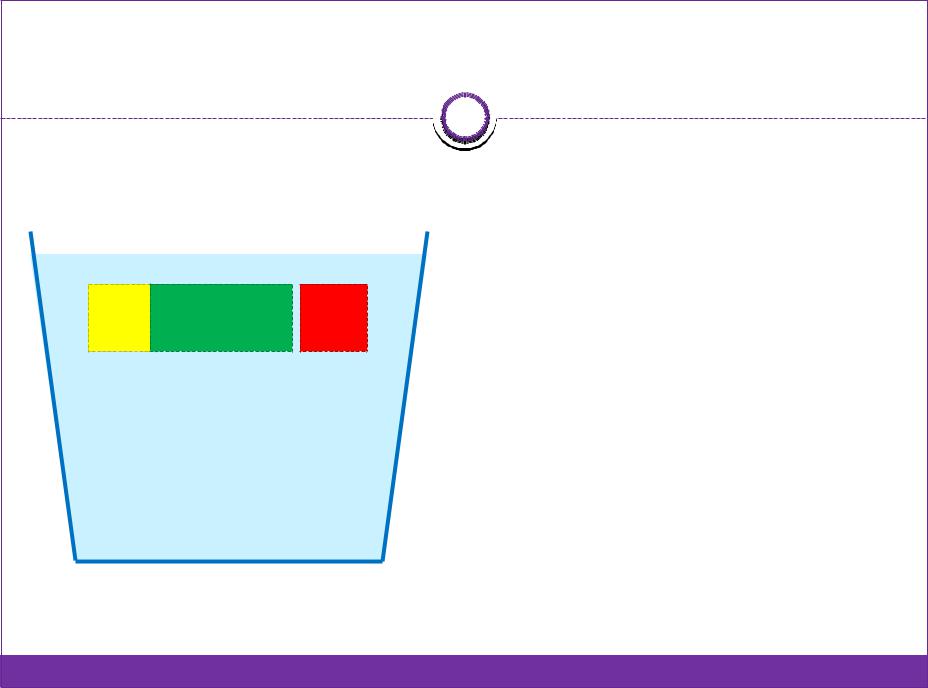
|
3. Гетерокоагуляция |
||
|
|
|
14 |
|
|
|
Причина явления ‒ |
|
|
|
электростатическое |
+ |
0 |
‒ |
притяжение частиц золя |
противоположного q. |
|||
|
|
|
Наиболее полно |
|
|
|
гетерокоагуляция |
|
|
|
протекает при равенстве по |
|
|
|
величине, но различия по |
|
|
|
знаку q гранул 2-х золей. |

4. Сенсибилизация …
15
…вызвана добавлением очень малых количеств ВМС и понижает устойчивость коллоидов.
…связана с особенностями ВМС:
1.образование макроионов с большой адсорбционной способностью;
2.одновременная адсорбция макроионов
на нескольких |
частицах с |
образованием |
|
механизм). |
|

16 |
Коллоидная защита … |
|
|
||
… повышение |
‒ |
|
устойчивости |
||
коллоидов |
|
|
добавлением |
|
|
ВМС в |
+ |
|
концентрация |
||
х, достаточных |
||
для полного |
|
|
адсорбционног |
|
|
о насыщения |
|
|
поверхности |
|
|
мицелл |
Вывод: адсорбционный слой |
|
защищаемого |
||
является механическим |
||
золя. |
||
препятствием для иона ‒ |
||
|
||
|
коагулянта. |

Защитное число … |
|
|
17 |
… min масса ВМС (мг), достаточная для |
|
предотвращения 10 см3 гидрозоля от |
|
коагулирующего действия 1 см3 раствора |
|
NaCl с ω=10% (массовая концентрация 100 г/л). |
|
100 VВМС ωВМС |
|
З.Ч. |
Vзоля |
|
|
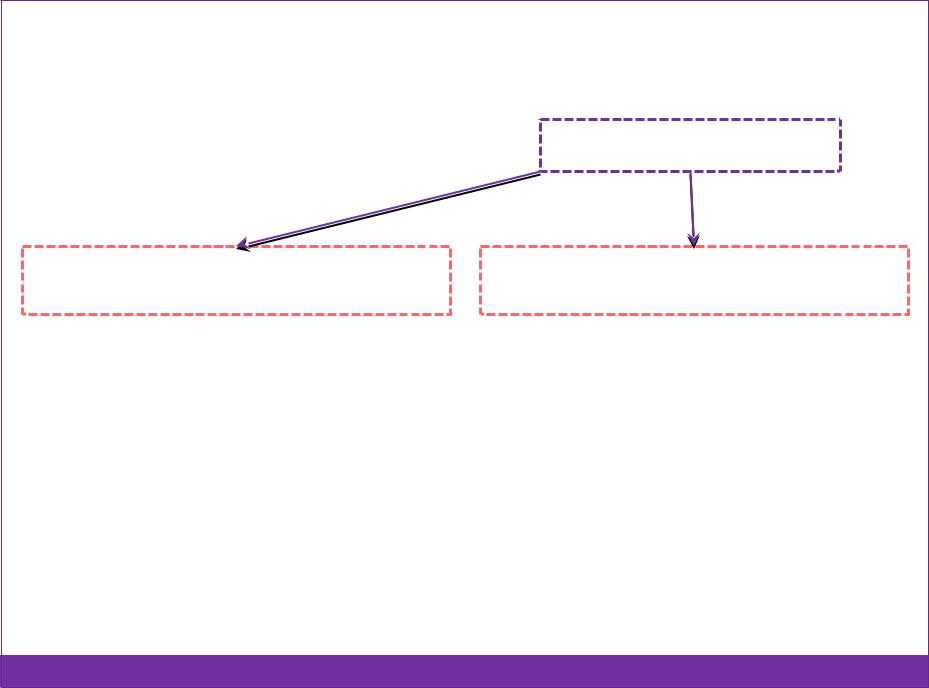
Процесс перехода свежевыпавшего при |
||
коагуляции осадка во взвешенное состояние |
||
|
|
пептизаци |
(золь) под влиянием пептизаторовя‒ |
||
Адсорбционная |
Диссолюционна |
|
|
|
я |
В к л ю ч а ю т с т а д и и : |
||
введение пептизатора; |
|
а) образование пептизатора |
↓Fe(OH)3 |
|
|
+ FeCl3(пепт.) → |
||
а) ↓Fe(OH)3 + HCl → FeOCl (пепт) + 2Н2О |
||
|
|
за счёт хим. реакции; |
{[Fe(OH) ] ·nFe3+·(3n‒x)Cl‒}x+ ·xCl‒ |
||
б) адсорбция ионов пептизатора на поверхности |
||
3 m |
|
|
б) ↓Fe(OH)3 + FeOCl (пепт) → |
||
частиц осадка, появление у них одинакового q и за |
||
{[Fe(OH) ] ·nFeО+·(n‒x)Cl‒}x+ ·xCl‒ |
||
3 m |
|
|
счёт электростатического отталкивания – переход в |
||
|
|
18 |
|
раствор. |
|
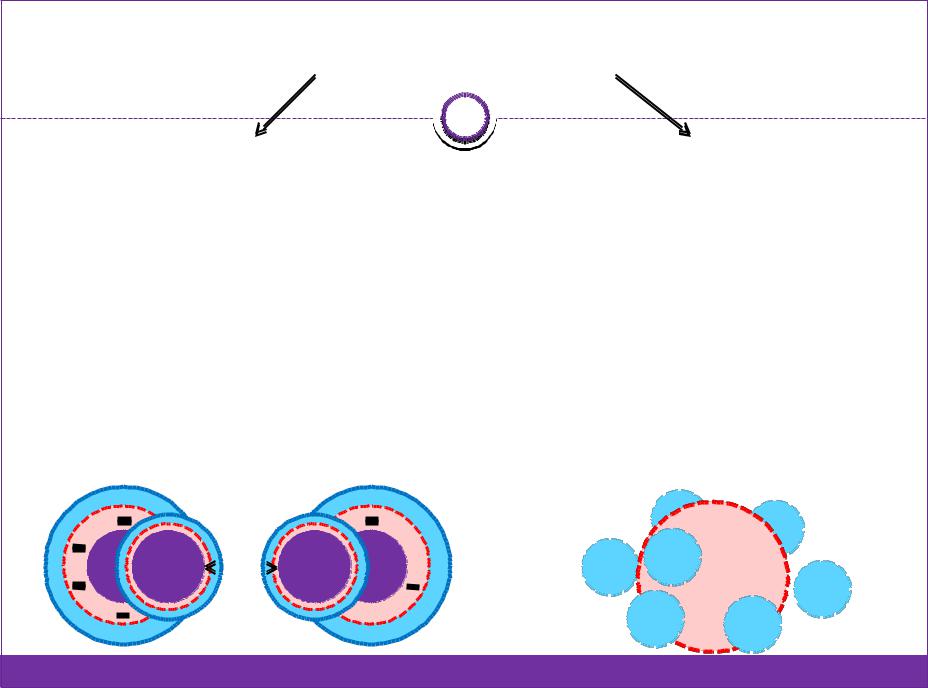
|
Теории коагуляции |
|
||||
|
|
19 |
|
|
|
|
Физическая |
Адсорбционная |
|||||
(ДЛФО) |
(Фрейндлих) |
|
||||
Уменьшение толщины |
Адсорбция ионов – |
|||||
диффузионного слоя и |
||||||
коагулянтов на |
||||||
гидратной оболочки, |
||||||
уменьшение расстояния |
агрегате и грануле, |
|||||
между мицеллами, |
снижение величины |
|||||
возникновение сил |
q и ζ – потенциала, |
|||||
притяжения, коагуляция. |
||||||
При действии ионов- |
коагуляция. |
|
||||
|
10‒9 |
|
|
|
|
|
коагулянтов происходит |
|
|
|
|||
На данном |
- |
- |
|
|||
|
10‒7 |
|
|
|||
сжатие ионной атмосферы. |
|
|||||
расстоянии |
|
|||||
цы сближаются на |
|
|||||
Част+и |
|
++ |
|
|||
действуют силы |
-+- |
- |
||||
расстоянии, где действуют |
|
|||||
силыотталкиванияпритяжения. |
|
|
||||

Кинетика коагуляции |
||
20 |
|
|
νкоаг. |
dсd |
|
dt |
||
|
||
Производная частичной концентрации по |
||
времени, взятая со знаком «‒». |
||
