
Винницкий национальный медицинский университет им. Н.И.Пирогова
Кафедра биологической и общей химии
МЕТОДИЧЕСКИЕ РАЗРАБОТКИ
практических занятий по биоорганической химии для иностранных студентов медицинского и стоматологического факультетов
Винница 2004
Методические разработки утверждены ученым советом Винницкого национального медицинского университета им. Н.И. Пирогова (протокол № от
2004)
Авторы-составители: доц. О.В. Смирнова, проф. А.А. Пентюк, проф. Н.Б.Луцюк, доц. О.Я. Сливка, ст. преп. Т.М. Зелинская, ас. Л.Г. Глухова, ас. О.Г. Cулим
Рецензент – А.С. Азаров, кхн, доцент
Редакционно-издательская группа ВНМУ: Ответственный редактор-Тарасюк С.В. , профессор. Секретарь – Н.Д. Королева, кандидат псих. наук.
Компьютерная верстка - Пунковская С.А.
2
Содержание
1. |
Основные термины и понятия в органической химии. Но- |
|
|
менклатура органических соединений………………………….. |
4 |
2.Пространственное строение органических соединений. |
|
|
|
Энантиомерия. Конформационная изомерия………………….. |
5 |
3. |
Электронное строение углерода и его химических связей. Со- |
|
|
пряжение и ароматичность………………………………………. |
6 |
4. |
Электронные эффекты в биологически активных соединени- |
|
|
ях…………………………………………………………………... |
8 |
5. |
Кислотность и основность биологически активных соедине- |
|
|
ний………………………………………………………………… |
9 |
6. |
Реакционная способность алканов и галогеналканов………….. |
11 |
7. |
Реакционная способность алкенов и аренов…………………… |
12 |
8. |
Гидроксисоединения: спирты и фенолы. Простые эфиры. |
|
|
Тиолы……………………………………………………………... |
14 |
9. |
Нуклеофильное присоединение в оксосоединениях…………... |
14 |
10. |
Нуклеофильное замещение в карбоновых кислотах и их био- |
|
|
логически активных производных……………………………… |
16 |
11. |
Гетерофункциональные биологически активные соединения… |
18 |
12. |
Гетероциклические биологически активные соединения…….. |
20 |
13. |
Моносахариды……………………………………………………. |
21 |
14. |
Олиго - и полисахариды…………………………………………. |
23 |
15. |
Аминокислоты как структурные единицы пептидов и белков... |
25 |
16. |
Пептиды и белки (самостоятельная работа)……………………. |
26 |
17. |
Пептиды и белки…………………………………………………. |
27 |
18. |
Нуклеиновые кислоты…………………………………………… |
29 |
19. |
Липиды……………………………………………………………. |
31 |
20. |
Перечень вопросов к контрольной работе № 1………………… |
33 |
21. |
Перечень вопросов к контрольной работе № 2………………… |
34 |
Тема: Основные термины и понятия в органической химии. Номенклатура органических соединений.
1. Значение темы: основные понятия, используемые в органической химии,
3
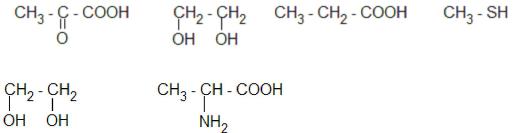
необходимы для объяснения реакционной способности веществ, в том числе биологически активных соединений, в норме и при патологических процессах, а также для понимания химизма действия лекарств в организме человека.
2.Основные вопросы темы:
2.1.Классификация органических соединений: а) по строению углеродного скелета;
б) по природе функциональных групп (примеры функциональных групп и классов соединений).
2.2.Полифункциональные соединения (определение, примеры).
2.3.Гетерофункциональные соединения (определение, примеры).
2.4.Радикалы (определение). Радикалы алканов, алкенов, аренов. Остатки спиртов, карбоновых кислот.
2.5.Первичный, вторичный, третичный атомы углерода.
2.6.Принципы международной номенклатуры (МН) органических соединений.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр. 11-34;
1991, стр. 16-39.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Н.А. Тюкавкиной, 1985, стр. 24-27.
4.Задание для закрепления материала (выполнить в протокольной тетради):
4.1.К какому классу органических соединений относятся следующие вещества
4.2.Назвать соединения по международной номенклатуре:
4.3.Написать формулы соединений: 2-оксипропановая кислота; бутендиовая кислота.
5.Пример тестового контроля:
5.1.Аминалон - принимает участие в обменных процессах головного мозга, имеет строение H2 N-CH2-CH2-CH2-COOH. Назовите его по МН.
5.2.Составная часть коллагена - оксилизин - это 2,6-диамино-5- оксигексановая кислота. Напишите её структурную формулу.
Ответы:
5.1. 4-аминобутановая кислота.
4

5.2.
Тема: Пространственное строение органических соединений. Энантиомерия. Конформационная изомерия.
1.Значение темы: большинство природных соединений существуют в определенных пространственных формах и биохимические реакции протекают с учетом пространственных факторов. Только определенные изомеры проявляют биологическую активность, которая может утрачиваться в процессе изомеризации, а это способно вызывать патологические изменения в организме.
2.Основные вопросы темы:
2.1.Стереоизомерия, конфигурация молекулы.
2.2.Энантиомерия: определение, поляризованный луч, оптическая активность оптические изомеры, проекции Фишера, хиральность, хиральный центр, относительная и абсолютная конфигурация, энантиомеры, диастереомеры, рацемат, глицеральдегид, молочная и винная кислоты, связь энантиомерии с биологической активностью.
2.3.Конформационная изомерия: определение, причина, конформация заслоненная и заторможенная, торсионное напряжение, проекции Ньюмена; конформации циклоалканов (ванны и кресла): угловое напряжение, аксиальное и экваториальное направление заместителей, связь конформационной изомерии с биологической активностью, примеры.
3.Литература:
3.1Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр. 47, 5079, 82-83; 1991, стр. 54-87.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1995. стр. 27-34, 138-148, 243-244.
4.Задания для закрепления материала (выполнить в протокольной тетради):
4.1.Написать строение, конфигурацию, конформацию етаноламина.
4.2.Написать в проекции Фишера энантиомеры аланина CH3-CH(NH2)-COOH, и указать относительную конфигурацию.
5.Примеры тестового контроля:
5.1.Написать строение, конфигурацию и конформацию хлорциклогексана.
5.2.Какая конформация - заслоненная или заторможенная - энергетически более выгодна и почему?
5
5.3.Написать в проекции Фишера энантиомеры молочной кислоты СН3-СН(ОН)-СООН и указать относительную конфигурацию.
Ответы:
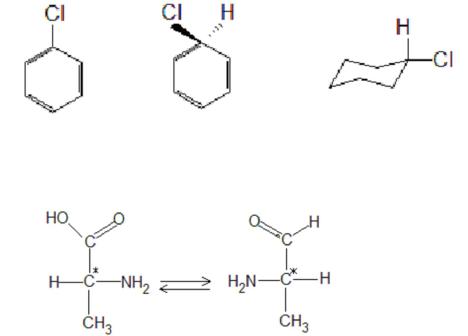
5.1.
5.2.Энергетически выгодна заторможенная конформация, при которой атомы наиболее удалены друг от друга и торсионное напряжение минимально.
5.3.
D- |
L- |
6. Лабораторная работа: Составление моделей органических соединений.
Тема: Электронное строение углерода и его химических связей. Сопряжение и ароматичность.
1.Значение темы: реакционная способность веществ определяется типом связей в их молекулах. Необходимо знать суть явлений сопряжения, ароматичности для объяснения биологической активности соединений в норме и патологии.
2.Основные вопросы темы:
2.1.Типы гибридизации атома углерода. Электронное строение сигма и пи связей.
2.2.Принцип и основной вывод метода молекулярных орбиталей.
2.3.Сопряжение в органических соединениях.
2.3.1.Сопряжение систем с открытой цепью (бутадиен); определение понятий сопряженная система и сопряжение, виды сопряжения, примеры, энергия сопряжения (делокализации).
2.3.2.Сопряжение и ароматичность в системах с замкнутой цепью (арены, гетероциклы):
ароматичность (определение), признаки ароматичности, пиррольный и пиридиновый атомы азота.
2.3.3.Сопряжение и термодинамическая устойчивость.
6
2.3.4.Значение сопряжения и ароматичности для биологических систем.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И, Биоорганическая химия, 1985, стр. 29-
31, 35-42, 1991, стр. 40-48.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, стр. 34-42.
4.Задание для закрепления материала (выполнить в протокольной тетради):
4.1. Докажите ароматичность имидазола.
4.2.Указать тип гибридизации атомов углерода в молекулах уксусной кислоты и пиррола.
5.Пример тестового контроля:
5.1.Что такое сопряжение? Какой вид сопряжения в молекуле анилина?
5.2.Укажите тип гибридизации атомов углерода и строение связи углерод-
углерод в молекуле ацетальдегида.
5.3. Укажите признаки ароматичности нафталина.
Ответы:
5.1.Сопряжение - это перераспределение электронной плотности в системе пи-связей, приводящее к стабилизации системы.
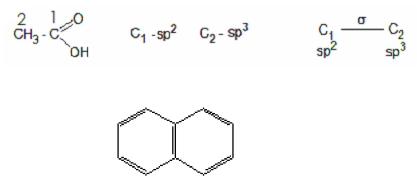
5.2.
5.3.
нафталин
а) плоский скелет молекулы вследствие sp2- гибридизации атома углерода.
б) непрерывность цепи сопряжения - , . в) правило Хюккеля 4n + 2 = 10, n = 2.
Тема: Электронные эффекты в биологически активных соединениях
7
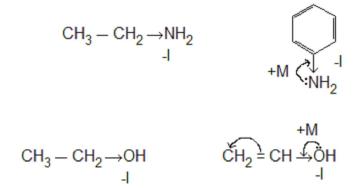
1.Значение темы: одним из факторов, определяющих реакционную способность соединений, является перераспределение электронной плотности, вследствие различной электроотрицательности атомов элементов, и электронные эффекты.
2.Основные вопросы темы:
2.1.Электроотрицательность атомов разных элементов.
2.2.Индуктивный эффект, причины его появления, графическое изображение.
2.3.Мезомерный эффект, причины его появления, графическое изображение.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия,1985, стр.42-45,
1991,стр.49-51.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, стр. 36 -40.
4.Задания для закрепления материала (выполнить в протокольной тетради):
4.1.Изобразите графически электронные эффекты в хлорэтане и хлорбензоле и укажите их вид и знак.
4.2.Изобразите графически электронные эффекты в этаноле и феноле и укажите их вид и знак.
5.Пример тестового контроля:
5.1.Изобразите графически электронные эффекты в аминоэтане и анилине и укажите их вид и знак.
5.2.Изобразите графически электронные эффекты в этаноле и виниловом спирте и укажите их вид и знак.
Ответы:
5.1.
5.2.
Тема: Кислотность и основность биологически активных соединений.
8

1.Значение темы: кислотно-основные свойства обусловливают реакционную способность биологически активных соединений. Так лекарственные веществаамины используют в виде солей различных кислот, что повышает их растворимость в воде. Образованием тиолятов тяжелых металлов объясняется действие антидота унитиола.
2.Основные вопросы темы:
2.1.Кислотность и основность по Бренстеду и Льюису (привести примеры).
2.2.Кислотность спиртов, фенолов, тиолов: влияние двойной связи, замести телей и длины углеводородной цепи.
2.3.Основность аминов, спиртов; влияние заместителей и длины углеводородной цепи.
2.4.Биологическое значение кислотности и основности органических веществ.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр. 112-
123; 1991, стр. 100-117.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, стр. 42-51.
4.Задание для закрепления материала (выполнить в протокольной тетради):
4.1.Расположите в порядке уменьшения кислотности, графически укажите электронные эффекты в ряду:
а) метанол—трет-бутанол—изопропанол; б) фенол—пара-нитрофенол—пара-аминофенол.
4.2.Расположите в порядке уменьшения основности, графически укажите электронные еффекты в ряду: анилин—пара-метиланилин—пара-аминобензойна кислота.
5.Пример тестового контроля:
5.1.Расположите в порядке увеличения кислотности: этанол, 2-хлорэтанол и объясните причину этого.
5.2.Расположите в порядке увеличения основности: метиламин, диметила-
мин и объясните причину этого. Ответы:
5.1.
В молекуле этанола электронная плотность от радикала смещается к атому кислорода. В молекуле 2-хлорэтанола электронная плотность от радикала стягивается к атомам кислорода и хлора. Поэтому на атоме кислорода в хлорэтаноле электронная плотность будет меньше, чем в мо-
9

лекуле этанола, протон слабее связан с кислородом, легче отщепляется и кислотные свойства выражены сильнее.
5.2.
Вмолекуле метиламина электронная плотность на атоме азота создается неподеленной электронной парой и индуктивным эффектом радикала, что обусловливает высокую основность метиламина. В молекуле диметиламина электронная плотность азота еще выше за счет индуктивного эффекта двух радикалов, поэтому и выше основность диметиламина, чем метиламина.
6.Лабораторная работа:
6.1. Получение этилата натрия и его гидролиз.
Всухую пробирку поместить 3 капли абсолютного этанола и небольшой кусочек металлического натрия, предварительно отжатого от керосина на фильтровальной бумаге. Пробирку закрыть пробкой и собрать выделяющийся газ. Затем пробку убрать и отверстие пробирки поднести к пламени горелки. Отметить результаты. К осадку в пробирке добавить 2- 4 капли этанола, 1 каплю фенолфталеина и 1-2 капли воды. Написать уравнение реакции, отметить результаты опыта, объяснить кислотность спиртов.
6.2. Получение гликолята меди (П).
В пробирку внести 2 капли раствора CuS04 и 2 капли раствора NaOH. Отметить результаты. Затем внести 1 каплю глицерина и встряхнуть. Написать уравнения реакций, отметить результаты опыта, привести пример практического применения этой реакции.
6.3. Образование фенолята натрия и разложение его кислотой.
В пробирку внести 3 капли Н2О, несколько кристалликов фенола и встряхнуть. Отметить растворимость фенола в воде. Затем добавить по каплям раствор NaOH до образования прозрачного раствора. Подкислить этот раствор несколькими каплями соляной кислоты. Написать уравнения реакций, отметить результаты, объяснить значение кислотности фенолов.
6.4. Качественная реакция на хлоргидрат новокаина.
В пробирку внести 5 капель раствора хлоргидрата новокаина и 1 -2 капли раствора AgN03. Напишите уравнение реакции, объясните биологическое значение основности аминов.
Cхема протокола лабораторной работы
10
