
№ |
Название опыта, уравнение и механизм ре- |
Выводы (внешний эффект |
опыта |
акции |
реакции, тип реакции, |
|
|
биологическое и практи- |
|
|
ческое значение. |
|
|
|
|
|
|
|
|
|
Схема располагается на развернутой двойной странице тетради.
Тема: Реакционная способность алканов и галогеналканов.
1.Значение темы: реакции с алканами и их производными протекают в организме человека, а также широко используются для синтеза лекарственных веществ. Поэтому необходимо знать механизмы этих реакций.
2.Основные вопросы темы:
2.1.Способы разрыва химической связи в органических соединениях, свободные радикалы, электрофилы, нуклеофилы (определение, примеры).
2.2.Реакции радикального замещения (SR) в алканах, электронное строение С–С связи, механизм реакции; понятие о цепных процессах.
2.3.Биологическое значение свободных радикалов:
-образование свободных радикалов в организме человека;
-участие свободных радикалов в биохимических процессах в норме;
-токсическое действие свободных радикалов;
-обрыв свободно-радикальных реакций, антиоксиданты.
2.4.Механизм нуклеофильного замещения в галогеналканах, значение этой реакции.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр.158160, 172-174; 1991, стр. 149-152, 172-173.
3.3.Руководство к практическим занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, стр. 81-83.
4.Задания для закрепления материала (выполнить в протокольной тетради ):
4.1.Опишите механизм хлорирования пропана.
4.2.Опишите графически механизм взаимодействия хлорэтана с метиламином.
5.Пример тестового контроля:
5.1.Опишите механизм бромирования бутана.
11
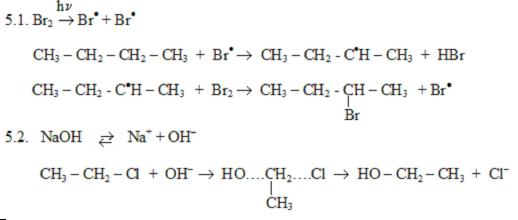
5.2. Опишите механизм взаимодействия хлорэтана со щелочью Ответы:
6.Лабораторная работа:
6.1. Галогенирование алканов (демонстрация).
Вдве пробирки внести по 1 мл гексана и по 1 мл бромной воды. Одну пробирку плотно обернуть черной бумагой. Обе пробирки облучать УФсветом 1-2 мин. Отметить результаты опыта.
Тема: Реакционная способность алкенов и аренов.
1.Значение темы: реакции с алкенами и аренами идут в организме человека. Поэтому необходимо знать механизм их протекания для объяснения процессов в норме и патологии. Кроме того, эти реакции широко используются для синтеза лекарственных веществ; поэтому знание механизма реакций даст возможность синтезировать вещества с заданными свойствами.
2.Основные вопросы темы:
2.1.Реакции электрофильного присоединения (АE) в алкенах: электронное строение двойной связи, механизм реакции АE; гидрирование, галогенирование, гидрогалогенирование, гидратация алкенов. Правило Марковникова. Примеры реакций гидрирования и гидратации алкенов в биологических системах.
2.2.Реакции электрофильного замещения (SE) в аренах: электронное строение бензола, механизм реакции SE; галогенирование, алкилирование, нитрование, сульфирование бензола и его производных. Ориентирующее действие заместителей в бензольном ядре. Биологическое значение реакций замещения в бензольном ядре.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр. 131-
152; 1991 стр. 124-142.
12
3.3Руководство к практическим занятиям по биоорганической химии, под ред. Тюкавкиной Н.А. 1985, стр. 61-80.
4.Задания для закрепления материала (выполнить в протокольной тетради):
4.1.Опишите графически механизм гидратации пропена.
4.2.Опишите графически механизм реакции метилирования бензойной кислоты.
5.Пример тестового контроля:
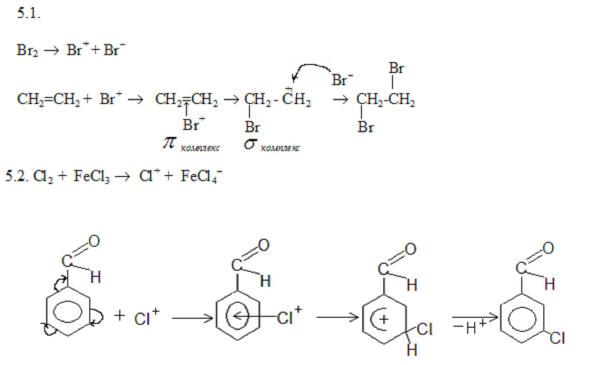
5.1.Опишите графически механизм бромирования этилена.
5.2.Опишите графически механизм хлорирования бензальдегида.
Ответы:
комплекс |
комплекс |
6.Лабораторная работа:
6.1. Получение этилена и его свойства (демонстрация).
В сухую пробирку вносят 1 мл смеси С2Н5ОН и Н2SO4конц, немного оксида алюминия, закрывают газоотводной трубкой и осторожно нагревают. Газ, который выделяется, пропускают через раствор перманганата калия, затем– через бромную воду. Сделать выводы.
6.2. Образование триброманилина.
В пробирку вносят 1 каплю анилина, 1 мл воды, хорошо встряхивают и добавляют 2-3 капли бромной воды. Сделать выводы.
6.3. Нитрование бензола.
13
В сухую пробирку вносят 10 капель бензола и осторожно добавляют 10 капель нитрующей смеси, хорошо встряхивают. Содержимое пробирки выливают в другую пробирку с 5 мл воды. Отметить появление запаха. Сделать выводы.
Тема: Гидроксисоединения: спирты и фенолы. Простые эфиры. Тиолы.
1.Значение темы: изучение реакционной способности кислород- и серосодержащих биологически активных соединений даст возможность прогнозировать превращение этих соединений в организме человека.
2.Основные вопросы темы :
2.1.Механизм реакций нуклеофильного замещения и элиминирования в спиртах. Биологическое значение этих рекций.
2.2.Простые эфиры. Образование пероксидов. Доброкачественность диэтилового эфира.
2.3.Тиолы. Биологическое значение их.
2.4.Окисление спиртов, фенолов, тиолов. Билогическое значение этих реакций.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия.1985,1991.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, 1991.
3.4.Рево А.Я., Зеленкова В.В. Малый практикум по органической химии,
1980.
Тема: Нуклеофильное присоединение в оксосоединениях.
1.Значение темы: изучение механизмов нуклеофильного присоединения в оксосоединениях дает возможность прогнозировать химические превращения альдегидов и кетонов в организме человека.
2.Основные вопросы темы:
2.1.Электронное строение оксогруппы. Механизм нуклеофильного присоединения (АN) к тригональному атому углерода.
2.2.Взаимодействие со спиртами; механизм образования полуацеталей и ацеталей. Их биологическое значение.
2.3.Взаимодействие с аминами: механизм присоединения-отщепления. Биологическое значение иминов.
14
2.4.Альдольная конденсация: механизм щелочного катализа; биологическое значение (синтез в организме цитрата (лимонной) и нейраминовой кислот).
2.5.Окисление и восстановление альдегидов и кетонов. Примеры этих реакций в организме человека.
3.Литература:
3.1.Конспект лекции.
3.2.Тюкавкина Н.А., Бауков Ю.И., Биоорганическая химия, 1985, стр. 197-
203; 1991, стр. 181-194.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, стр. 93-108, oп. 23,26 (стр. 106,107).
3.4.Рево А.Я. и др. Малый практикум по органической химии, 1980, oп. 29,35 (стр. 50, 52).
4.Задание для закрепления материала (выполнить в протокольной тетради).
4.1.Описать графически механизм образования полуацеталя и ацеталя при взаимодействии пропаналя и этанола.
4.2.Описать графически механизм взаимодействия пиридоксальфосфата с метиламином.
4.3.Описать графически механизм синтеза нейраминовой кислоты.
5.Примеры тестового контроля:
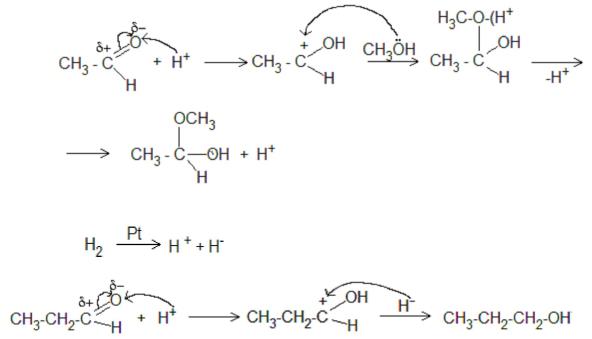
5.1.Описать механизм образования полуацеталя при взаимодействии ацетальдегида и метанола.
5.2.Описать механизм восстановления пропаналя.
Ответы:
5.1.
5.2.
15
6.Лабораторная работа:
6.1. Окисление формальдегида гидроксидом меди (II).
Впробирку внести по 5 капель раствора гидроксида натрия и воды, добавить 1 каплю раствора сульфата меди (II). Отметить результаты. Добавить 3 капли раствора формалина. Пробирку осторожно нагреть до кипения. Написать уравнения реакций, отметить внешний эффект, объяснить результаты. Значение реакции для клинического анализа.
6.2. Открытие ацетона йодоформной пробой.
В пробирку поместить 1 каплю раствора йода в йодиде калия и добавить почти до обесцвечивания по каплям раствор гидроксида натрия. К обесцвеченному раствору добавить 1 каплю ацетона. Написать уравнения реакций, отметить внешний эффект, объяснить результаты и биологическое значение.
Тема: Нуклеофильное замещение в карбоновых кислотах и их биологически активных производных.
1.Значение темы: изучение механизмов нуклеофильного замещения в карбоновых кислотах дает возможность прогнозировать химические превращения карбоновых кислот и их производных в организме человека.
2.Основные вопросы темы:
2.1.Электронное строение карбокси-группы и карбоксилат-иона.
2.2.Кислотность карбоновых кислот. Влияние заместителей на кислотность
карбоновых кислот.
2.3.Соли карбоновых кислот, схема образования, роль в организме человека.
2.4.Механизм нуклеофильного замещения (SN) у тригонального атома углерода: образование и гидролиз сложных эфиров и тиоэфиров. Механизм кислотного катализа реакции этерификации; механизм кислотного и щелочного гидролиза сложных эфиров. Образование и гидролиз сложных эфиров и тиоэфиров в организме человека.
2.5.Декарбоксилирование карбоновых кислот: пирувата (пировиноградной кислоты), 3-оксобутирата ( - кетомасляной), цитрата (лимонной).
3.Литература:
3.1.Конспект лекций.
3.2. Тюкавкина Н.А., Бауков Ю.И.. Биоорганическая химия, 1985, стр. 193197,114, 117-118,204,207-209.236,245-249,1991,стр. 194-206.
3.3.Руководство к лабораторным занятиям по биоорганической химии, под ред. Тюкавкиной Н.А., 1985, стр. 109-110. 113-114.
16
3.4. Рево А.Я. и др. Малый практикум по органической химии, 1980, on. 46,47 (стр. 61).
4.Задания для закрепления материала (выполнить в протокольной тетради):
4.1.Расположить в порядке увеличения кислотности следующие кислоты: оксалат (щавелевая), ацетат( уксусная),монохлорацетат ( монохлоруксусная).
4.2.Описать графически механизм образования и гидролиза (кислотного и щелочного) метилацетата.
4.3.Написать схемы реакций образования производных ацетата (уксусной кислоты): натриевой соли, ангидрида, хлорангидрида, амида.
4.4.Знать формулы следующих кислот: формиат (муравьиная), ацетат (уксусная), пропионат (пропионовая), бутират (масляная), хлорацетат (хлоруксусная), оксалат (щавелевая).
5.Примеры тестового контроля:
5.1.Какая кислота более сильная и почему: ацетат (уксусная) или монохлорацетат (монохлоруксусная)?
5.2.Описать графически механизм образования и гидролиза этилпропионата
сиспользованием кислотного катализа.
Ответы:
5.1. Более сильная монохлорацетат:
за счет отрицательного индуктивного эффекта атома хлора электронная плотность смещается в его сторону и протон карбокси-группы лучше отщепляется.
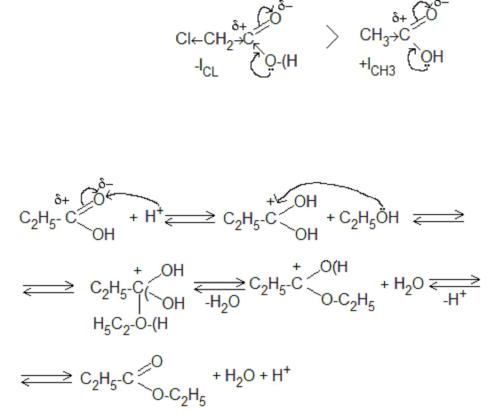
5.2. Механизм етерификации:
17
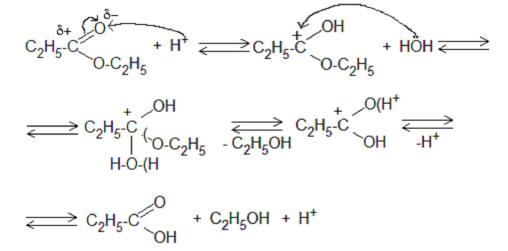
Механизм гидролиза:
6. Лабораторная работа:
6.1. Сравнительная оценка силы кислот.
На полоску универсальной индикаторной бумаги нанести рядом по капле растворов хлоридной (соляной), формиата (муравьиной), ацетата (уксусной), оксалата (щавелевой) и дистиллированной воды. Определить рН и сделать выводы.
6.2. Идентификация щавелевой кислоты в виде кальциевой соли.
В пробирку внести 4-5 капель раствора оксалата натрия и 2 капли раствора хлорида кальция. Выпавший белый осадок оксалата кальция разделить на две пробирки, затем в одну пробирку добавить 1-2 капли ацетата, в другую 1-2 капли хлоридной кислоты. Объяснить результаты.
6.3. Разложение оксалата (щавелевой кислоты) при нагревании.
Насыпать в сухую пробирку оксалата слоем 10-15 мм, закрыть пробкой с газоотводной трубкой и погрузить трубку в другую пробирку с 1 мл раствора гидроксида бария. Нагреть пробирку с оксалатом. Написать уравнения реакций и сделать выводы.
6.4. Получение этилацетата.
В сухую пробирку налить 0,5 мл этанола, 0,5 мл ацетата (ледяной уксусной кислоты), 2-3 капли 96% серной кислоты и осторожно нагреть. Отметить результаты опыта, указать биологическое значение сложных эфиров.
Тема: Гетерофункциональные биологически активные соединения.
1. Значение темы: Геторофункциональные соединения - аминоспирты, окси- и оксокислоты, являются продуктами обмена веществ в организме человека. Реакционная способность их обусловлена взаимным влиянием функциональ-
18
ных групп, что определяет особенности их метаболических превращений в организме.
2.Основные вопросы темы:
2.1.Оксикислоты: лактат (молочная), тартрат (винная), цитрат (лимонная), 3-оксибутират ( -оксимасляная), малат (яблочная); их свойства по окси- и карбокси-группам, изомерия. Химизм образования и превращений в организме человека.
2.2.Оксокислоты: пируват (пировиноградная), ацетоацетат (ацетоуксусная), оксалоацетат (щавелевоуксусная). Кето-енольная таутомерия. Химические свойства по функциональным группам, декарбоксилирование. Кетоновые тела. Химизм образования и превращения оксокислот в организме человека.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр. 239250, 1991, стр. 257-266.
3.3.Руководство к лабораторным занятиям по биоорганической химии под ред. Тюкавкиной Н.А., 1985, стр. 138-141; опыты № 36, 37, 38.
3.4.Рево А.Я. и др. Малый практикум по органической химии, 1980, опыты № 60, 61, 62, 63.
4.Задание для закрепления материала (выполнить в протокольной тетради):
4.1.Напишите формулы энантиомеров лактата (молочной кислоты).
4.2.Напишите кето- и енольную формы пирувата (пировиноградной кислоты), схему реакции ее этерификации с этанолом.
5.Пример тестового контроля:
5.1.Напишите схему образования лактата (молочной кислоты) в организме человека.
5.2.Напишите уравнение взаимодействия оксалоацетата (щавелевоуксусной кислоты) с метанолом.
Ответы:
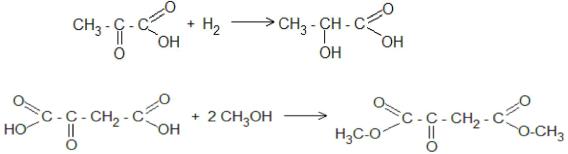
5.1.
5.2.
.
19
6. Лабораторная работа:
6.1. Доказательство наличия двух карбокси-групп в винной кислоте.
В пробирку внести 5 капель раствора тартрата (винной кислоты), добавить 2 капли раствора КОН и стеклянной палочкой потереть стенки пробирки. Отметить изменения. Затем добавить 4-5 капель раствора КОН. Отметить изменения, написать уравнения реакций и сделать выводы.
6.2. Доказательство наличия двух окси-групп в тартрате (винной кислоте).
В пробирку вносят 2 капли раствора сульфата меди и две капли раствора NaOH, затем добавить раствор из первого опыта. Отметить внешний эффект реакции, написать уравнения реакций и сделать выводы.
6.3. Разложение цитрата (лимонной кислоты).
В сухую пробирку с газоотводной трубкой внести кристаллического цитрата (1 см по высоте пробирки) и 1 мл Н2SО4 конц. Смесь нагреть. Конец газоотводной трубки опустить в пробирку с 1 мл гидроксида бария, а затем в пробирку со щелочным раствором йода. Отметить внешний эффект реакции, написать уравнения реакций и сделать выводы.
6.4. Определение доброкачественности ацетилсалициловой кислоты.
В пробирку внести небольшой кусочек таблетки ацетилсалициловой кислоты (аспирина), добавить 5 капель воды и 1 каплю раствора хлорида железа (III). Отметить внешний эффект реакции. Сделать выводы о доброкачественности препарата.
Тема: Гетероциклические биологически активные соединения.
1.Значение темы: Структуры гетероциклов лежат в основе таких биологически важных молекул как витамины, коферменты, азотистые основания нуклеиновых кислот и другие. Они являются основой многочисленных лекарственных веществ. Знание свойств гетероциклов необходимо для понимания природы биохимических процессов и свойств лекарственных веществ.
2.Основные вопросы темы:
2.1.Пиридин, свойства, биологически активные производные: никотиновая кислота, витамин РР, НАД, химическая основа действия его.
2.2.Хинолин, свойства, биологически активные производные.
2.3.Пурин, химические свойства, биологически активные производные: оксипурины, аминопурины, лекарственные вещества, таутомерия.
3.Литература:
3.1.Лекционный материал.
3.2.Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, 1985, стр. 285287, 291-292, 425; 1991, стр. 291-295,301-303.
3.3.Руководство к лабораторным занятиям по биоорганической химии под ред. Тюкавкиной Н.А., 1985, стр. 166-171.
20
