
Карабинцева Фармацевтическая технология методички / Экологическая биотехнология
.pdfчто, в свою очередь, ухудшает условия существования других форм жизни в воде. Отрицательное с гигиенической точки зрения свойство ПАВ — их высокая пенообразующая способность. Хотя ПАВ не являются высокотоксичными веществами, имеются сведения о косвенном их воздействии на гидробионты. При концентрациях 5–15 мг/дм3 рыбы теряют слизистый покров, при более высоких концентрациях может наблюдаться кровотечение жабр. Попадая внутрь живых организмов, у высших животных и человека ПАВ вызывают генетические нарушения, снижают иммунитет, способствуют возникновению злокачественных опухолей. Для микроорганизмов токсичная доза 0,8–4,0 мг/дм3, для водорослей — 0,5–6,0, для беспозвоночных — 0,01–0,9 мг/дм3. Поэтому в настоящее время большую актуальность приобретают исследования, направленные на создание эффективных методов очистки окружающей среды от загрязнения поверхностноактивными веществами.
Среди способов очистки сточных вод в отстойниках — перевод ПАВ в пену, адсорбция активным углем, использование ионообменных смол, нейтрализация катионактивными веществами и другие, однако эти методы дороги и недостаточно эффективны. Главными факторами понижения концентрации ПАВ являются процессы биохимического окисления, сорбция взвешенными веществами и донными отложениями. Степень биохимического окисления ПАВ зависит от их химического строения и условий окружающей среды.
Биодеградация — основной процесс удаления ПАВ из водных и почвенных природных сред. По отношению к этому процессу все поверхностно-активные вещества принято делить на три группы:
1)легкоокисляемые, или так называемые биологически мягкие анионные ПАВ, — алкилсульфат и хлорсульфанол. Эти вещества сравнительно легко окисляются микроорганизмами. В аэротенках очистных сооружений они разлагаются на 80 %, в почве летом — от нескольких суток до 1 мес, зимой — в течение 3–4 мес;
2)трудноокисляемые, или биологически жесткие ПАВ, типа сульфанолов НП-1 и НП-3;
3)вещества с промежуточной степенью доступности для биодеградации.
При попадании в водную среду и почву молекулы ПАВ подвергаются деструкции в результате биохимических и физико-химических
31
процессов и «потребляются» (разрушаются) микроорганизмами, присутствующими в воде, почве и активном иле.
По стадийности деструкции и потребления молекул ПАВ в процессе их биоразложения различают:
1)первичную биоразлагаемость — разрушение структуры молекулы с отщеплением гидрофильных групп, обусловливающее потерю поверхностно-активных свойств молекул ПАВ, что проявляется в первую очередь исчезновением пенообразования;
2)полную биоразлагаемость — дальнейшее усвоение осколков молекул ПАВ микробными сообществами вплоть до разложения на
СО2 и Н2О.
В России действует национальный стандарт ГОСТ Р 50595-93
«Вещества поверхностно-активные. Метод определения биоразлагаемости в водной среде», распространяющийся на метод определения биоразлагаемости поверхностно-активных веществ и устанавливающий условия, приемы и метод определения их биоразлагаемости как таковых, так и в составах бытовых и технических препаратов. Поверхностно-активные вещества при попадании в водную среду разлагаются с различной скоростью под воздействием физикохимических и биохимических факторов в зависимости от условий среды и вида ПАВ. Метод позволяет устанавливать кинетические характеристики процессов биоразложения ПАВ в аэробных условиях в водной среде, а также ориентировочно-допустимый уровень содержания ПАВ в сточных водах, подаваемых в аэротенки. Показатели биоразлагаемости ПАВ, определяемые по ГОСТ Р 50595-93, учитываются при санкционировании ассортимента, объемов производства и применения ПАВ, а также при выборе условий и способов очисткисточныхвод.Методоснованнаопределенииспособностимолекул ПАВ подвергаться биоразложению в аэробных условиях биологических очистных сооружений и водных объектов.
Биохимическое окисление ПАВ проводят как в естественных условиях на полях фильтрации, орошения и в биологических прудах, так и в искусственно созданных условиях — в биофильтрах и в аэротенках. Поля фильтрации, поля орошения и биофильтры функционируютзасчетпочвенныхбиоценозов;биологическиепрудыиаэротенки — за счет биоценозов водоемов.
В природных условиях процессы деструкции многих ПАВ происходят очень медленно и определяются уровнем загрязнения и видом
32
загрязняющего вещества, рН, температурой воды (чем выше температура, тем интенсивнее идет окисление), особенностями микробиоценоза, а в почве — типом и влажностью почвы, содержанием почвенного органического вещества, механическим составом. Для развития микроорганизмов, осуществляющих биоразложение ПАВ в почве, особенно большое значение имеют ее сорбционные свойства. В тяжелых почвах с высоким содержанием глинистых минералов и органического вещества ПАВ разлагаются значительно медленнее, чем в легких песчаных и супесчаных почвах.
В процессах трансформации и детоксикации анионных ПАВ в почве ведущая роль принадлежит бактериям родов Pseudomonas и Bacillus, которые могут адаптироваться к детергентам и использовать их в качестве единственного источника углерода. Активные деструкторы ПАВ встречаются также среди бактерий родов Xanthomonas,
Mycobacterium, Nocardia, Achromobacter.
Данные по биоразлагаемости ПАВ свидетельствуют о необходимости, с одной стороны, синтеза и внедрения в производство легко биоразрушаемых соединений, а с другой — о разработке новых, более интенсивных методов очистки окружающей среды от ПАВ. Эти методы должны основываться на использовании специально полученных высокоактивных чистых культур микроорганизмов — деструкторов ПАВ. Применение таких культур в микробном методе очистки будет способствовать защите окружающей среды от загрязнениясинтетическимисоединениямиисохранениюокружающейчеловека природы.
2.3. Разложение ПАУ
Одна из важнейших причин современного экологического кризиса — все возрастающее химическое загрязнение окружающей природной среды. В ряду приоритетных загрязнителей находятся и полициклические ароматические углеводороды, являющиеся широко распространенными продуктами неполного сгорания ископаемых топлив и органических веществ. ПАУ в виде промышленных выбросов предприятий химической, нефтехимической промышленности, ливневого стока попадают в природные экосистемы, одним из важнейших элементов которых выступает почва. В загрязненных водных экосистемах ПАУ входят в пищевые цепи через биоаккумуляцию и
33
вызывают функциональные расстройства у гидробионтов различного уровня организации.
Полициклические ароматические углеводороды — это высоко-
молекулярные органические соединения бензольного ряда, различающиеся по числу бензольных колец (от 2 до 7). Некоторые низкомолекулярные ПАУ (нафталин, фенантрен, антрацен) менее токсичны и подвержены воздействию микроорганизмов, значительная часть высокомолекулярных ПАУ более устойчива к биодеградации и относится к канцерогенам, тератогенам и генотоксикантам.
Биологические методы очистки окружающей среды, основанные на способности микроорганизмов утилизировать ароматические субстраты, наиболее экономичны и эффективны. Способностью утилизировать соединения с расщеплением ароматического кольца обладают многие почвенные бактерии и грибы. В почвах ПАУ потенциально доступны для многих организмов. Они окисляются отдельными видами бактерий родов Pseudomonas, Mycobacterium, Bacillus,
Flavobacterium, Nocardia и грибов Aspergillus, Penicillium и др. Боль-
шим метаболическим потенциалом в отношении ароматических углеводородов обладают бактерии рода Pseudomonas, способные к полной минерализации или частичной трансформации таких соединений, как нафталин, фенантрен, флуорен и др. Эффективность трансформации ПАУ в почве зависит от ее свойств, возраста загрязнения, концентрации ПАУ, дополнительных источников углерода (в виде корневых выделений, растительных остатков, компоста) и т. д.
Установлено, что биодеградация ПАУ микроорганизмами осуществляется интенсивнее в ризосфере растений, чем непосредственно в почве. Интродуцированные в ризосферу растений хемотаксически активные микроорганизмы-деструкторы способны к колонизации прикорневой зоны растений; осуществляя деструкцию ПАУ в прикорневой зоне, такие микроорганизмы одновременно снижают токсическую нагрузку ПАУ на растения. В ризосфере растений доминирующей группой являются бактерии рода Pseudomonas. Некоторые PGPR Pseudomonas способны стимулировать рост растений за счет синтеза фитогормонов и защищать растения от фитопатогенов, продуцируя антибиотики, сидерофоры и т. д. Бактерии рода Pseudomonas способны также к деградации полициклических ароматических углеводородов. Совмещение в определенных штаммах Pseudomonas фитостимулирующих и биодеградативных функций
34
может быть использовано в фитобиоремедиации загрязненных ПАУ почв. Эффективность деградации ПАУ при совместном применении растений и бактерий-деструкторов существенно повышается.
Способность к биодеградации ПАУ часто обусловлена наличием у микроорганизмов плазмид деградации. Генетический контроль деградации нафталина детально изучен на примере плазмиды NAH7, размером 83 т.п.н. Плазмиды деградации нафталина участвуют и в биодеградации фенантрена благодаря широкой субстратной специфичности кодируемых ими ферментов. ПАУ-катаболитические гены
вбактериальныхклеткахнаходятсянетольковплазмидах(например,
вNAH7), но также и в хромосомах. У Pseudomonas putida OUS82,
утилизирующей фенантрен и нафталин, все гены окисления нафталина до фенолов (кластер pah) содержатся в хромосоме.
Внастоящее время выделены микроорганизмы (в основном относящиеся к псевдомонадам), способные разлагать не только антрахинон и фенантрен, но и ПAУ с большим числом конденсированных ароматических ядер: флуорен, хризен, пирен и др.
Вприродных средах трансформация ПАУ зависит от многих факторов и представляет собой протекающие с различной скоростью
иэффективностью абиотические и микробиологические процессы окисления, восстановления и конъюгации.
Высокая экологическая опасность загрязнения окружающей среды ПАУ, перспективность ее очистки микробиологическими методами и в тоже время ощутимый недостаток фундаментальных и прикладных исследований в этой области определяют необходимость создания широкой коллекции новых ПАУ-деградирующих микроорганизмов, обладающих рядом полезных свойств, всестороннего исследования физиологических, генетических и экологических аспектов микробной деградации ПАУ и разработки на этой основе современных подходов к биоремедиации почв, загрязненных ПАУ.
2.4. Биотрансформация галогенсодержащих органических соединений
Соединения, содержащие в своем составе галогены, — одна из крупнейших групп загрязнителей природной среды. Представители этойгруппыпопадаютвокружающуюсредупрямоиликосвенно,так как входят в состав медицинских препаратов, гербицидов, раствори-
35
телей,лаков,красителей,огнетушителей.Галогензамещенныесоединения склонны к накоплению и постепенному распространению по пищевым цепям. Причина токсичности и устойчивости этих соединений определяется наличием в них трудно расщепляемой галогенуглеродной связи. Основной метод борьбы с загрязнением галогенсо- держащимиорганическимисоединениямивнастоящеевремя—сжи- гание остатков, накапливаемых в результате производственных процессов, а также обжигание или обработка растворителями загрязненных почв. Оба метода не исключают вторичное загрязнение окружающей среды продуктами неполного сжигания отходов (диоксинами). Применение указанных методов не может решить проблему конверсии больших объемов загрязнений.
Более перспективным представляется использование биологических технологий. Скорость и эффективность процессов конверсии опасных веществ при использовании биологических технологий будет обусловлено свойствами и активностью микроорганизмовдеструкторов. Доступность молекулы галогенсодержащих соединений для микроорганизмов зависит от числа и положения атомов галогена в молекуле, которое и определяет последующие этапы катаболизма.Сравнительнолегкоусваиваютсямоногалогенорганические соединения. Соединения, содержащие два атома галогена, более биостойки, причем соединения с орто-положением двух атомов галогена в ароматическом кольце устойчивее, чем с мета-положением, при этом некоторые микроорганизмы, разлагающие моно- и дигалогенированные соединения, не способны использовать полигалогенированные субстраты, и наоборот, штаммы, метаболизирующие полигалогенированные субстраты, оставляли интактными моно- и дигалогенированные соединения. Существуют и такие штаммы, которые способны утилизировать целый спектр от дидо полигалогенированных субстратов, причем одни микроорганизмы могут инициировать расщепление сложного субстрата, а другие могут проводить более поздние реакции.
По способности подвергаться воздействию дегалогенирующих ферментов атом фтора принципиально отличается от атомов хлора и брома, поскольку размер первого ближе к размеру атома водорода. Энергия связи всех галогенов с атомом углерода, кроме фтора, ниже, чем связи С — Н, поэтому фторсодержащие органические соединения наиболее стойкие. В ферментативных реакциях, при протекании которых размеры атома важнее, чем энергия связи, пути под-
36
готовительного метаболизма фторзамещенных соединений и их незамещенных аналогов более сходны, чем при метаболизме хлор- и бромзамещенных соединений.
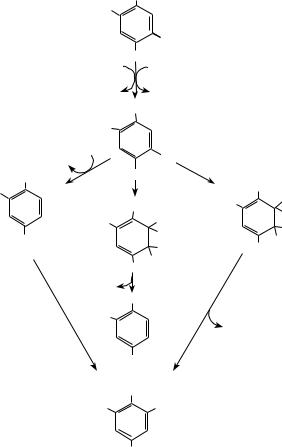
Пути разложения галогенированных молекул, которые могут трансформироваться и в аэробных и в анаэробных условиях, могут быть различными. Например, гербицид 2,4,5-Т может трансформироваться через восстановительное дегалогенирование (путь а), восстановление b, гидратацию с, элиминирование d, окисление оксидазой смешанных функций е [Кузнецов, Градова, 2006]:
O – CH2 – COOH
|
Cl |
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
O2 |
Cl |
NADH |
|
|
|
|
|
H O |
|
NAD+ |
|
|
|
|
|
2 |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
+ |
CHO |
|
|
|
|
H |
|
|
COOH |
|
|
|
HCl |
2 |
|
Cl |
|
|
|
|
|
|
|
|
|
|
||
|
Cl |
|
|
|
|
|
|
OH |
a |
|
c |
|
OH |
|
|
Cl |
|
b |
|
|
|
||
|
|
|
|
OH |
|||
|
|
OH |
|
|
Cl |
|
|
|
|
|
|
|
H |
||
|
Cl |
|
H |
|
|
|
|
|
|
|
|
|
Cl |
||
|
|
|
H |
|
|
|
|
Cl |
|
|
|
|
Cl |
H |
|
|
|
HCl |
|
|
|||
|
|
|
|
|
|
||
|
|
Cl |
|
|
|
|
|
e |
HCl |
OH |
|
|
d |
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
HCl |
|
|
|
|
|
|
|
|
|
|
Cl
 e
e
OH
Cl OH
Cl
37
Низкомолекулярные галогензамещенные алканы и алкены в аэробной среде окисляются в условиях кометаболизма. Участие метанотрофов, использующих метан в качестве источника углерода и энергии в аэробных условиях, увеличивает эффективность этого процесса. Перхлорэтилен (ПХЭ), трихлорэтилен (ТХЭ), дихлорэтилен (ДХЭ) и винилхлорид кометаболизируются метанотрофами. При сочетании анаэробной и аэробной обработки возможна полная деградация устойчивых хлорированных органических растворителей в контаминированных ими средах.
Почвенные микроорганизмы родов Pseudomonas, Nocardia, Achromobacter, Arthrobacter, Acinetobacter способны частично разла-
гать хлорсодержащие ароматические соединения, в том числе и полихлорированные бифенилы (ПХБ). Бактерии родов Alcaligenes,
Acinetobacter, Achromobacter, Pseudomonas, Klebsiella, а также стреп-
томицеты и лигнолитические грибы вызывают окислительную деструкцию полихлорированных полиядерных ароматических соединений. Активация же микромицетами ПХБ приводит к их полимеризации и связыванию с природными полимерами.
В анаэробных условиях ароматическое кольцо не окисляется, но восстанавливается, что показано для бензойной кислоты, фенола и катехола. При отсутствии кислорода замещенные ароматические соединения деградируются более легко, чем незамещенные. Так, в анаэробных условиях пентахлорфенол разлагается эффективнее, чем в аэробных. Полихлорированные ароматические соединения последовательно дегалогенируются до восстановления кольца. В условиях анаэробиоза в донных отложениях замещенные ди- и трихлорфенолы разлагаются в течение 5–7 дней. При использовании смешанной популяции микроорганизмов возможна полная минерализация таких стойких галогензамещенных ароматических соединений, как ПХБ,
ДДТ, 2,4,5-Т .
Применение клонирования in vitro с объединением генов, отвечающих за первичную деградацию различных по структуре синтетических соединений и кодирующих ферменты с широкой субстратной специфичностью, позволяет создавать высокоэффективные и устойчивые штаммы, перспективные для получения на их основе биопрепаратов для очистки природных сред от хлорароматических соединений. По оценкам специалистов микробиологический способ примерно в 50 раз дешевле физико-химических методов. Использование ми-
38
кроорганизмов позволяет решить проблему вторичных загрязнений, так как разрушение ксенобиотиков можно провести без накопления вредных или токсичных веществ. Кроме этого, с помощью специальных штаммов возможно осуществить обезвреживание значительных объемов загрязнителей.
2.5. Разложение пестицидов
Пестициды — химические вещества, предназначенные для борьбысвреднымиорганизмамиивозбудителямиболезнейкакнепосредственно в сельскохозяйственном производстве, так и в ряде других отраслей народного хозяйства. В качестве пестицидов используется значительное число химических соединений, относящихся к более чем 100 классам. Органические соединения, к которым принадлежат пестициды высокой физиологической активности: хлорорганические соединения (гексахлорциклогексан, гептахлор и др.); фосфорорганические соединения (хлорофос, метилнитрофос, карбофос и др.); производные карбаминовой, тио- и дитиокарбаминовой кислот (пиримор, карбин, тиллом); нитропроизводные фенолов (нитрафен, каратан); фталимиды (каптан, фталан); минеральные масла; органические соединения ртути (гранозан, меркуран и др.); хиноны (дихлон); производные мочевины; и др.
Взависимости от способности сопротивляться процессам разложения пестициды подразделяются на слабостойкие (сохраняются в окружающей среде 1–12 нед), среднестойкие (сохраняются 1–18 мес)
иочень стойкие (сохраняются 2 года и более).
Внастоящее время для переработки пестицидов предлагаются главным образом три метода: химические, физические и биологические. Использование физико-химических методов требует значи-
тельных затрат энергии и экономически невыгодно, а самое главное, они не решают проблем экологической безопасности. Так, в процессе сжигания происходит частичный выброс продуктов термогидролиза, бензопирена и т. д., которые не менее опасны, чем исходные вещества. При химической дезактивации непременно встает вопрос об утилизации продуктов химической реакции. Оценивая значение детоксикации пестицидов методами окисления, восстановления, изомеризации, алкилирования или гидролиза, следует учитывать, что во
39
многих случаях конечные продукты метаболизма представляют потенциальную опасность для человека и животных
К биологическим методам относятся методы, основанные на внесении в почву микроорганизмов — деструкторов ядохимикатов. В настоящее время выделено значительное количество штаммов грибов, бактерий, актиномицетов и водорослей, разрушающих эти вещества до нетоксичных соединений. Преимущество использования биологических методов дезактивации пестицидов над физикохимическими объясняется тем, что микроорганизмы минерализуют пестициды в естественном цикле круговорота веществ, при этом затраты энергии на утилизацию незначительны. Однако примененять эти методы нужно с учетом исследования влияния на окружающую среду газообразных продуктов, образующихся при разложении ядохимикатов в почве.
Доминирующая роль во включении пестицидов в природный круговорот веществ принадлежит гетеротрофным микроорганизмам. На скорость разложения пестицидов в почве оказывают влияние, помимо физико-химических свойств того или иного соединения, различные внешние факторы: механические свойства почвы, содержание минеральных и органических веществ, реакция среды, температура и влажность воздуха и почвы и др. В природных экосистемах некоторые пестициды сравнительно быстро разлагаются до конечных продуктов. В первую очередь это простые пестициды и структурно сходные с природными веществами. В ряде случаев такая быстрая трансформация нежелательна, поскольку полезный эффект от применения пестицидов сводится на нет.
В настоящее время предлагают различные биотехнологические способы очистки почвы от избыточных количеств пестицидов, основанные на использовании микроорганизмов — деструкторов ксенобиотиков.
Методами генной инженерии получены микроорганизмы, способные эффективно разлагать 2,4-Д и 2,4,5-Т. Многие почвенные микроорганизмы могут легко метаболизировать хлорированные жирные кислоты (трихлоруксусную кислоту (ТХУ), 2,2-дихлорпропионовую кислоту или ее натриевую соль), которые применяются как герби-
циды. С помощью микроорганизмов Pseudomonas pseudoalcaligenes
возможно разложение хлорированных ароматических пестицидов (2,4-дихлорфеноксиуксусной кислоты и 2,4,5-трихлорфеноксиуксус-
40
