
- •Лабораторная работа 1. Определение коэффициента внутреннего трения и средней длины свободного пробега молекул воздуха.
- •Теоретическое введение
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы.
- •Лабораторная работа 2 Определение коэффициента вязкости жидкости по методу Стокса
- •Теоретическое введение
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 3 Определение коэффициента теплопроводности калориметрическим методом
- •Теоретическое введение
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 4 Определение коэффициентов переноса электронного газа в металлах по их удельным сопротивлениям
- •Теоритическое введение
- •Теория метода измерений
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 5 Определение универсальной газовой постоянной
- •Теоретическое введение
- •Теория метода измерений и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 6 Определение отношения методом Клемана- Дезорма.
- •Теоретическое введение
- •Теория метода измерения и описание установки
- •Порядок выполнения работы
- •Контрольные вопросы
- •Лабораторная работа 7 Определение удельной теплоты плавления твердых тел
- •Теоретическое введение
- •Описание метода измерений и установки
- •Порядок выполнения работы
- •Контрольные работы
- •Лабораторная работа 8 Определение приращения энтропии при плавлении олова
- •Теоретическое введение
- •Описание метода измерений и установки
- •Порядок выполения работы
- •Контрольные вопросы
- •Министерство образования и науки
Теория метода измерения и описание установки
Установка,
применяемая в работе Клемана и Дезорма,
представляет собой стеклянный баллон
вместительностью в несколько литров
 .
.

Баллон наполняется
воздухом при атмосферном давлении
 и плотно закрывается пробкой. Баллон
берется настолько большим, чтобы можно
было пренебречь изменением объема газа
в коленах манометра. Сквозь пробку
проходят две трубки: одна из них соединена
с жидкостным манометром и краном
и плотно закрывается пробкой. Баллон
берется настолько большим, чтобы можно
было пренебречь изменением объема газа
в коленах манометра. Сквозь пробку
проходят две трубки: одна из них соединена
с жидкостным манометром и краном к насосу, вторая имеющая кран
к насосу, вторая имеющая кран соединена с окружающим пространством.
соединена с окружающим пространством.
Отверстие крана
и трубки для выпускания сжатого воздуха
должны быть большими для того, чтобы
воздух выпускался за очень короткое
время, так как в противном случае процесс
нельзя считать адиабатическим. Жидкостью
в манометре является вода. Для
характеристики состояния газа мысленно
выделим внутри баллона произвольную
порцию газа ограниченную замкнутой
поверхностью. Эта поверхность на

 изображена
пунктиром. Она играет роль оболочки, в
которую заключена рассматриваемая
порция газа. В различных процессах, газ,
заключенный в эту «оболочку», будет
расширяться и сжиматься, совершая работу
против давления окружающего газа и
обмениваясь с ним теплом.
изображена
пунктиром. Она играет роль оболочки, в
которую заключена рассматриваемая
порция газа. В различных процессах, газ,
заключенный в эту «оболочку», будет
расширяться и сжиматься, совершая работу
против давления окружающего газа и
обмениваясь с ним теплом.
Газ, заключенный
в сосуд («оболочку») последовательно
проходит через три состояния. Каждое
из этих состояний характеризуется
соответственно давлением
 ,
объемом
,
объемом и температурой
и температурой .
.
Для определения
параметра первого состояния газа с
помощью насоса в баллон («оболочку»)
дополнительно накачивается небольшая
порция воздуха, затем кран
 закрывается. За счет работы сжатия
выполненной внешней силой, температура
и давление воздуха в баллоне («оболочке»)
несколько повышается. Спустя короткое
время сжатый и нагретый воздух в баллоне
охлаждается до комнатной температуры
закрывается. За счет работы сжатия
выполненной внешней силой, температура
и давление воздуха в баллоне («оболочке»)
несколько повышается. Спустя короткое
время сжатый и нагретый воздух в баллоне
охлаждается до комнатной температуры .
После этого водяным манометром измеряется
давлением газа в баллоне.
.
После этого водяным манометром измеряется
давлением газа в баллоне.
Обозначим это
давление
 .
В момент отсчета давления
.
В момент отсчета давления параметры характеризующие состояние
газа внутри «оболочки» имеют следующие
значения
параметры характеризующие состояние
газа внутри «оболочки» имеют следующие
значения .
.

1 состояние:

Затем на короткое
время открывают кран
 ,
при открытом кране
,
при открытом кране часть газа выйдет из баллона и его
давление
часть газа выйдет из баллона и его
давление сравняется с атмосферным давлением
сравняется с атмосферным давлением .
При этом теплообмен воздуха находящегося
в баллоне («оболочке») с окружающим
воздухом не успевает произойти, т.е.,
здесь имеет место адиабатическое
расширение воздуха
.
При этом теплообмен воздуха находящегося
в баллоне («оболочке») с окружающим
воздухом не успевает произойти, т.е.,
здесь имеет место адиабатическое
расширение воздуха .
Воздух в баллоне «оболочке» расширяясь,
совершает работу против внешнего
давления за счет своей внутренней
энергии, благодаря чему, он охлаждается
до температуры
.
Воздух в баллоне «оболочке» расширяясь,
совершает работу против внешнего
давления за счет своей внутренней
энергии, благодаря чему, он охлаждается
до температуры .
В течение этого кратковременного
процесса кран
.
В течение этого кратковременного
процесса кран открыт, параметры характеризующие
состояние газа внутри «оболочки» имеют
следующие значения
открыт, параметры характеризующие
состояние газа внутри «оболочки» имеют
следующие значения .
.
2 состояние:

Затем кран
 быстро закрывается и через некоторое
время газ (воздух) в баллоне («оболочке»)
изохорически нагревается до комнатной
температуры
быстро закрывается и через некоторое
время газ (воздух) в баллоне («оболочке»)
изохорически нагревается до комнатной
температуры и его давление увеличивается. Пусть
давление газа в этот момент равно
и его давление увеличивается. Пусть
давление газа в этот момент равно ,
процесс нагревания газа изображен на
,
процесс нагревания газа изображен на ,
изохорой 2-3, при этом точки 3 и 1 будут
на одной изотерме 1-3, конечное состояние
газа соответствует следующим значениям
параметров:
,
изохорой 2-3, при этом точки 3 и 1 будут
на одной изотерме 1-3, конечное состояние
газа соответствует следующим значениям
параметров:
3 состояние:

По измеренным
давлениям
 можно вычислить отношение теплоемкостей
можно вычислить отношение теплоемкостей

Переход из первого состояния во второе совершается путем быстрого расширения, которое с достаточным приближением можно рассматривать как адиабатическое. Этот переход описывается дифференциальным уравнением адиабаты для идеального газа (20)

Заметим, что
разности давлений
 и
и в сотни и тысячи раз меньше атмосферного
давления
в сотни и тысячи раз меньше атмосферного
давления .
По этой причине для упрощения вычислений
с этими разностями можно обращаться
как с бесконечно малыми дифференциалами
.
По этой причине для упрощения вычислений
с этими разностями можно обращаться
как с бесконечно малыми дифференциалами
 (26)
(26)
 (27)
(27)
Теперь уравнение (20) можно написать так
 (28)
(28)
В состояниях же 1
и 3 температуры газа одинаковы. Поэтому
в этих состояниях произведение
 одно
и то же, следовательно, соответствующие
изменения давления и объема связаны
соотношением
одно
и то же, следовательно, соответствующие
изменения давления и объема связаны
соотношением

или
 (29)
(29)
из этого соотношения совместно с предыдущим получаем
 (30)
(30)
В эту формулу
входит отношение разностей давлений,
а поэтому безразлично в каких единицах
измерять давления. Проще всего разности
давлений измерять в миллиметрах водяного
столба с помощью манометра, как это
показано на рисунке. Из графика процесса
 видно, что
видно, что
 (31)
(31)
 (32)
(32)
С учетом этих формул для определения величины отношения теплоемкостей имеет такой вид:
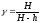 (32)
(32)
