
Обмен+углеводов.+Патохимия.+2011
.pdfРабота № 1. Определение активности ЛДГ в сыворотке крови.
Принцип метода основан на определении скорости снижения реакции катализируемой ЛДГ. Спектрофотометрическое определение оптической плотности при окислении НАДН2 в НАД+ проводят при длине волны 340 нм (тест Варбурга).
ПВК + НАД∙Н + Н+ ← лактатдегидрогеназа → МК + НАД+
Скорость падения Е (оптической плотности) пропорциональна снижению концентрации НАДН и активности ЛДГ.
Ход работы: Настроить спектрофотометр на длину волны 340 нм. В чистую пробирку внести ниже перечисленные реактивы, затем перелить их в кювету спектрофотометра и через 30 секунд снимать показания прибора начиная с Ео через каждую минуту, в течение 3 минут.
Реактивы реакционной смеси:
1.Фосфатный буфер 2,5 мл.
2.Сыворотка крови 0,1 мл.
3. |
Р – р. НАДН |
0,1 мл. |
4. |
Р. – р. ПВК |
0,1 мл. |
Расчет:
Из полученных в ходе измерений трех Ес (экстинций), найти среднее значение ( Е/мин.), которое умножить на коэффициент пересчета в международные единицы (U/л) – 8095.
U/л = 8095 х Е/мин.
Если полученный результат разделить на 16,67, то получим результат в нмоль/л.
В норме активность ЛДГ в сыворотке крови, замеренная при комнатной температуре, находится в пределах 120 – 240 U/л.
Работа № 2. Определение содержания молочной кислоты в сыворотке крови.
41
Принцип метода: Определение молочной кислоты основано на реакции катализируемой ЛДГ (см. выше) и тесте Варбурга – спектрофотометрической регистрации прироста НАДН при длине волны 340 нм, эквимолярному окисленной молочной кислоте.
Ход работы:
1.Этап. Получение безбелкового экстракта молочной кислоты.
В центрифужную пробирку отмерить 0,5 мл. крови (сыворотки) и 1 мл 0,6 М хлорной кислоты. Через 5 мин. инкубации осадить белки центрифугированием при 5 тыс.об/мин., в течение 5 минут. Полученную надосадочную жидкость слить в чистую пробирку и использовать для исследования в следующем этапе.
2.Этап. Запуск реакции и инкубирование. Приготовить реакционную смесь
(табл. 4.)
Таблица 4.
Приготовление реакционной смеси
Реагенты (мл). |
|
Пробирки |
|
|
|
|
|
|
Опыт |
Контроль |
|
|
|
|
|
Буферный раствор |
2,0 |
|
2,0 |
|
|
|
|
Хлорный экстракт |
0,2 |
|
|
|
|
|
|
Р – р. НАД |
0,1 |
|
0,1 |
|
|
|
|
Р – р. хлорной |
|
|
0,2 |
кислоты |
|
||
|
|
|
|
|
|
|
|
Инкубирование провести в термостате при 39 градусах, в течение 30 минут.
3.Этап. Спектрофотометрирование.
Содержимое пробирок опыта и контроля поочередно перелить в чистые кюветы и снять показания экстинций с прибора при длине волны 340 нм., против воздуха.
4.Этап. Расчет: Еоп – Ек = Е
С ммоль/л = Е х 10535 , где 10535 – коэффициент пересчета в ммоль/л.
В нормальной венозной сыворотке крови содержание молочной кислоты находится в пределах – 0,6 – 1,6 ммоль/л.
Клинико диагностическое значение: Определение активности ЛДГ и содержания молочной кислоты в сыворотке крови широко используется в
42
клинической практике для характеристики функционального состояния гликолиза, тканевого дыхания и проницаемости клеточных мембран. Так при снижении или полном прекращении поступления кислорода в ткани, при ингибировании или структурном повреждении ферментов тканевого дыхания происходит повышение обоих биохимических показателей. Однако при большинстве патологических состояний повышенная активность гликолиза и проницаемость мембран сочетаются, и это приводит к более резкому увеличению концентрации МК и активности ЛДГ, например, при воспалительных процессах в почках, мышцах, ишемии тканей и т.д.
Существуют патологические состояния, когда наоборот, активность гликолиза снижается при гипогликемических состояниях, дефиците регуляторных факторов, стимулирующих гликолиз или при его ингибировании.
4.3. ЛЕКЦИЯ № 2
Тема: Катаболизм глюкозы. Гликолиз.
Основные пути катаболизма глюкозы
Катаболизм глюкозы в клетке может проходить как в аэробных, так и в анаэробных условиях, его основная функция это синтез АТФ.
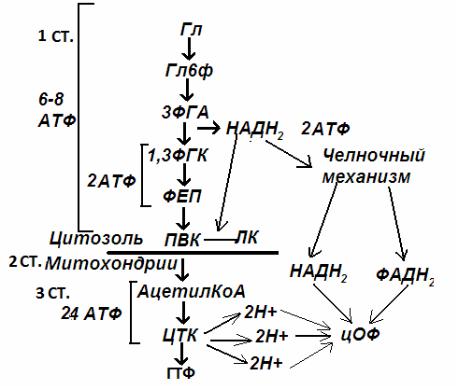
Рис. 5. Аэробное окисление глюкозы
Аэробное окисление глюкозы
43
В аэробных условиях глюкоза окисляется до СО2 и Н2О. Суммарное уравнение:
С6Н12О6 + 6О2 → 6СО2+ 6Н2О + 2880 кДж/моль.
Этот процесс включает несколько стадий (рис.5)
1.Аэробный гликолиз. В нем происходит окисления 1 глюкозы до 2 ПВК, с образованием 2 АТФ (сначала 2 АТФ затрачиваются, затем 4 образуются) и 2 НАДН2;
2.Превращение 2 ПВК в 2 ацетил КоА с выделением 2 СО2 и образованием 2 НАДН2;
3.ЦТК и цепь окислительного фосфорилирования. В третьей стадии происходит окисление 2 молекул ацетил КоА с выделением 4 СО2, 6 Н2О, образованием 2 ГТФ (дают 2 АТФ), 6 НАДН2 и 2 ФАДН2; и суммарным образованием 24 молекул АТФ.
Врезультате аэробного окисления глюкозы образуется 38 (36) АТФ, из них: 4 АТФ в реакциях субстратного фосфорилирования, 34 (32) АТФ в реакциях окислительного фосфорилирования. КПД аэробного окисления составит 65%.
Анаэробный катаболизм глюкозы
Катаболизм глюкозы без О2 идет в анаэробном гликолизе и ПФШ (ПФП).
•В ходе анаэробного гликолиза происходит окисления 1 глюкозы до 2 молекул молочной кислоты с образованием 2 АТФ (сначала 2 АТФ затрачиваются, затем 4 образуются). В анаэробных условиях гликолиз является единственным источником энергии. Суммарное уравнение: С6Н12О6 + 2Н3РО4 + 2АДФ → 2С3Н6О3 + 2АТФ + 2Н2О.
•В ходе ПФП из глюкозы образуются пентозы и НАДФН2. В ходе ПФШ из глюкозы образуются только НАДФН2.
Гликолиз
Гликолиз – главный путь катаболизма глюкозы (а также фруктозы и галактозы). Все его реакции протекают в цитозоле.
Аэробный гликолиз это процесс окисления глюкозы до ПВК, протекающий в присутствии О2.
Анаэробный гликолиз – это процесс окисления глюкозы до лактата, протекающий в отсутствии О2. Анаэробный гликолиз отличается от аэробного только наличием последней 11 реакции, первые 10 реакций у них общие.
44

Этапы гликолиза
В любом гликолизе можно выделить 2 этапа:
• 1 этап подготовительный, в нем затрачивается 2 АТФ. Глюкоза фосфорилируется и расщепляется на 2 фосфотриозы;
•2 этап, сопряжён с синтезом АТФ. На этом этапе фосфотриозы превращаются в ПВК. Энергия этого этапа используется для синтеза 4 АТФ и восстановления 2НАДН2, которые в аэробных условиях идут на синтез 6 АТФ, а в анаэробных условиях восстанавливают ПВК до лактата.
Энергетический баланс гликолиза
Таким образом, энергетический баланс аэробного гликолиза:
8АТФ = 2АТФ + 4АТФ + 6АТФ (из 2НАДН2)
Энергетический баланс анаэробного гликолиза:
2АТФ = 2АТФ + 4АТФ
Общие реакции аэробного и анаэробного гликолиза
1. Гексокиназа (гексокиназа II, АТФ: гексозо 6 фосфотрансфераза) в мышцах фосфорилирует в основном глюкозу, меньше – фруктозу и галактозу. Кm<0,1 ммоль/л. ( М) глюкозо 6 ф, АТФ. (+М) адреналин, индуктор инсулин.
Глюкокиназа (гексокиназа IV, АТФ: глюкозо 6 фосфотрансфераза) фосфорилирует глюкозу. Кm 10 ммоль/л, активна в печени, почках. Не ингибируется глюкозо 6 ф. Индуктор инсулин. Гексокиназы осуществляют фосфорилирование гексоз.
|
|
H |
|
|
|
O |
|
Mg2+ |
H |
|
|
|
O |
|||||||||
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
C |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
АТФ АДФ |
H |
|
|
|
|
|
|
|
|
|
||
H |
|
|
|
|
C |
|
|
OH |
|
C |
|
|
OH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HO |
|
|
C |
|
|
H |
|
|
|
HO |
|
|
C |
|
|
H |
||||||
|
|
|
|
гексокиназа |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H |
|
|
|
C |
|
|
OH |
H |
|
|
|
C |
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
глюкокиназа |
H |
|
|
|
|
|
|
|
OH |
|||||
H |
|
|
C |
|
|
OH |
|
|
C |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
CH2OPO32- |
||||||||
глюкоза глюкозо-6ф
2. Фосфогексозоизомераза (глюкозо 6ф фруктозо 6ф изомераза) осу ществляет альдо кетоизомеризацию открытых форм гексоз.
45

|
H |
O |
|
|
|
|
|
|
|
|
|
CH2OH |
|
|||||||||
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
|
|
OH |
|
|
|
|
|
|
|
|
C |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
H |
|
|
|
C |
|
|
|
H |
|
|
|
|
|
|
C |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
H |
|
|
|
|
|
|
|
|
фосфогексозоизомераза H |
|
|
|
|
|
|
|
|
|
||||
|
C |
|
|
|
OH |
|
|
|
C |
|
|
|
OH |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
2- |
|
|
|
|
H |
|
|
C |
|
|
|
OH |
2- |
||||
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
OPO |
|
|
|
|
|
|
|
|
|
OPO |
|||||||
|
|
CH |
|
|
|
|
|
|
CH |
|||||||||||||
|
2 |
3 |
|
|
|
|
|
|
2 |
3 |
||||||||||||
глюкозо-6ф |
|
|
|
|
|
|
|
фруктозо-6ф |
||||||||||||||
3. Фосфофруктокиназа 1 (АТФ: фруктозо 6ф 1 фосфотрансфераза) осуществляет фосфорилирование фруктозы 6ф. Реакция необратима и самая медленная из всех реакций гликолиза, определяет скорость всего гликолиза.
(+М) АМФ, фруктозо 2,6 дф (мощный активатор, образуется с участием фосфофруктокиназы 2 из фруктозы 6ф), фруктозо 6 ф, Фн.
(+М) глюкагоном, АТФ, НАДН2, цитратом, жирными кислотами, кетоновыми телами.
Индуктор инсулин.
|
|
|
CH OH |
|
|
|
|
|
|
|
CH OPO |
2- |
|||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
C |
|
|
|
O |
|
|
АТФ |
АДФ |
|
|
|
C |
|
|
|
O |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
HO |
|
C |
|
|
|
H |
|
|
|
Mg2+ |
HO |
|
C |
|
|
|
H |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
H |
|
|
C |
|
|
|
OH |
|
|
фосфофруктокиназа |
1 H |
|
|
C |
|
|
|
OH |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||
H |
|
|
C |
|
|
|
OH |
2- |
|
|
|
H |
|
|
C |
|
|
|
OH |
2- |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OPO |
||||||||
|
|
|
|
CH |
OPO |
|
|
|
|
|
|
CH |
|||||||||||
|
|
2 |
3 |
|
|
|
|
|
2 |
3 |
|||||||||||||
|
|
фруктозо-6ф |
|
|
|
|
|
фруктозо-1,6-ф |
|||||||||||||||
4. Альдолаза А (фруктозо 1,6 ф: ДАФ лиаза). Альдолазы действуют на открытые формы гексоз, имеют 4 субъединицы, образуют несколько изоформ. В большинстве тканей содержится Альдолаза А. В печени и почках – Альдолаза В.
|
|
|
CH OPO 2- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
2 |
3 |
|
|
|
|
|
|
|
|
H |
|
|
|
O |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
C |
|
|
|
O |
|
|
|
CH OPO 2- |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
3 |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
C |
|
|
|
H |
|
|
|
|
|
|
O |
|
+ H |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
C |
|
OH |
||||
H |
|
|
|
|
|
|
|
|
|
|
Альдолаза А |
|
|
|
|
|
|
|
|
|
|
|
||
|
C |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
CH2OPO32- |
|||||||||||||
|
|
|
|
|
CH OH |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|||||
H |
|
|
C |
|
|
|
OH |
|
|
|
|
ДАФ |
|
|
|
3-ФГА |
||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
OPO 2- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
2 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
фруктозо-1,6-ф
46

5. Фосфотриозоизомераза (ДАФ ФГА изомераза).
CH OPO 2- |
|
|
|
|
H |
|
|
|
O |
||||||||
|
|
|
|
|
|
|
C |
||||||||||
|
|
2 |
|
|
3 |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
O |
|
|
|
|
|
H |
|
|
C |
|
OH |
|||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|
OH |
Триозофосфат- |
|
|
CH2OPO32- |
|||||||||
CH |
|||||||||||||||||
2 |
|
|
|
изомераза |
3-ФГА |
||||||||||||
ДАФ |
|
||||||||||||||||
6. 3 ФГА дегидрогеназа (3 ФГА: НАД+ оксидоредуктаза (фосфори лирующая)) состоит из 4 субъединиц. Катализирует образование макроэргической связи в 1,3 ФГК и восстановление НАДН2, которые используются в аэробных условиях для синтеза 8 (6) молекул АТФ.
|
H |
|
|
|
O |
2Н3РО4 2НАД |
+ |
2НАДН2 |
|
O |
|
OPO32- |
||||||||
2 H |
|
|
C |
|
2 H |
|
C |
|
||||||||||||
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||
|
|
C |
|
|
OH |
|
|
|
|
|
|
|
C |
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
CH2OPO32- ФГА дегидрогеназа |
|
|
CH2OPO32- |
|||||||||||||
|
|
3-ФГА |
|
|
|
|
|
1,3-ФГК |
||||||||||||
7. Фосфоглицераткиназа (АТФ: 3ФГК 1 фосфотрансфераза). Осуществляет субстратное фосфорилирование АДФ с образованием АТФ.
|
O |
|
OPO32- |
|
COOH |
|||||||||||
|
|
C |
|
|
||||||||||||
|
||||||||||||||||
2 H |
|
|
|
|
|
|
|
2АДФ 2АТФ 2 H |
|
|
|
|
|
|||
|
C |
|
|
OH |
|
|
C |
|
OH |
|||||||
|
|
|
|
|
|
|||||||||||
|
|
|
CH2OPO32- |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
CH2OPO32- |
||||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
фосфоглицераткиназа |
|||||||||||||
|
1,3-ФГК |
3-ФГК |
||||||||||||||
В следующих реакциях низкоэнергетический фосфоэфир переходит в высокоэнергетический фосфат.
8. Фосфоглицератмутаза (3 ФГК 2 ФГК изомераза) осуществляет перенос фосфатного остатка в ФГК из положения 3 положение 2
|
|
COOH |
|
|
|
|
|
|
|
COOH |
||||||||
2 H |
|
|
|
|
|
OH |
|
|
|
|
2 H |
|
|
|
|
|
|
OPO32- |
|
C |
|
|
|
|
|
|
|
|
C |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
OPO |
2- фосфоглицератмутаза |
|
|
|
|
|||||||||
|
|
CH |
|
CH |
OH |
|||||||||||||
|
2 |
3 |
|
|
|
|
|
|
|
|||||||||
|
3-ФГК |
|
|
|
|
|
|
2 |
|
|
||||||||
|
|
|
|
|
|
|
2-ФГК |
|||||||||||
47

9. Енолаза (2 ФГК: гидро лиаза) отщепляет от 2 ФГК молекулу воды и образует высокоэнергетическую связь у фосфора. Ингибируется ионами F .
2H2O
|
|
COOH |
|
Mg2+ |
|
|
COOH |
||||||
2 H |
|
|
|
|
OPO32- |
|
|
|
|
|
|
|
OPO32- |
|
C |
|
|
|
|
2 C |
|
|
|||||
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|||||||
|
Енолаза |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH2OH |
|
|
CH2 |
||||||||
|
|
2-ФГК |
|
|
|
ФЕП |
|||||||
10. Пируваткиназа (АТФ: ПВК 2 фосфотрансфераза) осуществляет субстратное фосфорилирование АДФ с образованием АТФ.
(+М) фруктозо 1,6 дф, глюкозой.
( М) АТФ, НАДН2, глюкагоном, адреналином, аланином, жирными кислотами, Ацетил КоА.
Индуктор: инсулин, фруктоза.
COOH |
2АДФ 2АТФ |
COOH |
|
COOH |
||||||||||||||||
|
|
|
|
OPO32- |
|
Mg2+ |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
2 C |
|
|
|
|
2 C |
|
OH |
|
|
|
2 C |
|
O |
|||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
Пируваткиназа |
|
CH2 |
|
|
CH3 |
|||||||||||||
ФЕП |
|
|
|
|
ПВК (енол) |
|
ПВК (кето) |
|||||||||||||
Образующаяся енольная форма ПВК затем неферментативно переходит в более термодинамически стабильную кетоформу. Данная реакция является последней для аэробного гликолиза. Дальнейший катаболизм 2 ПВК и использование 2 НАДН2 зависит от наличия О2.
Реакция анаэробного гликолиза
В анаэробных условиях ПВК, подобно О2 в дыхательной цепи, обеспечивает регенерацию НАД+ из НАДН2, что необходимо для продолжения реакций гликолиза. ПВК при этом превращается в молочную кислоту. Реакция протекает
вцитоплазме с участием лактатдегидрогеназы (ЛДГ).
11.Лактатдегидрогеназа (лактат: НАД+ оксидоредуктаза). Стоит из 4 субъединиц, имеет 5 изоформ.
COOH |
2НАДН |
2НАД+ |
|
COOH |
||||||||||
2 |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 C |
|
O |
|
|
|
|
|
2 H |
|
C |
|
OH |
||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
||||||||||
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
ЛДГ |
|
|
CH3 |
||||||||
ПВК |
|
|
|
|
|
|
Лактат |
|||||||
|
|
|
|
|
|
|
48 |
|
|
|
|
|
|
|

Лактат не является конечным продуктом метаболизма, удаляемым из организма. Из анаэробной ткани лактат переноситься кровью в печень, где превращаясь в глюкозу (Цикл Кори), или в аэробные ткани (миокард), где превращается в ПВК и окисляется до СО2 и Н2О.
Катаболизм пвк в митохондриях
В аэробных условиях ПВК и водороды с НАДН2 транспортируются в матрикс митохондрий. ПВК самостоятельно не проходит внутреннюю мембрану митохондрий, перенос ее через мембрану осуществляется вторично активным транспортом симпортом с Н+. ПВК в митохондриях используется в 2 реакциях:
Пируватдегидрогеназный комплекс (ПВК: НАД+ оксидорудуктаза
(декарбоксилирующая)) содержит 3 фермента и 5 коферментов: а) Пируватдекарбоксилаза содержит (Е1) 120 мономеров и кофермент ТПФ; б) Дигидролипоилтрансацилаза (Е2) содержит 180 мономеров и коферменты липоамид и HSКоА; в) Дигидролипоилдегидрогеназа (Е3) содержит 12 мономеров и коферменты ФАД и НАД. Пируват ДГ комплекс осуществляет окислительное декарбоксилирование ПВК с образованием Ацетил КоА. Активатор: HSКоА, НАД+, АДФ. Ингибитор: НАДН2, АТФ, Ацетил КоА, жирные кислоты, кетоновые тела. Индуктор инсулин.
|
|
|
|
COOH |
HSKoA НАД+ |
|
НАДН2 CO2 |
SKoA |
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
O |
|
||
|
|
|
|
|
|
|
|
|
Пируватдегидрогеназа |
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
CH |
|
|
|
CH3 |
|
|||||||||||||||||||||||
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
ПВК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
АцетилКоА |
|
|||||||||
|
|
|
Механизм работы Пируват ДГ комплекса. Процесс проходит 5 стадий: |
||||||||||||||||||||||||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
CO2 |
HC |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
E1-ТПФ |
|
|
|
|
|
|
|
|
|
|
E2-ЛК |
|
|
E3-ФАДН2 |
НАД+ |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
||||||||||||||||||||
|
|
|
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
5 |
|||||
COOH |
|
|
|
|
|
|
|
|
SH |
3 |
|
|
|
|
|
|
|
|
|
SH |
|
||||||||||||
|
|
|
|
E1-ТПФ |
|
E2-ЛК |
|
|
|
E2-ЛК |
|
|
|
E3-ФАД |
НАДН2 |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
C O |
|
|
|
|
|
|
|
SH |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
HSKoA |
H C |
|
C |
|
SKoA |
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
C |
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
O |
|
|
|
|
|
|
|
||||||
49
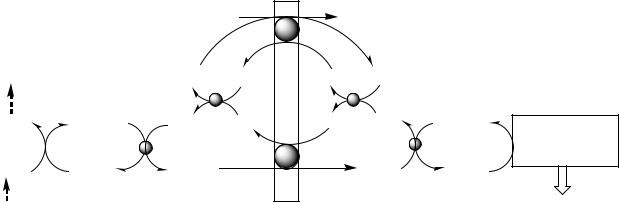
Далее Ацетил КоА поступает в ЦТК, где он окисляется до 2 СО2 с образованием 1 ГТФ, восстановлением 3 НАДН2 и 1 ФАДН2.
Челночные системы
В аэробных условиях О2 обеспечивает регенерацию НАД+ из НАДН2, что необходимо для продолжения реакции гликолиза (НАД+ субстрат 3 ФГА ДГ).
Так как внутренняя мембрана митохондрий непроницаема для НАДН2, восстановленный в гликолизе НАДН2, передает свои водороды на дыхательную цепь митохондрий с помощью специальных систем, называемых «челночными». Известны 2 челночные системы: малат аспартатная и глицерофосфатная.
1. Малат аспартатный челнок является универсальным, работает в печени, почках, сердце.
|
|
|
|
мембрана |
|
|
|
|
|
|
H+ |
транслоказа |
|
|
|
|
|
|
|
H+ |
|
|
|
ПВК |
цитоплазма |
глу |
асп |
асп |
глу |
матрикс митохондрий |
|
|
трансаминаза |
|
|
трансаминаза |
|
||
1,3-ФГК |
НАДН |
ЩУК |
a-КГ |
a-КГ |
ЩУК |
НАДН |
Дыхательная |
|
2 |
малат ДГ |
2 |
||||
|
малат ДГ |
|
цепь |
||||
3-ФГА |
НАД+ |
малат |
|
|
малат |
НАД+ |
|
глюкоза |
|
|
|
транслоказа |
|
3АТФ |
|
|
|
|
|
|
|
||
50
